Los agonistas de los receptores del GLP-1 son una clase de medicamentos cada vez más populares para la pérdida de peso y el manejo de la diabetes. Un mecanismo importante de estos medicamentos es la estimulación gástrica directa de los receptores del GLP-1, lo que lleva a un vaciamiento gástrico retardado y una potencial retención de contenidos gástricos en pacientes que se someten a anestesia. Este artículo explora los retos que estos medicamentos pueden suponer para el profesional de la anestesia.
INTRODUCCIÓN
 Los agonistas de los receptores del péptido similar al glucagón (GLP-1) son una clase emergente y cada vez más popular de medicamentos usados para el tratamiento de la diabetes mellitus de tipo 2 y, más recientemente, de la obesidad. Desde la ampliación de los usos aprobados para incluir la pérdida de peso, estos medicamentos se han hecho cada vez más populares. Uno de los mecanismos de acción de los agonistas del GLP-1 es el retraso del vaciado gástrico.1 Describimos dos casos de pacientes que tomaban agonistas de los receptores GLP-1 y que presentaron volúmenes elevados de contenido gástrico complejo, a pesar del ayuno adecuado y según las guías prácticas de ayuno de la Sociedad Americana de Anestesiología (ASA).2 Dado que el uso de agonistas de los receptores del GLP-1 es cada vez más frecuente, los profesionales de la anestesia deben ser conscientes de estos medicamentos y de los riesgos potenciales que suponen para los pacientes que reciben anestesia.
Los agonistas de los receptores del péptido similar al glucagón (GLP-1) son una clase emergente y cada vez más popular de medicamentos usados para el tratamiento de la diabetes mellitus de tipo 2 y, más recientemente, de la obesidad. Desde la ampliación de los usos aprobados para incluir la pérdida de peso, estos medicamentos se han hecho cada vez más populares. Uno de los mecanismos de acción de los agonistas del GLP-1 es el retraso del vaciado gástrico.1 Describimos dos casos de pacientes que tomaban agonistas de los receptores GLP-1 y que presentaron volúmenes elevados de contenido gástrico complejo, a pesar del ayuno adecuado y según las guías prácticas de ayuno de la Sociedad Americana de Anestesiología (ASA).2 Dado que el uso de agonistas de los receptores del GLP-1 es cada vez más frecuente, los profesionales de la anestesia deben ser conscientes de estos medicamentos y de los riesgos potenciales que suponen para los pacientes que reciben anestesia.
CASO 1:
Una mujer de 60 años se presentó para una resonancia magnética con sedación por claustrofobia. Tenía antecedentes de hipertensión y sobrepeso (índice de masa corporal [BMI] 28 kg/m2). El mes anterior, inició con semaglutide (Ozempic, Novo Nordisk, Plainsboro, NJ) para perder peso (última dosis 7 días antes de la presentación). A pesar del ayuno de comida sólida por más de 18 horas antes de la evaluación, describió sentirse “llena”. Se hizo un ultrasonido gástrico en el punto de atención, que reveló contenido gástrico sólido. Se tomó la decisión de cancelar su estudio de imagenología por temor a un alto riesgo de aspiración durante la administración de la anestesia.
CASO 2:

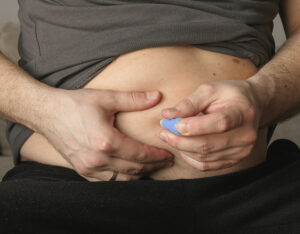
Figura 1: Representa el contenido gástrico en un paciente con agonista del GLP-1 y que ha seguido adecuadamente las directrices de ayuno de la ASA.
Se programó una histerectomía asistida por robot por hiperplasia endometrial para una mujer de 50 años con antecedentes médicos de obesidad de clase 2 (BMI de 37.7 kg/m2), diabetes de tipo 2, hipertensión y apnea obstructiva del sueño. Cabe destacar que anteriormente padecía enfermedad por reflujo gastroesofágico, pero estos síntomas se habían resuelto desde que empezó tirzepatide (Mounjaro, Eli Lilly, Indianapolis, IN) 12.5 mg/0.5 mL pen injector injection (última dosis 2 días antes de la operación). Sus otros medicamentos incluían: metformina, hidroclorotiazida, pregabalina, oxicodona, 5 mg por razón necesaria (uso intermitente con la última dosis el día anterior a la operación), y sertralina. Había estado en ayuno desde la noche anterior a la operación.
La inducción de la anestesia general y la intubación se desarrollaron sin incidentes. Después de la intubación, se colocó una sonda orogástrica y se aspiró el contenido gástrico (Figura 1).
El caso no presento complicaciones desde el punto de vista quirúrgico. Al finalizar el caso, se trasladó a la paciente a la camilla de traslado y se la sentó en previsión de una emergencia. Poco antes de la extubación, desarrolló una emesis de gran volumen de partículas que coincidía con lo que había informado de haber comido varios días antes de la operación (Figura 2). Afortunadamente, el tubo endotraqueal seguía en su sitio y su vía aérea permanecía protegida. Una vez resuelta la emesis, fue extubada sin complicaciones. Se la observó atentamente en la UCPO y no se encontraron pruebas de aspiración gastropulmonar, por lo que se le dio el alta ese mismo día.

Figura 2: Muestra vómito de gran volumen de material particulado en un paciente con agonista del GLP-1, que es coherente con lo que el paciente informó haber comido varios días antes de la operación.
DEBATE
Los agonistas de los receptores GLP-1 son una clase de medicamentos cada vez más populares que se recetan a los pacientes. Estos medicamentos se han descrito como un “gran avance” para la pérdida de peso. El receptor GLP-1 se presenta en diversos sistemas orgánicos, incluyendo el tracto gastrointestinal (GI), el páncreas, el corazón, el hígado y el cerebro. La estimulación de este receptor provoca pérdida de peso, mejora el control glucémico en pacientes diabéticos y mejora los resultados cardíacos y renales. El principal mecanismo de acción está relacionado con la activación de los nervios aferentes vagales que inervan el estómago y con la unión directa a los receptores GLP-1 de las células de la mucosa gástrica, lo que provoca un retraso del vaciado gástrico.1 En los diabéticos, la pérdida de peso combinada con la estimulación de la secreción de insulina de las células beta pancreáticas da lugar a una optimización de la hemoglobina A1c.3 La mejora de los acontecimientos cardíacos agudos graves está probablemente relacionada con la reducción general de los factores de riesgo (p. ej., la disminución del nivel de hemoglobina glucosilada, el control de la presión sanguínea, la disminución del índice de masa corporal, la disminución del nivel de colesterol de lipoproteínas de baja densidad, la mejora de la tasa de filtración glomerular y la disminución de la relación albúmina-creatinina), y con la estimulación directa de los receptores GLP-1 en el miocardio, lo que conduce a una mejor función endotelial y perfusión microvascular.4,5 Son frecuentes los efectos secundarios GI, como náuseas, vómitos o diarrea, pero los síntomas pueden disminuir con el uso continuo.6 También se han descrito casos de pancreatitis aguda y enfermedades biliares y de la vesícula biliar, como la colecistitis. Aunque poco frecuentes, se han descrito reacciones anafilácticas y angioedema.7
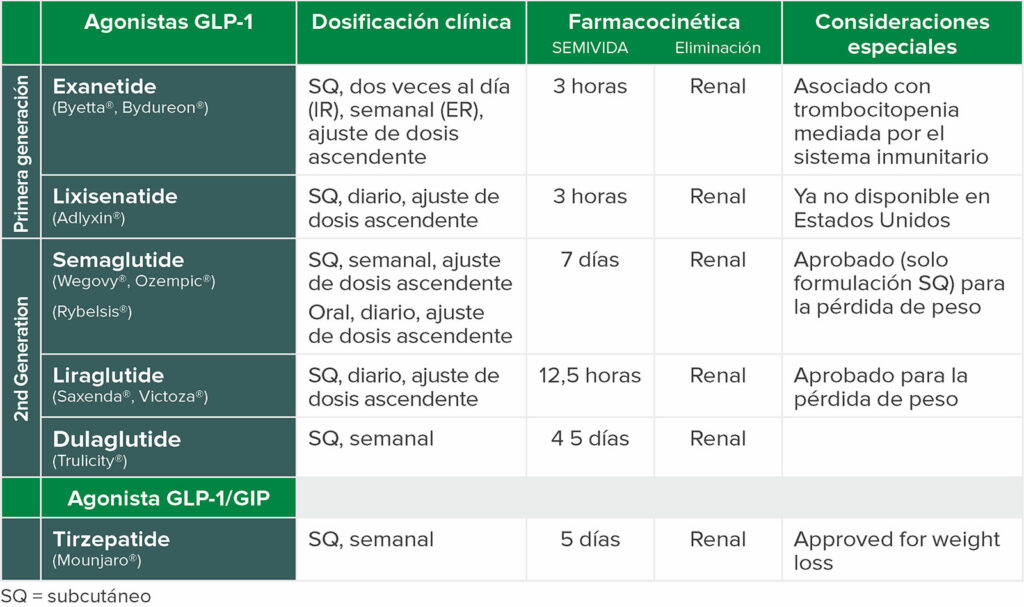
A pesar de los beneficios de esta clase de medicamentos en pacientes obesos y diabéticos, existen riesgos anestésicos potenciales. Los agonistas de los receptores GLP-1 tienen un mecanismo de acción conocido de vaciado gástrico retardado.8 Los medicamentos pueden dar lugar a volúmenes elevados de contenido gástrico complejo, a pesar de un ayuno adecuado, según las guías prácticas de la ASA para el ayuno preoperatorio. Las dos pacientes presentadas en esta serie de casos estaban tomando un agonista del receptor GLP-1 (Tabla 1) para tratar la diabetes y ayudar con la pérdida de peso. Y, aunque la aspiración pulmonar es una complicación poco frecuente en pacientes sometidos a atención anestésica, es algo devastador. Además, está entre los tres principales eventos adversos relacionados con el manejo de las vías aéreas en el proyecto de reclamaciones cerradas de la ASA. 9 La etiología más frecuente de la aspiración está relacionada con la regurgitación pasiva o activa del contenido gástrico.10,11 Por este motivo, el reconocimiento de las poblaciones de pacientes con riesgo elevado de aumento del volumen gástrico es clave para administrar una anestesia segura (Tabla 2).
Tabla 1: Agonistas frecuentes del GLP-1.16,17
Tabla 2: Factores de riesgo para la aspiración
Patología esofágica
|
Alto riesgo de íleo/disfunción intestinal
|
Obstrucción intraabdominal
|
Caso de emergencia |
| Gastroparesia conocida, sospechada o inducida (diabetes de larga data, trastornos neuromusculares, medicamentos, p. ej., agonista del GLP-1) | Caso con duración o complejidad prolongada |
| Embarazo | Sangrado gastrointestinal activo |
- Asai. T. Editorial II: Who is at increased risk of pulmonary aspiration? Br J Anaesth. Oct 2004;93(4):497-500. doi:10.1093/bja/aeh234
- Robinson M, Davidson, A. Aspiration under anaesthesia: risk assessment and decision-making. Continuing Education in Anaesthesia, Critical Care & Pain 2014;14:171-175.
- Beam W. Aspiration Risk Factors. Mayo Clinic Surgical and Procedural Emergency Checklist: Mayo Clinic; 2023.
- Bohman JK, Jacob AK, Nelsen KA, et al. Incidence of gastric-to-pulmonary aspiration in patients undergoing elective upper gastrointestinal endoscopy. Clin Gastroenterol Hepatol. Jul 2018;16(7):1163-1164. doi:10.1016/j.cgh.2017.11.024
Aunque se evitó en estos casos, el riesgo de aspiración pulmonar en pacientes sedados o anestesiados con vías respiratorias desprotegidas es preocupante. En el primer caso, la gran atención prestada a los antecedentes y síntomas de la paciente, combinada con la evaluación con ultrasonido gástrico, llevó a la cancelación del caso y a evitar una situación de alto riesgo para la paciente. En el segundo caso, se observó que la paciente tenía un alto volumen de contenido intragástrico complejo con colocación de sonda orogástrica y emesis de contenido gástrico sólido en el momento de la emergencia que consistió en comida de 2-3 días antes de la operación.
No está claro si el agonista del receptor GLP-1 fue la causa directa del elevado volumen de contenido gástrico remanente, ya que la paciente también padecía diabetes de larga evolución y consumía opiáceos, ambos asociados a la gastroparesia.12,13 Como prueba de nuestra preocupación por los pacientes que toman agonistas de los receptores GLP-1, informamos de un caso clínico reciente que describía a un paciente que tomaba semaglutida y que tuvo un episodio de aspiración con restos de comida durante la inducción de la anestesia, a pesar de haber ayunado durante 18 horas.14 Además, encontramos varias revisiones retrospectivas de pacientes que tomaban agonistas de los receptores GLP-1 y se sometían a una endoscopia, que mostraban un mayor riesgo de retención de contenido gástrico en pacientes que tomaban estos medicamentos.15,16
El grupo de trabajo sobre ayuno preoperatorio de la ASA ha publicado recientemente una guía basada en el consenso sobre el tratamiento preoperatorio de los pacientes que reciben agonistas de los receptores GLP-1 (Figura 3).17 La recomendación del grupo de expertos para las intervenciones electivas es suspender los agonistas de los receptores GLP-1 de dosis diaria el día de la intervención y las fórmulas de dosis semanal una semana antes. El día de la intervención, la recomendación es preguntar específicamente por los síntomas GI, como náuseas, vómitos, dolor abdominal y distensión abdominal, y tener en cuenta la posibilidad de retrasar las intervenciones electivas en pacientes sintomáticos. Si los pacientes son asintomáticos desde el punto de vista GI y se ha mantenido el medicamento según las directrices, la recomendación es proceder con la intervención. En pacientes sin síntomas GI, pero que no han suspendido el medicamento según lo aconsejado, el grupo de trabajo recomienda proceder con precauciones de “estómago lleno” con la consideración de evaluar el volumen gástrico mediante ultrasonido para ayudar en la toma de decisiones. Este grupo señaló que no existen pruebas que sugieran una duración óptima del ayuno.17 Otras organizaciones profesionales, como la Society of Perioperative Assessment and Quality Improvement, también han presentado recomendaciones consensuadas para suspender los agonistas del receptor GLP-1 el día de la operación, a menos que exista una gran preocupación por la disfunción intestinal posoperatoria.18 Dada la larga semivida de la mayoría de los medicamentos de esta clase, no es factible suspender los medicamentos por al menos 5 semividas antes de la operación para permitir la normalización de la función gástrica. Además, dados los potenciales beneficios cardiovasculares y el riesgo insignificante de hipoglucemia, hay un interés por continuar con esta clase de medicamentos sin interrupción perioperatoria.19
Figura 3: Guía basada en el consenso de la Sociedad Americana de Anestesiología sobre el manejo preoperatorio de agonistas del receptor GLP-1*
| Evaluación: Ante las preocupaciones relacionadas con informes de retraso en el vaciamiento gástrico asociado con agonistas del receptor GLP-1, el grupo de trabajo sobre ayuno preoperatorio de la ASA compartió una guía sobre el manejo preoperatorio de estos medicamentos. Para pacientes programados para intervenciones electivas tener en cuenta lo siguiente: Días previos a la intervención:
Día de la intervención:
*Extracto de las directrices basadas en el consenso de la Sociedad Americana de Anestesiología sobre el manejo preoperatorio de pacientes (adultos y niños) con agonistas del receptor del péptido 1 similar al glucagón (GLP-1) https://www.asahq.org/about-asa/newsroom/news-releases/2023/06/american-society-of-anesthesiologists-consensus-based-guidance-on-preoperative. Actualizado el 29 de junio de 2023. Sociedad Americana de Anestesiología. |
En este momento, el enfoque óptimo de estos pacientes aún debe refinarse y esperamos que estudios adicionales ayuden a guiar nuestra toma de decisiones. Es importante un enfoque sistemático para evaluar el riesgo en esta población de pacientes con una historia sensible del uso de medicamentos, síntomas y revisión de comorbilidades. Puede ser prudente reevaluar las directrices tradicionales de ayuno en estos pacientes. El uso de ultrasonido gástrico para definir el contenido gástrico antes de la anestesia puede tenerse en cuenta para pacientes que se presentan para anestesia y toman estos medicamentos, cuando esté disponible.20-22
En el contexto de incertidumbre con respecto al contenido gástrico, podría tenerse en cuenta la inducción de secuencia rápida de la anestesia y la descompresión gástrica antes de la emergencia. También debe reconocerse que el riesgo de emesis y aspiración durante la emergencia es una preocupación real incluso con descompresión gástrica si el paciente tiene contenido gástrico sólido residual.
CONCLUSIÓN
Presentamos dos casos de pacientes en tratamiento con agonistas del receptor GLP-1 con retraso de vaciado gástrico, a pesar de un ayuno preoperatorio adecuado. Reconocemos que es difícil determinar la causa directa del retraso del vaciado gástrico en estas pacientes, ya que existían numerosos factores de riesgo. No obstante, dado que el uso de agonistas del receptor GLP-1 es cada vez más frecuente, los profesionales de la anestesia deben ser conscientes de estos medicamentos y de los riesgos potenciales que suponen para los pacientes que reciben anestesia. Se necesitan más estudios que investiguen la seguridad de estos agentes en relación con el tratamiento cerca del período preanestésico.
William Brian Beam, MD, es profesor adjunto de Anestesiología en Mayo Clinic, Rochester, MN.
Lindsay R. Hunter Guevara, MD, es profesora adjunta de Anestesiología en Mayo Clinic, Rochester, MN.
Las autoras no tienen conflictos de intereses.
REFERENCIAS
- Prillaman M. “Breakthrough” obesity drugs are effective but raise questions. Scientific American. 2023 https://www.scientificamerican.com/article/breakthrough-obesity-drugs-are-effective-but-raise-questions/ Accessed March 9, 2023.
- Joshi GP, Abdelmalak BB, Weigel WA, et al. 2023 American Society of Anesthesiologists practice guidelines for preoperative fasting: carbohydrate-containing clear liquids with or without protein, chewing gum, and pediatric fasting duration—a modular update of the 2017 American Society of Anesthesiologists practice guidelines for preoperative fasting. Anesthesiology. 2023;138:132–151. PMID: 36629465.
- Holst JJ, Orskov C. The incretin approach for diabetes treatment: modulation of islet hormone release by GLP-1 agonism. Diabetes. 2004;53:S197–204. PMID: 15561911.
- Gerstein HC, Sattar N, Rosenstock J, et al. Cardiovascular and renal outcomes with efpeglenatide in type 2 diabetes. N Engl J Med. 2021;385:896–907. PMID: 34215025.
- Heuvelman VD, Van Raalte DH, Smits MM. Cardiovascular effects of glucagon-like peptide 1 receptor agonists: from mechanistic studies in humans to clinical outcomes. Cardiovasc Res. 2020;116:916–930. PMID: 31825468.
- Trujillo J. Safety and tolerability of once-weekly GLP-1 receptor agonists in type 2 diabetes. J Clin Pharm Ther. 2020;45:43–60. PMID: 32910487.
- Ornelas C, Caiado J, Lopes A, et al. Anaphylaxis to long-acting release exenatide. J Investig Allergol Clin Immunol. 2018;28:332–334. PMID: 30350785.
- Urva S, Coskun T, Loghin C, et al. The novel dual glucose-dependent insulinotropic polypeptide and glucagon-like peptide-1 (GLP-1) receptor agonist tirzepatide transiently delays gastric emptying similarly to selective long-acting GLP-1 receptor agonists. Diabetes Obes Metab. 2020;22:1886–1891. PMID: 32519795.
- Bailie R, Posner KL. New trends in adverse respiratory events from ASA Closed Claims Project. ASA Newsletter. 2011;75:28–29. https://pubs.asahq.org/monitor/article-abstract/75/2/28/2553/New-Trends-in-Adverse-Respiratory-Events-From-ASA?redirectedFrom=fulltext Accessed March 9, 2023.
- Mendelson CL. The aspiration of stomach contents into the lungs during obstetric anesthesia. Am J Obstet Gynecol. 1946;52:191–205. PMID: 20993766.
- Warner MA, Warner ME, Weber JG. Clinical significance of pulmonary aspiration during the perioperative period. Anesthesiology. 1993;78:56–62. PMID: 8424572.
- Jung HK, Choung RS, Locke GR, 3rd, et al. The incidence, prevalence, and outcomes of patients with gastroparesis in Olmsted County, Minnesota, from 1996 to 2006. Gastroenterology. 2009;136:1225–1233. PMID: 19249393.
- Camilleri M. Gastroparesis: etiology, clinical manifestations, and diagnosis. UpToDate. 2022. https://www.uptodate.com/contents/gastroparesis-etiology-clinical-manifestations-and-diagnosis Accessed July 5, 2023.
- Klein SR, Hobai IA. Semaglutide, delayed gastric emptying, and intraoperative pulmonary aspiration: a case report (Semaglutide, vidange gastrigue retardee et aspiration pulmonaire peroperatoire: une presentation de case). Can J Anaesth. 2023; Mar 28. PMID: 36977934. Online ahead of print.
- Kobori T, Onishi Y, Yoshida Y, et al. Association of glucagon-like peptide-1 receptor agonist treatment with gastric residue in an esophagogastroduodenoscopy. J Diabetes Investig. 2023:14:767–773. PMID: 36919944.
- Silveira SQ, da Silva LM, de Campos Vieira Abib A, et al. Relationship between perioperative semaglutide use and residual gastric content: a retrospective analysis of patients undergoing elective upper endoscopy. J Clin Anesth. 2023;87:111091. PMID: 36870274.
- Girish PJ, Abdelmalak BB, Weigal WA, et al. American Society of Anesthesiologists consensus-based guidance on preoperative management of patients (adults and children) on glucagon-like peptide-1 (GLP-1) receptor agonists. asahq.org. Updated June 29, 2023. https://www.asahq.org/about-asa/newsroom/news-releases/2023/06/american-society-of-anesthesiologists-consensus-based-guidance-on-preoperative Accessed July 5, 2023.
- Pfeifer KJ, Selzer A, Mendez CE, et al. Preoperative management of endocrine, hormonal, and urologic medications: Society for Perioperative Assessment and Quality Improvement (SPAQI) consensus statement. Mayo Clin Proc. 2021;96:1655–1669. PMID: 33714600.
- Hulst AH, Polderman JAW, Siegelaar SE, et al. Preoperative considerations of new long-acting glucagon-like peptide-1 receptor agonists in diabetes mellitus. Br J Anaesth. 2021;126:567–571. PMID: 33341227.
- Kruisselbrink R, Gharapetian A, Chaparro LE, et al. Diagnostic accuracy of point-of-care gastric ultrasound. Anesth Analg. 2019;128:89–95. PMID: 29624530.
- Cubillos J, Tse C, Chan VW, Perlas A. Bedside ultrasound assessment of gastric content: an observational study. Can J Anaesth. 2012;59:416–423. PMID: 22215523.
- Schwisow S, Falyar C, Silva S, Muckler VC. A protocol implementation to determine aspiration risk in patients with multiple risk factors for gastroparesis. J Perioper Pract. 2022;32:172–177. PMID: 34251910.


 Issue PDF
Issue PDF