Hipertermia maligna frente a síndromes similares a la MH inducidos por medicamentos
Los profesionales de anestesia reconocen la hipertermia maligna (MH) en el período perioperatorio como un síndrome hipermetabólico que evoluciona rápido y que puede ser mortal, y que se desencadena en el músculo en personas genéticamente susceptibles cuando se les administran anestésicos inhalatorios o succinilcolina. A menos que se reconozca y se trate sin demoras suspendiendo la administración del medicamento que la desencadenó, administrando dantrolene por vía intravenosa y aplicando otras medidas de apoyo, la crisis de MH tiene un alto índice de morbilidad y mortalidad. Los signos de MH que evolucionan rápido incluyen un aumento rápido de la temperatura, de frecuencia cardíaca (HR), la producción de CO2, el CO2 al final de la espiración, la frecuencia respiratoria (RR), la ventilación por minuto espontánea o mecánica, un aumento en el tono muscular y rigidez, e insuficiencia multiorgánica generalizada (MOSF). La lesión muscular puede provocar insuficiencia renal, incluso si la crisis de MH se trata de manera eficaz. La fiebre sumada a necesidades metabólicas no cubiertas, junto con insuficiencia cardíaca y microcirculatoria, puede provocar una coagulopatía, disfunción hepática, otro episodio de MOSF y la muerte.1,2
Los profesionales de anestesia conocen muy bien la MH porque la desencadenan los anestésicos. Dado que la intervención de anestesia causa la crisis de MH, esta se ha convertido en un problema relacionado con la anestesia. Sin embargo, hay otras condiciones hipermetabólicas inducidas por medicamentos que se producen por una actividad anormal del sistema nervioso central (SNC) y provocan señales similares a las de una crisis de MH (ver la tabla 1).3 Además, los anestésicos o las intervenciones de anestesia podrían contribuir a estas crisis o precipitarlas. Dichas crisis en el SNC pueden presentarse en el período perioperatorio extendido con señales similares a la MH, como hipermetabolismo (aumento de la HR, la RR, la temperatura y la producción de dióxido de carbono), anomalías en la actividad motora, anomalías en la actividad mental e insuficiencia cardiorrespiratoria progresiva. Aunque estas crisis inducidas por medicamentos se observan con mayor frecuencia en urgencias, neurología, psiquiatría y cuidados intensivos como emergencias que evolucionan rápido, también pueden producirse cerca del momento de una cirugía. Las condiciones hipermetabólicas de origen central inducidas por medicamentos son importantes para profesionales de anestesia porque pueden observarlas en el período perioperatorio, no son MH (aunque se parezcan a la MH) y podrían presentar exigencias de tratamiento distintas para evitar la morbilidad y la mortalidad. Aunque estas no se producen principalmente por anestésicos, algunas se pueden precipitar por medicamentos que con frecuencia se administran o se dejan de administrar de forma temporal en el período perioperatorio. La fiebre asociada a la crisis de MH y a estas condiciones hipermetabólicas de origen central, no responde bien a los antipiréticos. Los anticolinérgicos y los antipsicóticos con efectos anticolinérgicos están relativamente contraindicados porque inhiben la disipación del calor y la sudoración.4 El dantrolene es un antídoto específico para la crisis de MH debido a su acción directa en el músculo, pero también podría ser útil para controlar la fiebre que causa la hiperactividad muscular y el calor que producen estos problemas del SNC y de otro tipo.5-8
Tabla 1: Señales y síntomas similares a la MH.
| Aumento de la temperatura |
| Taquicardia |
| Taquipnea |
| Hipercapnia en aumento, en especial, con ventilación controlada y fija |
| Confusión, agitación y alteraciones en la actividad mental |
| Rigidez en los músculos, calambres, temblores, espasmos |
| Hipertensión/Hipotensión |
| Arritmia cardíaca |
La línea directa de MH atendida por voluntarios, financiada por donaciones y por la Asociación de Hipertermia Maligna de los Estados Unidos (Malignant Hyperthermia Association of the United States, MHAUS), recibe llamadas de profesionales de anestesia y cirugía, miembros del personal de enfermería perioperatoria y otras personas que tienen preguntas sobre la identificación y el tratamiento de las crisis de MH, el tratamiento posterior a una crisis y otras condiciones que se asemejan a la MH (https://www.mhaus.org). Tras analizar las llamadas a la línea directa de MH, se observa que algunas de estas llamadas están relacionadas con condiciones similares a la MH inducidas por medicamentos o toxinas (datos no publicados; comunicación personal del autor con la base de datos de la línea directa de la MHAUS).
Los síndromes similares a la MH inducidos por medicamentos incluyen el síndrome maligno por neurolépticos (NMS), el síndrome de parkinsonismo-hiperpirexia (PHS), el síndrome serotoninérgico (SS), la suspensión de la administración de baclofeno, y la intoxicación con estimulantes como las anfetaminas, la MDMA y la cocaína, y con drogas psicoactivas como la fenciclidina (PCP o “polvo de ángel”) y la dietilamida del ácido lisérgico (LSD) (ver la tabla 2). Aunque el entorno clínico de estos síndromes suele no ser perioperatorio y aunque el cuadro clínico inicial puede no ser tan fulminante como el de la MH típica, estas condiciones también pueden causar problemas médicos potencialmente mortales que el equipo de anestesia y cirugía debe tratar durante la operación y después de ella. Además, es evidente que se debe diferenciar a estos problemas inducidos por medicamentos y de rápida evolución de los efectos inflamatorios y neurológicos centrales que se producen por condiciones orgánicas como la encefalitis, la sepsis, un absceso en el SNC, un tumor, un traumatismo de cráneo y algunas apoplejías. Además, la confusión acompañada por hipermetabolismo se observa en el hipertiroidismo, la insolación y la catatonía letal sin tratar.
Tabla 2: Condiciones similares a la MH inducidas por medicamentos.
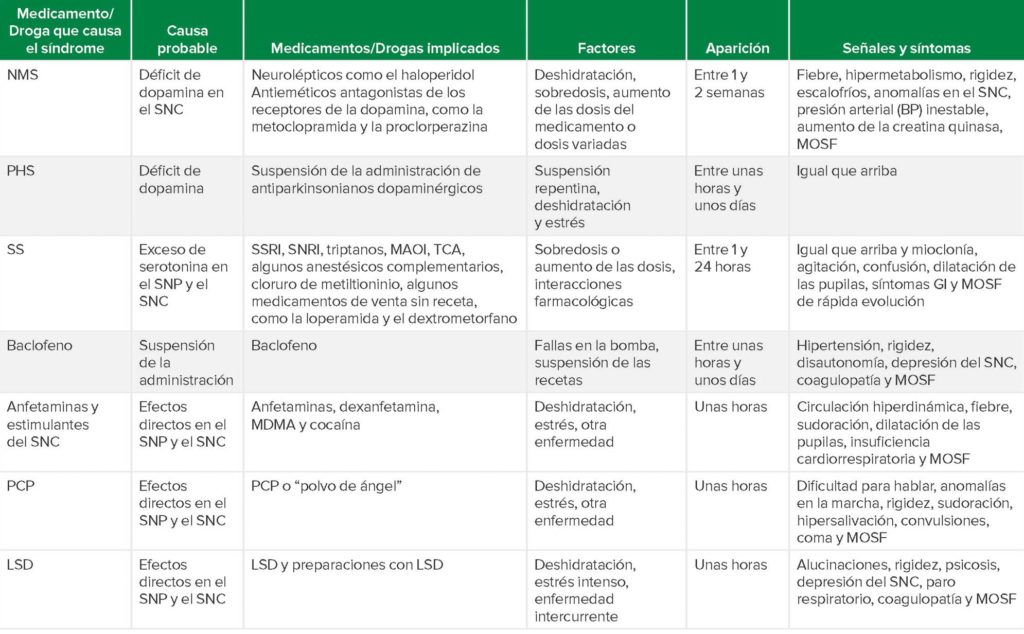
Abreviaturas de la tabla: NMS (síndrome maligno por neurolépticos), SNC (sistema nervioso central), SNP (sistema nervioso periférico), MOSF (insuficiencia multiorgánica generalizada), PHS (síndrome de parkinsonismo-hiperpirexia), SS (síndrome serotoninérgico), SSRI (inhibidores selectivos de la recaptación de serotonina), SNRI (inhibidores selectivos de la recaptación de noradrenalina), triptanos (un tipo de medicamentos derivados de la triptamina que se administran para tratar las migrañas y la cefalea en brotes), TCA (antidepresivos tricíclicos), MAOI (inhibidores de la monoaminoxidasa), GI (gastrointestinales), MDMA (3,4-metilendioximetanfetamina o “éxtasis”), PCP (fenciclidina o “polvo de ángel”), LSD (dietilamida del ácido lisérgico).
Síndrome maligno por neurolépticos (NMS)
El NMS es una condición relativamente infrecuente que se asocia a la administración de dosis crónicas o ascendentes de medicamentos neurolépticos que bloquean la actividad dopaminérgica del cerebro. Los neurolépticos se administran como sedación, control del comportamiento y tratamiento de trastornos psicóticos. Después de una operación, se podrían administrar para el control del comportamiento en un cuadro confusional durante la recuperación postanestésica, por sus propiedades antieméticas o en la UCI después de una cirugía. Las personas que reciben estos medicamentos y que están enfermas, deshidratadas, agitadas o catatónicas son más susceptibles a tener el NMS. Los neurolépticos “ocultos”, como la proclorperazina, también pueden provocar el NMS. Estos medicamentos se administran a menudo en el período perioperatorio para tratar o prevenir las náuseas. Las señales hipermetabólicas, con fiebre, anomalías en la actividad muscular (incluyendo rigidez) y anomalías en la actividad mental, pueden aparecer en cuestión de horas y hasta una o dos semanas después del inicio de la administración de los neurolépticos. La evolución de estas señales suele revertirse con el tiempo cuando se suspende la administración de los agentes que las causan, pero, si no se identifica el NMS, este puede evolucionar hasta provocar daños musculares, insuficiencia cardiorrespiratoria y la muerte. El tratamiento básico implica el diagnóstico precoz, la suspensión de la administración de los neurolépticos y atención médica de apoyo. Ya que no se han hecho ensayos aleatorizados controlados, se han utilizado benzodiacepinas, medicamentos dopaminérgicos como la bromocriptina o la amantadina, el dantrolene y la terapia electroconvulsiva (ECT) con distintos grados de éxito. El diagnóstico del NMS no se puede determinar ni con análisis de laboratorio ni con los síntomas que presenta el paciente. El diagnóstico requiere antecedentes médicos y un examen completo, además de la eliminación de cualquier otra condición orgánica o inducida por medicamentos.9,10 Si se sospecha que el paciente tiene el NMS, el Servicio de Información sobre el Síndrome Maligno por Neurolépticos (Neuroleptic Malignant Syndrome Information Service, NMSIS), patrocinado por la MHAUS, proporciona bibliografía y apoyo telefónico o por correo electrónico en su sitio web (www.NMSIS.org).
Síndrome de parkinsonismo-hiperpirexia (PHS)
El PHS se produce por la suspensión de la administración de dopaminérgicos de acción central que controlan la rigidez muscular, el retraso motor y otros síntomas de la enfermedad de Parkinson. A menudo, los síntomas fluctúan, y las dosis de los medicamentos podrían variar porque los pacientes se vuelven relativamente resistentes a los dopaminérgicos. A veces, se suspende la administración de dopaminérgicos durante una hospitalización por una condición médica o quirúrgica aguda para minimizar los efectos secundarios en el sistema nervioso autónomo. El PHS, una condición semiaguda que se asemeja al NMS y a la MH, podría producirse después de la suspensión repentina del tratamiento farmacológico contra la enfermedad de Parkinson. Este síndrome se reporta en hasta el 4 % de los pacientes a quienes se suspende la administración de dopaminérgicos de forma repentina, y aproximadamente un tercio de los pacientes que tienen el síndrome presentan secuelas a largo plazo.11 Se observan fiebre, anomalías en la actividad muscular y otras señales de hipermetabolismo con disautonomía. El PHS podría precipitarse por la deshidratación, una infección y otros factores de estrés para el organismo, o después de la administración de antidopaminérgicos de acción central, como el droperidol, o neurolépticos, como el haloperidol. También se puede producir en pacientes con enfermedad de Parkinson tras una pérdida brusca de la estimulación cerebral profunda (DBS) para dicha enfermedad o tras la implantación de electrodos para la DBS.12,13 Aunque el NMS es una condición potencialmente mortal causada por medicamentos que bloquean la dopamina de origen central, el PHS se produce por la suspensión de un tratamiento con dopaminérgicos. Por este motivo, se debe evitar la suspensión total del tratamiento con dopaminérgicos en el período perioperatorio, si es posible. Además, los pacientes a quienes se suspendió la administración de antiparkinsonianos en el período perioperatorio deben retomar el tratamiento lo antes posible.14
Síndrome serotoninérgico (SS)
El SS se suele observar cuando se administran simultáneamente varios medicamentos que aumentan los niveles de serotonina de origen central, pero también puede producirse tras la administración de una dosis única o una sobredosis de uno o más serotoninérgicos. La serotonina o 5-hidroxitriptamina, una monoamina derivada del triptófano, es un neurotransmisor que está en el cerebro, en los intestinos y en las plaquetas. La serotonina modula una amplia gama de acciones del sistema nervioso central (SNC) y del sistema nervioso periférico (SNP) que incluyen la regulación del estado de ánimo, el apetito, el sueño, algunas funciones cognitivas, la agregación plaquetaria y la contracción de los músculos lisos del útero, los bronquios y los vasos sanguíneos pequeños.15 Por consiguiente, se han diseñado varios antidepresivos para manipular los niveles de serotonina en el SNC. Estos incluyen los inhibidores selectivos de la recaptación de serotonina (SSRI), los inhibidores selectivos de la recaptación de noradrenalina (SNRI), los antidepresivos tricíclicos (TCA) y los inhibidores de la monoaminoxidasa (MAOI). Se ha informado de que el SS tiene una incidencia del 0,9 % al 2 % en los pacientes que reciben tratamiento crónico y una incidencia máxima del 14 % al 16 % tras una sobredosis.16 Los SSRI y los SNRI son los que se asocian con mayor frecuencia al SS. Los anestésicos complementarios que se administran con frecuencia y otras clases importantes de medicamentos (incluyendo algunos de venta sin receta) podrían contribuir al SS o precipitarlo (ver la tabla 3).17-20
Tabla 3: Algunos medicamentos que pueden causar o potenciar el síndrome serotoninérgico.
| Antidepresivos | Triptanos |
| SSRI Citalopram Fluoxetina Fluvoxamina Paroxetina TrazodonaSNRI Duloxetina Sibutramina Venlafaxina Tricíclicos MAOI |
Almotriptán Eletriptán Frovatriptán Naratriptán Rizatriptán Sumatriptán Zolmitriptán |
| Anestésicos complementarios | Otros |
| Cocaína Petidina Metadona Ondansetrón Tramadol Fentanilo |
Buspirona ciclobenzaprina Dextrometorfano ergotamina 5-Hidroxitriptófano linezolid Loperamida Cloruro de metiltioninio Hierba de San Juan |
El SS puede provocar alteraciones en el estado mental, disautonomía, hipotensión, rigidez neuromuscular, agitación, clonus en los músculos oculares y periféricos, diaforesis y fiebre.
La aparición de los síntomas puede ser repentina tras la administración o la sobredosis del medicamento. El SS puede presentarse como un síndrome hipermetabólico e hipertérmico difícil de distinguir del NMS, el PHS y la MH. Como sucede con el NMS y el PHS, la evolución de los síntomas podría provocar insuficiencia cardiorrespiratoria, daño muscular, lesión multiorgánica y la muerte. La incidencia del SS podría subestimarse, quizá, por los casos leves que se pasan por alto o porque los cuadros más graves pueden emular otras causas. Por lo tanto, puede ser que el SS sea más frecuente en el período perioperatorio de lo que sabemos. Es importante que los profesionales de anestesia recuerden que varios anestésicos complementarios que administramos con frecuencia pueden provocar el SS o aumentar el riesgo de sufrirlo. El tratamiento implica la suspensión de la administración de todos los medicamentos que contribuyan al exceso de serotonina, junto con un tratamiento de apoyo.15,16 Aunque no está demostrado, algunas autoridades recomiendan la administración de ciproheptadina, un antagonista del receptor 2a de la 5-hidroxitriptamina de origen central, porque se considera que dicho receptor es uno de los principales factores de activación de la hipertermia a nivel central en el SS.16,21,22
Suspensión de la administración de baclofeno
Se ha informado de casos de NMS y reacciones similares a la MH tras la suspensión de la administración de baclofeno. El baclofeno mejora los efectos centrales del ácido gamma-aminobutírico (GABA), que es un neurotransmisor que inhibe al sistema nervioso central (SNC). Con frecuencia, los profesionales de anestesia y otros especialistas en dolor administran el baclofeno por vía oral o mediante una inyección directa/infusión en el líquido cefalorraquídeo para controlar la espasticidad después de que se produzcan daños en el SNC en condiciones como la parálisis cerebral, la lesión de médula ósea y distonía. Ya que los especialistas en anestesia y dolor administran baclofeno, es frecuente que participen en la recarga de la bombas de infusión, en la evaluación de una bomba de baclofeno con fallas o en la prescripción de una receta de baclofeno para un colega. En consecuencia, es importante que los miembros del equipo de atención anestésica sepan que el síndrome similar a la MH que se produce después de la suspensión repentina de la administración de baclofeno, con una deficiencia relativa de GABA en el SNC, puede causar síntomas graves, como fiebre, anomalías en la actividad mental, hiperactividad en el sistema nervioso autónomo, dificultad respiratoria, rabdomiólisis y coagulopatía. El tratamiento implica atención médica de apoyo y la reanudación del tratamiento con baclofeno.23
Drogas recreativas
Algunos estimulantes del SNC que se consumen con fines “recreativos” o en sobredosis causan condiciones hipermetabólicas que podrían asemejarse a una crisis de MH con efectos directos en el SNP y en el SNC. Estos incluyen las anfetaminas, la dextroanfetamina, la metanfetamina, la MDMA (metilendioximetanfetamina), la cocaína y las drogas psicoactivas, como la PCP y el LSD. Aunque con los antecedentes de consumo de drogas y con pruebas toxicológicas se suelen identificar estos problemas antes de una cirugía de emergencia por un traumatismo u otras condiciones agudas, estas drogas “recreativas” podrían encontrarse en pacientes que se harán una cirugía programada. Al igual que algunos pacientes se premedican a sí mismos con alcohol o marihuana “medicinal” antes de una cirugía para controlar la ansiedad, los consumidores habituales de estos psicoactivos podrían hacer lo mismo. Aunque los primeros síntomas subjetivos difieren cuando hace efecto cada una de estas drogas, todas podrían provocar señales de hiperactividad simpática, anomalías en la actividad motora, fiebre, e hipermetabolismo con insuficiencia cardiorrespiratoria y MOSF en el período perioperatorio. Los pacientes que se presenten para una cirugía y tengan anomalías en la actividad mental, señales de hiperactividad simpática y otros síntomas inusuales que no se deban a su problema médico principal deben hacerse pruebas toxicológicas si es posible.
Conclusión
Si bien los profesionales de anestesia conocen la MH como una crisis perioperatoria, es importante saber que, en el período perioperatorio, podrían observarse otros síndromes hipermetabólicos inducidos por medicamentos. Desde luego, los anestésicos complementarios que se administran de manera habitual podrían contribuir a estos síndromes o precipitarlos. El dantrolene sódico es el medicamento fundamental para tratar la crisis de MH, pero no es específico en el sentido de que podría aliviar algunas de las señales hipermetabólicas de otras condiciones. Dado que estas condiciones pueden asemejarse mucho a la crisis de MH y que el dantrolene podría controlar algunos de los síntomas, un diagnóstico incorrecto de MH podría retrasar o impedir la aplicación de otro tratamiento eficaz.
Charles Watson, MD, es asesor voluntario de la línea directa de MH para la Asociación de Hipertermia Maligna de los Estados Unidos (MHAUS), en Sherburne, NY.
Stanley Caroff, MD, es profesor de Psiquiatría en la Facultad de Medicina de la Universidad de Pennsylvania, dirige el Servicio de Información sobre el Síndrome Maligno por Neurolépticos (NMSIS) y es un ejecutivo de la MHAUS.
Henry Rosenberg, MD, es el presidente de la MHAUS.
Dres. Watson y Rosenberg no tienen conflictos de intereses.
El Dr. Caroff es asesor de Neurocrine Biosciences, Teva Pharmaceuticals. También ha recibido becas de investigación de Neurocrine Biosciences, Osmotica Pharmaceuticals, Eagle Pharmaceuticals.
Referencias
- Rosenberg H, Davis M, James D, et al. Malignant hyperthermia. Orphanet Journal of Rare Diseases. 2007:2:21.
- Rosenberg H, Hall D, Rosenbaum H. Malignant hyperthermia. In: Brendt J, ed. Critical Care Toxicology. Elsevier-Mosby; 2005:291–304.
- Parness J, Rosenberg H, Caroff SN. Malignant hyperthermia and related conditions. In: Kellum JA, Fortenberry JD, Fuchs BD & Shaw A, eds. Clinical Decision Support: Critical Care Medicine. Wilmington, Delaware: Decision Support in Medicine, LLC: 1913.
- Mann SC. Thermoregulatory mechanisms and antipsychotic drug-related heatstroke. In: Mann SC, Caroff SN, Keck PE, Lazarus A, eds. Neuroleptic Malignant Syndrome and Related Conditions. 2nd Ed. Washington, DC: American Psychiatric Publishing; 2003:45–74.
- Goulon M, de Rohan-Chabot P, Elkharrat D, et al. Beneficial effects of dantrolene in the treatment of neuroleptic malignant syndrome: a report of two cases. Neurology. 1983;33:516–518.
- Pawat SC, Rosenberg H, Adamson R, et al. Dantrolene in the treatment of refractory hyperthermic conditions in critical care: a multicenter retrospective study. Open Journal of Anesthesiology. 2015;5:63–71.
- Hadad E, Cohen-Sivan Y, Heled Y, et al. Clinical review: treatment of heat stroke: should dantrolene be considered? Crit Care. 2005;9:86–91.
- Shih TH, Chen KH, Pao SC, et al. Low dose dantrolene is effective in treating hyperthermia and hypercapnea, and seems not to affect recovery of the allograft after liver transplantation: case report. Transplantation Proceedings. 2010; 42:858–860.
- Caroff SN, Rosenberg H, Mann SC, et al. Neuroleptic malignant syndrome in the perioperative setting. Am J Anesthesiology. 2001; 28: 387–393.
- Caroff SN. Neuroleptic malignant syndrome. In: Mann SC, Caroff SN, Keck PE, Lazarus A, eds. Neuroleptic Malignant Syndrome and Related Conditions. 2nd Ed. Washington, DC: American Psychiatric Publishing; 2003:1–44.
- Newman EJ, Grosset DG, Kennedy, PGE. The parkinsonism-hyperpyrexia syndrome. Neurocrit Care 2009;10:136–140.
- Artusi CA, Merola A, Espay AJ, et al. Parkinsonism-hyperpyrexia syndrome and deep brain stimulation. J Neurol. 2015; 262:2780–2782.
- Caroff SN. Parkinsonism-hyperthermia syndrome and deep brain stimulation. Can J Anaesth. 2017;64:675–676.
- Newman EJ, Grossett DG, Kennedy PG. The parkinsonism-hyperpyrexia syndrome. Neurocrit Care. 2009;10:136–140.
- Frazer A, Hensler JG. Serotonin involvement in physiological function and behavior. In: Siegel GJ, Agranoff BW, Albers RW, et al., editors. Basic Neurochemistry: Molecular, Cellular and Medical Aspects. 6th edition. Philadelphia: Lippincott-Raven; 1999. Available from: https://www.ncbi.nlm.nih.gov/books/NBK27940/ Accessed December 12, 2020.
- Francescangeli J, Karamchandani K, Powell M, et al. The serotonin syndrome: from molecular mechanisms to clinical practice. Int J Mol Sci. 2019;20:2288.
- Nguyen H, Pan A, Smollin C, et al. An 11-year retrospective review of cyproheptadine. J Clin Pharm Ther. 2019;44:327–334. doi: 10.1111/jcpt.12796
- Basta MN. Postoperative serotonin syndrome following methylene blue administration for vasoplegia after cardiac surgery: a case report and review of the literature. Semin Cardiothoracic Vasc Anes. 2020: 1089253220960255. (pre-pub)
- Orlova Y, Rizzoli P, Loder E. Association of coprescription of triptan antimigraine drugs and selective serotonin reuptake inhibitor or selective norepinephrine reuptake inhibitor antidepressants with serotonin syndrome. JAMA Neurol. 2018;75:566–572.
- Boyer EW, Shannon M. The serotonin syndrome. N Engl J Med. 2005;352:1112–1120.
- Simon L, Kennaghan M. Serotonin syndrome [review]. StatPearls. NCBI Bookshelf. 2020:5. Published Jan 2020, Accessed October 2020.
- Nguyen H, Pan A, Smollin C, et al. An 11-year retrospective review of cyproheptadine use in serotonin syndrome cases reported to the California Poison Control System. J Clin Pharm Ther. 2019:44;327–334.
- Coffey RJ, Edgar TS, Francisco GE, et al. Abrupt withdrawal from intrathecal baclofen: recognition and management of a potentially life-threatening syndrome. Arch Phys Med Rehabil. 2002;83:735–741.


 Issue PDF
Issue PDF