Hipertermia maligna x síndromes semelhantes à HM induzidas por medicamento
Os profissionais de anestesia reconhecem a hipertermia maligna (HM) no período perioperatório como uma síndrome hipermetabólica com risco de vida de progressão rápida que é desencadeada no músculo de indivíduos geneticamente suscetíveis por agentes anestésicos inalatórios potentes e/ou succinilcolina. A menos que seja reconhecida e tratada rapidamente pela retirada do(s) agente(s) desencadeante(s), dantroleno sódico intravenoso e outras medidas de suporte, a crise de HM tem alta morbidade e mortalidade. Os sinais de evolução para HM incluem aumento rápido da temperatura, frequência cardíaca (FC), produção de CO2, CO2 expirado, frequência respiratória (FR), ventilação minuto espontânea ou necessária, aumento do tônus muscular com rigidez e falência de múltiplos órgãos e sistemas (FMOS). A lesão muscular pode levar à insuficiência renal, mesmo quando a crise de HM é tratada de forma eficaz. Febre com demanda metabólica não atendida junto com insuficiência cardíaca e microcirculatória pode levar a coagulopatia, disfunção hepática, outra FMOS e óbito.1,2
A HM é mais conhecida pelos anestesiologistas porque é desencadeada por drogas anestésicas. Como a intervenção anestésica causa uma crise de HM, ela se tornou um problema relacionado à anestesia. Mas existem outras condições hipermetabólicas induzidas por medicamentos que são causadas por atividade anormal do sistema nervoso central (SNC) e têm sinais semelhantes aos de uma crise de HM (ver Tabela 1).3 Além disso, medicamentos anestésicos ou intervenções podem contribuir ou precipitar tais crises. Essas crises do SNC podem se manifestar no período perioperatório prolongado com sinais de hipermetabolismo semelhantes aos da HM (FC, FR, temperatura e produção de dióxido de carbono elevadas), atividade motora anormal, estado mental anormal e insuficiência cardiorrespiratória progressiva. Embora essas crises induzidas por medicamentos sejam mais frequentemente vistas pela medicina de emergência, neurologia, psiquiatria e prestadores de cuidados intensivos como emergências médicas em evolução, elas também podem ocorrer no momento da cirurgia. As condições hipermetabólicas centrais relacionadas aos medicamentos são importantes para os profissionais de anestesia porque podem ser observadas no período perioperatório, não constituem HM (embora possam se assemelhar à HM) e podem ter diferentes requisitos de manejo para evitar morbidade e mortalidade. Embora não sejam causadas majoritariamente por drogas anestésicas, algumas podem ser precipitadas por drogas comumente administradas ou suspensas no período perioperatório. A febre associada à crise de HM e essas condições hipermetabólicas centrais respondem mal aos medicamentos antipiréticos. Os medicamentos anticolinérgicos e antipsicóticos com efeitos anticolinérgicos são relativamente contraindicados porque inibem a dissipação de calor e a sudorese.4 Dantroleno sódico é um antídoto específico para a crise de HM devido à sua ação direta no músculo, mas também pode ser útil no controle da febre causada pela hiperatividade muscular e a produção de calor causada por estes problemas do SNC e outros.5-8
Tabela 1: Sinais e sintomas semelhantes à HM.
| Aumento de temperatura |
| Taquicardia |
| Taquipneia |
| Hipercarbia crescente – especialmente com ventilação fixa e controlada |
| Confusão, agitação, estado mental alterado |
| Rigidez muscular, cãibras, tremores, espasmos |
| Hipertensão ou hipotensão |
| Arritmia cardíaca |
A Linha Direta de HM, atendida por voluntários e financiada por doações e pela Malignant Hyperthermia Association of the United States [MHAUS] recebe ligações de anestesiologistas, cirurgiões, equipes de enfermagem perioperatória e outros com perguntas sobre o reconhecimento e manejo de crises de HM, manejo pós-crise e outras condições que se assemelham à MH. (https://www.mhaus.org) A revisão das ligações feitas à Linha Direta mostra que algumas delas estão associadas a condições semelhantes à HM induzidas por medicamentos ou toxinas (dados não publicados; comunicação pessoal do autor com a MHAUS Hotline Database).
Entre as síndromes semelhantes à HM induzidas por medicamentos estão a síndrome maligna dos neurolépticos (SMN), a síndrome de parkinsonismo/hipertermia (SPH), a síndrome da serotonina (SS), abstinência de baclofeno, intoxicação causada por estimulantes como anfetamina, MDMA e cocaína, e por drogas psicoativas como a fenciclidina (PCP, “pó de anjo”) e dietilamida do ácido lisérgico (LSD) (ver Tabela 2). Embora o cenário clínico geralmente não seja perioperatório e a apresentação possa não ser tão fulminante como a HM clássica, essas condições também podem representar problemas médicos com risco de vida que a equipe de anestesia e cirúrgica tem que tratar no intra e pós-operatório. E, é claro, esses problemas induzidos por medicamentos em evolução devem ser diferenciados dos efeitos inflamatórios e neurológicos centrais de condições orgânicas como encefalite, sepse, abscesso do SNC, tumor, traumatismo craniano e alguns AVCs. Além disso, confusão, juntamente com hipermetabolismo, é observada com tireotoxicose, insolação e catatonia letal não tratada.
Tabela 2: Condições semelhantes à HM induzidas por medicamentos.
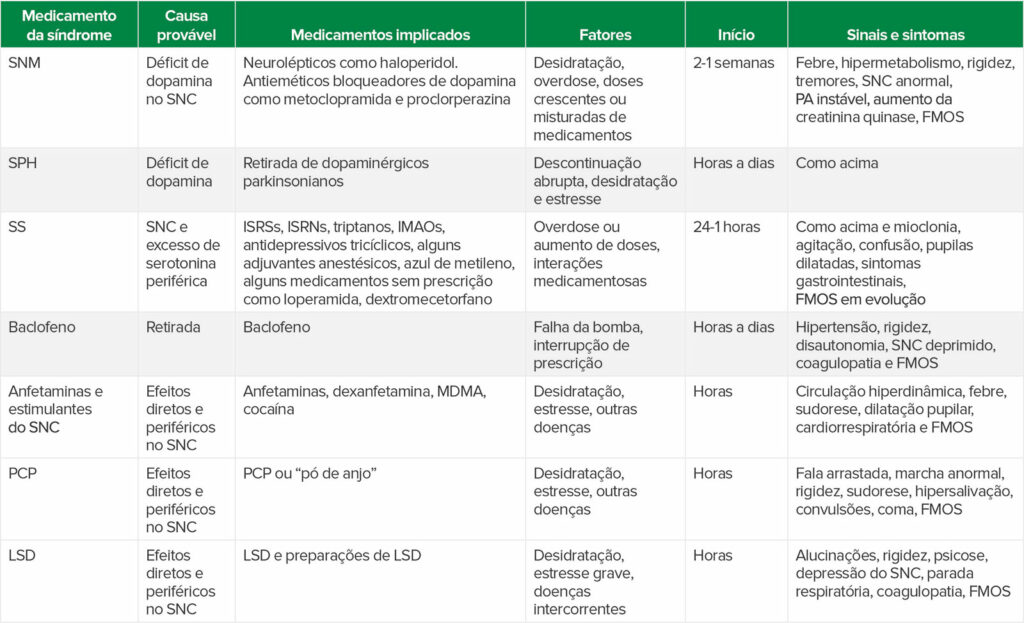
Abreviaturas da tabela: SNM (síndrome neuroléptica maligna), SNC (sistema nervoso central), FMOS (falência múltipla de órgãos e sistemas), SPH (síndrome de parkinsonismo-hiperpirexia), SS (síndrome da serotonina), ISRSs (inibidores seletivos da recaptação da serotonina), ISRNs (inibidores seletivos da recaptação da norepinefrina), triptanos (uma classe de medicamentos à base de triptamina usada para tratar enxaquecas e dores de cabeça em salvas), IMAOs (inibidores da monoamina oxidase), MDMA (3,4-metilenodioxi-metanfetamina ou “ectasy”), PCP (fenciclidina ou “pó de anjo”), LSD (dietilamida de ácido lisérgico).
Síndrome neuroléptica maligna (SNM)
A SNM é uma condição relativamente rara associada à administração de doses crônicas ou crescentes de drogas neurolépticas que bloqueiam a atividade dopaminérgica no cérebro. Os neurolépticos são administrados para sedação, controle comportamental e manejo de distúrbios psicóticos. No pós-operatório, eles podem ser usados para controle comportamental durante o delírio pós-operatório, para propriedades antieméticas ou na UTI após a cirurgia. Indivíduos que tomam esses medicamentos e estão doentes, desidratados, agitados ou catatônicos são mais suscetíveis à SNM. Neurolépticos “ocultos” como a proclorperazina também podem desencadear a SNM. Frequentemente, são administrados no perioperatório para náusea ou profilaxia de náusea. O aparecimento de sinais hipermetabólicos com febre, atividade muscular anormal (incluindo rigidez) e estado mental anormal podem ser vistos dentro de horas e até uma ou duas semanas após o início dos neurolépticos. A progressão desses sinais geralmente é revertida com o tempo quando os agentes causadores são descontinuados, mas a SNM não reconhecida pode progredir para lesão muscular, insuficiência cardiorrespiratória e óbito. O tratamento primário requer diagnóstico precoce, retirada dos neurolépticos e cuidados médicos de suporte. Na ausência de ensaios clínicos randomizados, benzodiazepínicos, medicamentos dopaminérgicos como bromocriptina ou amantadina, dantroleno e ECT (terapia eletroconvulsiva) têm sido empregados com sucesso variável. Nem os exames laboratoriais nem a apresentação de sintomas permitem o diagnóstico de SNM. O diagnóstico requer histórico e exames médicos completos, juntamente com a eliminação de outras condições orgânicas ou induzidas por drogas.9,10 Se houver suspeita de SNM, o Neuroleptic Malignant Syndrome Information Service (NMSIS), financiado pelo MHAUS, fornece publicações e suporte por telefone e e-mail em seu site (www.NMSIS.org)
Síndrome de parkinsonismo/hipertermia (SPH)
A SPH é causada pela retirada de medicamentos dopaminérgicos de ação central que controlam a rigidez muscular, o retardo motor e outros sintomas da doença de Parkinson. Os sintomas costumam flutuar e a dosagem do medicamento pode variar porque os pacientes podem se tornar relativamente insensíveis aos medicamentos dopaminérgicos. Os medicamentos dopaminérgicos às vezes são interrompidos durante a hospitalização aguda por condições médicas ou cirúrgicas ou no pré-operatório, a fim de minimizar seus efeitos colaterais autonômicos. A SPH, uma condição semiaguda que se assemelha a SNM e HM, pode ocorrer após a retirada súbita da terapia com medicamentos parkinsonianos. É relatada em até 4% dos pacientes nos quais os medicamentos dopaminérgicos são descontinuados agudamente e aproximadamente um terço dos pacientes que desenvolvem a síndrome têm sequelas de longo prazo.11 Febre, atividade muscular anormal e outros sinais de hipermetabolismo juntamente com instabilidade autonômica são observados. A SPH pode ser facilitada por desidratação, infecção e outros estresses do sistema, ou após a administração de drogas bloqueadoras de dopamina central como droperidol ou neurolépticos como haloperidol. Também pode ser induzida em pacientes com Parkinson após a perda súbita de estimulação cerebral profunda (ECP) para a doença de Parkinson ou após o implante de eletrodos para ECP.12,13 Enquanto que a SNM é uma condição com risco de vida causada por medicamentos que bloqueiam a dopamina central, a SPH é causada pela suspensão da terapia dopaminérgica. Por esse motivo, a interrupção completa da terapia dopaminérgica no período perioperatório deve ser evitada, se possível. Além disso, pacientes que tiveram seus medicamentos de Parkinson interrompidos no período perioperatório deverão retomar o tratamento o mais rapidamente possível.14
Síndrome da serotonina (SS)
A SS geralmente é observada quando vários medicamentos que aumentam os níveis centrais de serotonina são administrados concomitantemente, mas também pode ocorrer após uma dose única ou overdose de um ou mais medicamentos serotoninérgicos. A serotonina ou 5-hidroxitriptamina, uma monoamina derivada do triptofano, é um neurotransmissor no cérebro, intestino e plaquetas. A serotonina modula uma ampla gama de ações centrais e periféricas que incluem a regulação do humor, apetite, sono, algumas funções cognitivas, agregação plaquetária e contração da musculatura lisa do útero, brônquios e pequenos vasos sanguíneos.15 Consequentemente, uma série de medicamentos antidepressivos foi projetada para manipular os níveis de serotonina do SNC. Esses incluem os inibidores seletivos da recaptação da serotonina (ISRSs), inibidores seletivos da recaptação da norepinefrina (ISRNs), antidepressivos tricíclicos e inibidores da monoamina oxidase (IMAO). A incidência de SS foi relatada como afetando 0,9-2% dos pacientes em terapia crônica e até 14-16% após overdose.16 ISRSs e ISRNs são mais frequentemente associadas a SS. Os medicamentos adjuvantes anestésicos comumente usados e outras classes importantes de medicamentos – incluindo alguns vendidos sem receita – podem contribuir para a apresentação ou precipitação de SS (ver Tabela 3).17-20
Tabela 3: Alguns medicamentos que causam ou potencializam a síndrome da serotonina.
| Antidepressivos | Triptanos |
| ISRSs Citalopram Fluoxetina Fluvoxamina Paroxetina TrazodonaISRNs Duloxetina Sibutramina Venlafaxina Tricíclicos IMAOs |
Almotriptano Eletriptano Frovatriptano Naratriptano Rizatriptano Sumatriptano Zolmitriptano |
| Adjuvantes de anestesia | Diversos |
| Cocaína Meperidina Metadona Ondansetron Tramadol Fentanil |
Buspirona, ciclobenzaprina Dextrometorfano (“ergot”) 5-hidroxitriptofano linezolida Loperamida Azul de metileno Erva de São João |
A SS pode se apresentar com estado mental alterado, disfunção autonômica, hipotensão, rigidez neuromuscular, agitação, clônus ocular e periférico, diaforese e febre.
O início pode ser abrupto após a administração ou overdose do medicamento. A SS pode se apresentar como uma síndrome hipertérmica e hipermetabólica que é difícil de distinguir de SNM, SPH e HM. Tal como acontece com SNM e SPH, a progressão dos sintomas pode levar a insuficiência cardiorrespiratória, lesão muscular, lesão de múltiplos órgãos e óbito. A incidência de SS pode ser subestimada, possivelmente por causa de casos leves que são negligenciados ou porque apresentações mais graves podem mimetizar outras causas. Portanto, pode ser que a SS seja mais comum no período perioperatório do que sabemos. É importante que os anestesiologistas se lembrem de que vários medicamentos anestésicos adjuvantes que usamos comumente podem precipitar ou aumentar o risco de SS. O tratamento requer a suspensão de todos os medicamentos que contribuem para o excesso de serotonina juntamente com terapia de suporte.15,16 Embora não comprovado, algumas autoridades recomendam o uso do bloqueador central do receptor 5-hidroxitriptamina 2a, ciproeptadina, porque se acredita que o receptor 5-hidroxitriptamina 2a seja um dos ativadores centrais primários da hipertermia na SS.16,21,22
Abstinência de baclofeno
Reações semelhantes a SNM e HM foram relatadas após a retirada do baclofeno. O baclofeno aumenta os efeitos centrais do ácido gama-aminobutírico (GABA), um neurotransmissor inibidor do sistema nervoso central (SNC). O baclofeno é comumente administrado por via oral ou por injeção/infusão direta no líquido cefalorraquidiano por anestesiologistas e outros especialistas em dor para controlar a espasticidade observada após lesão do SNC em condições como paralisia cerebral, lesão da medula espinhal e distonia. Como o bacofleno é usado por especialistas em dor, não é infrequente que outros anestesiologistas se envolvam em recargas de bombas, avaliação de bomba de baclofeno com defeito ou prescrição de baclofeno para um colega. Portanto, é importante para os integrantes da equipe de cuidados anestésicos saber que a síndrome semelhante à HM após a retirada aguda do baclofeno, com deficiência relativa de GABA no SNC, pode ser dramática com febre, estado mental anormal, hiperatividade autonômica, dificuldade respiratória, rabdomiólise e coagulopatia. O tratamento envolve cuidados médicos de suporte e reinstituição da terapia com baclofeno.23
Drogas recreativas
Estimulantes do SNC selecionados usados para “recreação” ou em overdose causam condições hipermetabólicas que podem se assemelhar a crises de HM por meio de efeitos periféricos diretos e no SNC. Esses incluem anfetaminas, dextroanfetamina, metanfetamina, MDMA (metileno-dioxi-metanfetamina), cocaína e drogas psicoativas como PCP e LSD. Embora o histórico de medicamentos e a triagem toxicológica geralmente identifiquem esses problemas antes da cirurgia de emergência para trauma ou outras condições agudas, o uso “recreativo” pode ser encontrado em pacientes agendados para cirurgia eletiva. Assim como alguns pacientes se medicam com álcool ou maconha “medicinal” antes da cirurgia para controlar a ansiedade, os usuários habituais dessas drogas psicoativas podem fazer o mesmo. Embora os sintomas subjetivos iniciais variem à medida que cada um desses medicamentos começa a fazer efeito, todos podem produzir sinais de hiperatividade simpática, atividade motora anormal, febre e hipermetabolismo com cardiorrespiratório e FMOS no período perioperatório. Pacientes que se apresentam para cirurgia com estado mental anormal, sinais de hiperatividade simpática e outros sintomas incomuns que não são causados por seu problema médico primário devem passar por exames toxicológicos, se possível.
Conclusão
Embora os profissionais de anestesia conheçam a HM como uma crise perioperatória, é importante estar ciente de outras síndromes hipermetabólicas induzidas por medicamentos que podem ser observadas no ambiente perioperatório. Na verdade, os medicamentos adjuvantes anestésicos comumente usados podem contribuir para elas ou precipitá-las. O dantroleno sódico é o medicamento crítico para o tratamento da crise de HM, mas não é específico porque pode melhorar alguns dos sinais hipermetabólicos de outras condições. Como elas podem imitar de perto a crise de HM e o dantroleno pode controlar alguns dos sintomas, o diagnóstico incorreto de HM pode atrasar ou impedir outro tratamento eficaz.
Charles Watson, MD, é consultor voluntário da linha direta de MHM para a Malignant Hyperthermia Association of the United States (MHAUS), Sherburne, NY, EUA.
Stanley Caroff, MD, é professor de psiquiatria da Escola de Medicina da University of Pensilvânia e diretor do Neuroleptic Malignant Syndrome Information Service (NMSIS) e representante da MHAUS.
Henry Rosenberg, MD, é o presidente da MHAUS.
Os Drs. Watson e Rosenberg não apresentam conflitos de interesse.
O Dr. Caroff é consultor da Neurocrine Biosciences, Teva Pharmaceuticals. Ele também recebeu bolsas de pesquisa da Neurocrine Biosciences, Osmotica Pharmaceuticals e Eagle Pharmaceuticals.
Referências
- Rosenberg H, Davis M, James D, et al. Malignant hyperthermia. Orphanet Journal of Rare Diseases. 2007:2:21.
- Rosenberg H, Hall D, Rosenbaum H. Malignant hyperthermia. In: Brendt J, ed. Critical Care Toxicology. Elsevier-Mosby; 2005:291–304.
- Parness J, Rosenberg H, Caroff SN. Malignant hyperthermia and related conditions. In: Kellum JA, Fortenberry JD, Fuchs BD & Shaw A, eds. Clinical Decision Support: Critical Care Medicine. Wilmington, Delaware: Decision Support in Medicine, LLC: 1913.
- Mann SC. Thermoregulatory mechanisms and antipsychotic drug-related heatstroke. In: Mann SC, Caroff SN, Keck PE, Lazarus A, eds. Neuroleptic Malignant Syndrome and Related Conditions. 2nd Ed. Washington, DC: American Psychiatric Publishing; 2003:45–74.
- Goulon M, de Rohan-Chabot P, Elkharrat D, et al. Beneficial effects of dantrolene in the treatment of neuroleptic malignant syndrome: a report of two cases. Neurology. 1983;33:516–518.
- Pawat SC, Rosenberg H, Adamson R, et al. Dantrolene in the treatment of refractory hyperthermic conditions in critical care: a multicenter retrospective study. Open Journal of Anesthesiology. 2015;5:63–71.
- Hadad E, Cohen-Sivan Y, Heled Y, et al. Clinical review: treatment of heat stroke: should dantrolene be considered? Crit Care. 2005;9:86–91.
- Shih TH, Chen KH, Pao SC, et al. Low dose dantrolene is effective in treating hyperthermia and hypercapnea, and seems not to affect recovery of the allograft after liver transplantation: case report. Transplantation Proceedings. 2010; 42:858–860.
- Caroff SN, Rosenberg H, Mann SC, et al. Neuroleptic malignant syndrome in the perioperative setting. Am J Anesthesiology. 2001; 28: 387–393.
- Caroff SN. Neuroleptic malignant syndrome. In: Mann SC, Caroff SN, Keck PE, Lazarus A, eds. Neuroleptic Malignant Syndrome and Related Conditions. 2nd Ed. Washington, DC: American Psychiatric Publishing; 2003:1–44.
- Newman EJ, Grosset DG, Kennedy, PGE. The parkinsonism-hyperpyrexia syndrome. Neurocrit Care 2009;10:136–140.
- Artusi CA, Merola A, Espay AJ, et al. Parkinsonism-hyperpyrexia syndrome and deep brain stimulation. J Neurol. 2015; 262:2780–2782.
- Caroff SN. Parkinsonism-hyperthermia syndrome and deep brain stimulation. Can J Anaesth. 2017;64:675–676.
- Newman EJ, Grossett DG, Kennedy PG. The parkinsonism-hyperpyrexia syndrome. Neurocrit Care. 2009;10:136–140.
- Frazer A, Hensler JG. Serotonin involvement in physiological function and behavior. In: Siegel GJ, Agranoff BW, Albers RW, et al., editors. Basic Neurochemistry: Molecular, Cellular and Medical Aspects. 6th edition. Philadelphia: Lippincott-Raven; 1999. Available from: https://www.ncbi.nlm.nih.gov/books/NBK27940/ Accessed December 12, 2020.
- Francescangeli J, Karamchandani K, Powell M, et al. The serotonin syndrome: from molecular mechanisms to clinical practice. Int J Mol Sci. 2019;20:2288.
- Nguyen H, Pan A, Smollin C, et al. An 11-year retrospective review of cyproheptadine. J Clin Pharm Ther. 2019;44:327–334. doi: 10.1111/jcpt.12796
- Basta MN. Postoperative serotonin syndrome following methylene blue administration for vasoplegia after cardiac surgery: a case report and review of the literature. Semin Cardiothoracic Vasc Anes. 2020: 1089253220960255. (pre-pub)
- Orlova Y, Rizzoli P, Loder E. Association of coprescription of triptan antimigraine drugs and selective serotonin reuptake inhibitor or selective norepinephrine reuptake inhibitor antidepressants with serotonin syndrome. JAMA Neurol. 2018;75:566–572.
- Boyer EW, Shannon M. The serotonin syndrome. N Engl J Med. 2005;352:1112–1120.
- Simon L, Kennaghan M. Serotonin syndrome [review]. StatPearls. NCBI Bookshelf. 2020:5. Published Jan 2020, Accessed October 2020.
- Nguyen H, Pan A, Smollin C, et al. An 11-year retrospective review of cyproheptadine use in serotonin syndrome cases reported to the California Poison Control System. J Clin Pharm Ther. 2019:44;327–334.
- Coffey RJ, Edgar TS, Francisco GE, et al. Abrupt withdrawal from intrathecal baclofen: recognition and management of a potentially life-threatening syndrome. Arch Phys Med Rehabil. 2002;83:735–741.


 Issue PDF
Issue PDF