El sevofluorano y el desfluorano se introdujeron en el mercado de los EE. UU. a principios de la década de 1990, con algunas preocupaciones de seguridad sobre ambos. El sevofluorano tuvo una restricción con respecto al flujo de gases debido a preocupaciones por la formación del compuesto A y por una necrosis de las células tubulares renales asociada que se halló en un modelo en ratas.1 En cuanto al desfluorano, se observó que este era irritante de las vías aéreas y se asociaba con laringoespasmo, activación del sistema simpático, taquicardia e hipertensión.2–6 Revisamos el sistema de informes de eventos adversos de la Administración de Alimentos y Medicamentos (Food and Drug Administration, FDA) para determinar si estas preocupaciones iniciales probaron tener validez después de 25 años de uso clínico del sevofluorano y desfluorano.
Introducción
 En este informe, hemos explorado la base de datos del Sistema de Informes de Eventos Adversos de la FDA (FAERS) para determinar qué evidencia existe en cuanto a eventos adversos del sevofluorano y el desfluorano. La seguridad de los anestésicos volátiles está aceptada en general, pero se debatieron preocupaciones sobre su seguridad en el momento de su introducción en el uso clínico y, por lo tanto, esto merece una actualización. La justificación de nuestros esfuerzos para usar la base de datos del FAERS son los eventos adversos históricos del uso de anestésicos volátiles más antiguos y fármacos de bloqueo neuromuscular que fueron revelados después de su introducción en la práctica clínica.7, 8 Cuando se aprueban fármacos nuevos para un uso en entornos clínicos con una población diversa de pacientes y varias condiciones de comorbilidad, el proceso de eficacia comprobada, llamado “farmacovigilancia” puede revelar nuevas preocupaciones de seguridad.9 Como ejemplo, la hepatitis por halotano y los defectos de concentración renal inducidos por enflurano se identificaron por primera vez después de que estos gases anestésicos se introdujeran en el entorno clínico.
En este informe, hemos explorado la base de datos del Sistema de Informes de Eventos Adversos de la FDA (FAERS) para determinar qué evidencia existe en cuanto a eventos adversos del sevofluorano y el desfluorano. La seguridad de los anestésicos volátiles está aceptada en general, pero se debatieron preocupaciones sobre su seguridad en el momento de su introducción en el uso clínico y, por lo tanto, esto merece una actualización. La justificación de nuestros esfuerzos para usar la base de datos del FAERS son los eventos adversos históricos del uso de anestésicos volátiles más antiguos y fármacos de bloqueo neuromuscular que fueron revelados después de su introducción en la práctica clínica.7, 8 Cuando se aprueban fármacos nuevos para un uso en entornos clínicos con una población diversa de pacientes y varias condiciones de comorbilidad, el proceso de eficacia comprobada, llamado “farmacovigilancia” puede revelar nuevas preocupaciones de seguridad.9 Como ejemplo, la hepatitis por halotano y los defectos de concentración renal inducidos por enflurano se identificaron por primera vez después de que estos gases anestésicos se introdujeran en el entorno clínico.
Como antecedente, el sevofluorano se introdujo en la práctica clínica en los EE. UU. en 1995.10 La preocupación de seguridad inicial más importante fue el desarrollo de éter fluorometílico de pentafluoroisopropenil (compuesto A), un producto de degradación formado mediante la interacción del sevofluorano y absorbentes de dióxido de carbono. Los efectos del compuesto A no se habían estudiado exhaustivamente en los pacientes de ensayos en fase 1–3 de la FDA.
Esto condujo a una restricción del flujo de gases (FGF) de 2 litros por minuto (lpm) para reducir la exposición humana al compuesto A. Los estudios en modelos de ratas indicaron que el compuesto A podía provocar lesión renal dependiente de la dosis, caracterizada por necrosis tubular proximal en niveles inspirados tan bajos como 114 partes por millón (ppm).1
Posteriormente, se hicieron ensayos de fase IV en voluntarios y pacientes sometidos a largos períodos de anestesia con sevofluorano para examinar tanto el nivel de exposición al compuesto A, como posibles efectos basados en marcadores clínicos de la función renal. En uno de esos estudios, diseñado especialmente para examinar la exposición prolongada al sevofluorano en FGF de 1 lpm, las concentraciones máximas del compuesto A alcanzaron 34 ± 6 ppm, pero no se hallaron cambios clínicamente significativos en los marcadores bioquímicos de disfunción renal.11 Estudios posteriores revelaron que los humanos carecen casi por completo de una enzima renal, lo que es fundamental para dirigir la biodegradación del compuesto A un tiol renal tóxico en las ratas.12
El desfluorano se introdujo en 1992, y su baja solubilidad en sangre le permitió la ventaja clínica de una inducción y recuperación de la anestesia más rápidas y, posiblemente, un ajuste más rápido de la profundidad anestésica deseada en comparación con otros anestésicos volátiles. Sin embargo, después de su lanzamiento, se descubrió que el desfluorano podía activar respuestas reflejas en las vías aéreas debido a su pungencia extrema.2
En el trabajo preclínico con desfluorano también se había informado hipertensión y taquicardia sin motivo aparente, y, en poblaciones pediátricas, broncoespasmo. La baja potencia del desfluorano requirió que se usaran concentraciones más altas para lograr la eficacia clínica, lo que desenmascaró un efecto adverso en las vías aéreas debido a su pungencia. El efecto adverso en las vías aéreas se asoció con la activación del sistema simpático durante la exposición inicial después de la inducción de la anestesia y durante las transiciones ascendentes en la concentración.2,3 En nuestro laboratorio se había demostrado un aumento de 2,5 veces en la actividad del sistema nervioso simpático, taquicardia en el inicio del desfluorano después de la inducción de la anestesia y una activación neurocirculatoria adicional con la transición de 1,0 a 1,5 MAC.4 El trabajo subsiguiente indicó que la lidocaína nebulizada no disminuyó la respuesta refleja de las vías respiratorias, pero los opioides tuvieron un beneficio dosis-dependiente para atenuar la activación neurocirculatoria.13,14
En este informe, hemos explorado la base de datos del Sistema de Informes de Eventos Adversos de la FDA (FAERS) para eventos adversos del sevofluorano y del desfluorano después de veinticinco años de uso clínico en millones de pacientes.
Procuramos determinar si el autoinforme de eventos adversos a la FDA validó las preocupaciones iniciales relacionadas con la seguridad del sevofluorano y el desfluorano, y si surgieron nuevas preocupaciones de seguridad debido al uso clínico en una amplia población de pacientes.
Métodos
Para monitorear la seguridad de los fármacos en la práctica clínica, la FDA ha desarrollado el Sistema de Informes de Eventos Adversos (FDA Adverse Event Reporting System, FAERS).15 El FAERS es una base de datos para monitorizar todos los fármacos y los productos biológicos terapéuticos aprobados mediante la evaluación de la cantidad, la gravedad y los resultados generales de los medicamentos nuevos, incluyendo los anestésicos volátiles. Se consultó la base de datos del FAERS en busca de los eventos adversos (EA) informados para el sevofluorano y el desfluorano entre 1996 y diciembre de 2019. Mediante filtros demográficos, se analizaron los EA para los dos anestésicos volátiles con cada uno de los siguientes filtros de grupos etarios: de 0 a 1 mes, de 2 meses a 2 años, de 3 a 11 años, de 12 a 17 años, de 18 a 64 años, de 65 a 85 años, mayores de 85 años y edad sin especificar. Los EA se clasificaron por grupo de reacción. Por ejemplo, el grupo de reacción cardiovascular incluyó reacciones específicas como paro cardíaco, actividad eléctrica sin pulso (PEA) y taquicardia ventricular, entre otras. Para este artículo, se informaron reacciones generales en trastornos cardíacos, trastornos renales y urinarios, y trastornos respiratorios, torácicos y del mediastino, además de reacciones específicas, p. ej., taquiarritmias ventriculares (taquicardia ventricular, fibrilación ventricular, torsades de pointes). Los trastornos renales específicos (oliguria, anuria, daño renal agudo, insuficiencia renal, trastorno/disfunción tubular renal y necrosis tubular aguda) fueron agrupados para reducir la incidencia de otras reacciones urinarias menos graves, p. ej., retención urinaria. Todos los EA están informados como porcentaje de la cantidad total del grupo de reacción para ese anestésico en cada grupo etario.
Resultados
El uso de desfluorano arrojó 1140 informes de efectos adversos EA; la categoría más frecuente (grupo de reacción) fue la de lesión, intoxicación y complicaciones del procedimiento (24,9 %). Las cuatro subcategorías principales en este grupo de reacción incluyeron complicaciones posteriores al procedimiento, exposición fetal en el embarazo, complicaciones neurológicas y conciencia. Los EA cardíacos estuvieron en segundo lugar con el 23,9 %; las subcategorías más frecuentes incluyeron bradicardia, paro cardíaco, taquicardia y taquicardia ventricular. Los EA torácicos/respiratorios representaron el 19,4 %; la subcategoría principal fue broncoespasmo, que comprendió el 2,9 % de todos los EA relacionados con desfluorano. Los EA más frecuentes que le siguieron fueron hipoxia, disnea y laringoespasmo.
El sevofluorano tuvo 4977 EA informados; la categoría más frecuente fue la de lesión, intoxicación y complicaciones del procedimiento (30,4 %). Las cuatro subcategorías principales en este grupo de reacción incluyeron complicaciones posteriores al procedimiento, exposición fetal en el embarazo, complicaciones neurológicas de la anestesia y conciencia. Al igual que con el desfluorano, los EA cardíacos fueron la segunda categoría más frecuente del grupo de reacción para el sevofluorano, con 24,4 %. Las subcategorías más frecuentes incluyeron paro cardíaco, bradicardia, taquicardia y fibrilación ventricular. Los eventos respiratorios/torácicos representaron el 18,7 %, en un intervalo similar al del desfluorano. Las cuatro subcategorías incluyeron edema pulmonar, hipoxia, apnea y broncoespasmo (1,6 % de la cantidad total de EA con sevofluorano). El laringoespasmo fue la sexta subcategoría más frecuente en las complicaciones respiratorias/torácicas. Cabe destacar que los trastornos específicos renales comprendieron solamente el 4,4 % de todas las reacciones informadas para el sevofluorano, en comparación con el 5,3 % para el desfluorano.
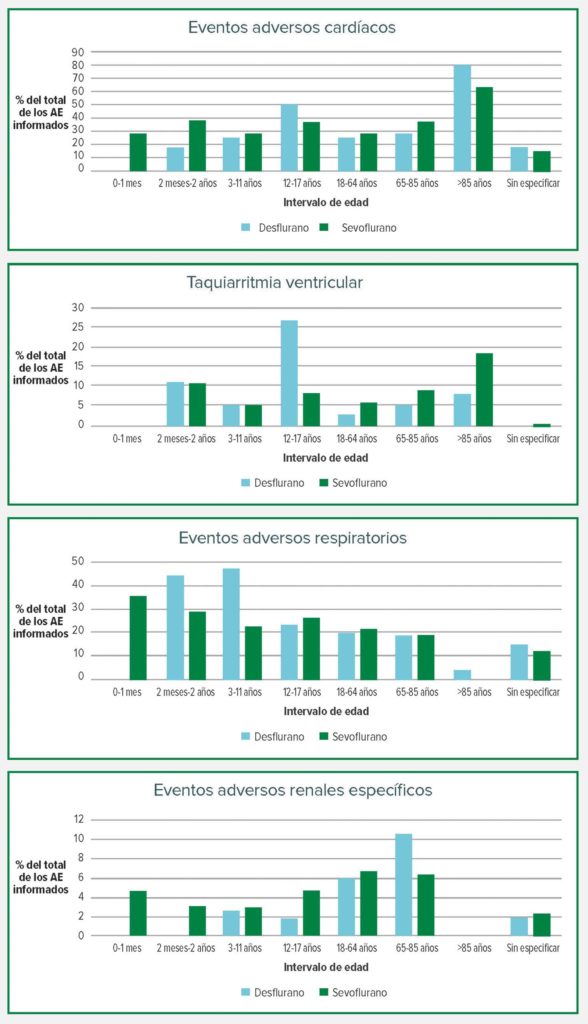
La figura 1 demuestra EA de interés para este informe. Tanto el desfluorano como el sevofluorano tuvieron una alta proporción de informados en el grupo etario de mayores de 85 (80 % y 63,6 %). La taquiarritmia ventricular tuvo una incidencia desproporcionadamente alta con el desfluorano en el rango de edad de 12 a 17 años, del 26,8 %, en comparación con el 8,2 % del sevofluorano. Hubo muy pocos eventos adversos informados en el grupo etario neonatal para el desfluorano, aunque no suele usarse en niños menores de 2 años por las recomendaciones del distribuidor. La proporción de eventos respiratorios en el total de EA para el desfluorano en comparación con el sevofluorano fue notablemente más alta en los grupos etarios de 2 meses a 2 años y de 3 a 11 años.
Debate
La base de datos del FAERS contenía 1140 eventos adversos informados para el desfluorano y 4977 informados para el sevofluorano. La frecuencia de los informes de EA se ve afectada por la cantidad total de cada anestésico administrado en la práctica clínica. Pero el informe de EA confirma, por prevalencia de los EA para cada anestésico, una cantidad de áreas de posible preocupación para estos dos anestésicos volátiles en el uso clínico. Los EA cardíacos fueron el segundo grupo de reacción informado con más frecuencia para ambos anestésicos. La proporción de taquiarritmias ventriculares fue más alta con el desfluorano en la población más joven, pero se observó que era más alta con el sevofluorano en la población de adultos mayores. Los eventos respiratorios fueron más prevalentes que otros eventos adversos en pacientes más jóvenes que recibieron desfluorano. El mayor porcentaje de EA en el grupo de lesión, intoxicación y complicaciones del procedimiento fueron EA de conciencia y neurológicos, que probablemente hayan reflejado la agitación posoperatoria y el deterioro cognitivo.
Hay varios enlaces entre la base de datos del FAERS y la ciencia clínica para cada anestésico.
Arritmias y anestésicos volátiles: Los estudios in vitro han demostrado que el desfluorano puede aumentar la liberación de catecolamina intramiocárdica,16 que puede ocasionar la generación de arritmias. El desfluorano también estuvo asociado con más arritmias que el sevofluorano después del bypass de injerto de arteria coronaria sin bomba,17 y estuvo asociado con tasas más altas de fibrilación auricular posoperatoria después de la cirugía cardíaca con bomba.18 La variabilidad entre las derivaciones del intervalo QT, llamada “dispersión del intervalo QT” (QTd), es un marcador de las diferencias regionales en la repolarización ventricular y se correlaciona mejor con el riesgo de disritmia que el propio intervalo QT.19 En adultos sanos que se someten a una cirugía no cardíaca, la inducción de anestesia solo con desfluorano (sin premedicación) pareció aumentar significativamente la QTd, mientras que la inducción solo con sevofluorano no estuvo asociada con ningún cambio,20 pero cuando se usaron midazolam y vecuronio antes de la intubación, tanto el desfluorano como el sevofluorano prolongaron la QTd sin diferencias significativas entre ambos.21 Aunque una QTd prolongada puede ocasionar varias arritmias, se desconoce su relación con la activación del sistema simpático, más frecuentemente asociada con el desfluorano.
Trastornos respiratorios y anestésicos volátiles: La proporción de EA respiratorios fue alta en el grupo etario más joven. Como se mencionó antes, en los primeros años de disponibilidad clínica del desfluorano hubo preocupaciones sobre la pungencia y la irritación de las vías aéreas. Como se observó en estudios recientes sobre los efectos respiratorios del desfluorano, hay una clara diferencia entre adultos y niños. En un estudio histórico de una gran cohorte de 14 000 niños, los investigadores hallaron que el uso del desfluorano era un factor de riesgo para eventos respiratorios intraoperatorios de todo tipo, así como para el laringoespasmo en particular.5 En un ensayo clínico de 400 niños sanos que recibieron aleatoriamente desfluorano o isoflurano, los niños que recibieron desfluorano tuvieron una frecuencia significativamente más alta de eventos respiratorios de cualquier gravedad, laringoespasmo y tos.6 Sin embargo, los resultados son muy diferentes en adultos. Un metanálisis de 13 ensayos controlados aleatorizados no mostró diferencia entre el sevofluorano y el desfluorano en las tasas de eventos de las vías aéreas superiores, de laringoespasmo o de tos en la aparición.22 Otro metanálisis de siete ensayos controlados aleatorizados no mostró diferencia entre el sevofluorano y el desfluorano en la incidencia de tos o laringoespasmo en adultos en general.23
Limitaciones
El FAERS depende del informe voluntario de eventos adversos por parte de los profesionales de atención médica y de los consumidores en los EE. UU., y, por este motivo, la base de datos tiene limitaciones importantes. Primero, no hay certeza de que la causa del evento adverso informado sea el fármaco en cuestión, ya que la FDA no requiere que se pruebe una relación causal. Segundo, la FDA no recibe información sobre todos los eventos adversos que ocurren por cada fármaco. Hay muchos factores que determinan si se debe presentar un informe, como la gravedad o la difusión del evento. Se espera que se informen efectos secundarios más graves, como las arritmias cardíacas, con más frecuencia que otras reacciones menos graves, como las náuseas posoperatorias. Por este motivo, la base de datos no puede usarse para calcular la incidencia de un evento adverso dado en la población. La frecuencia de uso del sevofluorano es más alta que la del desfluorano en pacientes adultos y pediátricos.24 Por lo tanto, la cantidad de eventos adversos para cualquier anestésico volátil no es relevante a menos que el denominador se conozca con precisión.
Conclusiones: A diferencia de otros anestésicos en los que su uso clínico reveló preocupaciones de seguridad nuevas o imprevistas, como la hepatitis por halotano o anafilaxia por rapacuronio, no parece haber eventos adversos nuevos o imprevistos después de casi 30 años de uso de desfluorano y sevofluorano. Se han realizado investigaciones tempranas que identifican los cambios neurocirculatorios de los efectos irritantes en las vías aéreas del desfluorano, y la ausencia de daño renal del sevofluorano, para explicar los hallazgos en los datos del FAERS. El desfluorano tuvo una alta incidencia de eventos de las vías aéreas en una población más joven, que no persistió en los pacientes de mayor edad. Se observaron arritmias cardíacas con ambos anestésicos, al igual que una prevalencia de taquicardia ventricular con desfluorano en pacientes más jóvenes.
Thomas Ebert, MD, PhD, es profesor de anestesiología en el Medical College of Wisconsin, Milwaukee, WI, y jefe de anestesiología en el Clement J. Zablocki Veterans Affairs Medical Center, Milwaukee, WI.
Alex Ritchay, MD, es anestesiólogo residente en el Departamento de Anestesiología del Medical College of Wisconsin, Milwaukee, WI.
Aaron Sandock, BA, es estudiante de medicina en el Medical College of Wisconsin, Milwaukee, WI.
Shannon Dugan, BS, es asistente de investigación en el Medical College of Wisconsin, Milwaukee, WI.
Los autores no tienen conflictos de intereses.
Referencias
- Gonsowski C, Laster M, Eger E, et al. Toxicity of compound A in rats. Anesthesiology. 1994;80:566–573.
- Muzi M, Lopatka C, Ebert T. Desflurane-mediated neurocirculatory activation in humans: effects of concentration and rate of change on responses. Anesthesiology. 1996;84: 1035–1042.
- Welskopf R, Moore M, Eger E, et al. Rapid increase in desflurane concentration is associated with greater transient cardiovascular stimulation than with rapid increase in isoflurane concentration in humans. Anesthesiology. 1994;80:1035–1045.
- Ebert T, Muzi M. Sympathetic hyperactivity during desflurane anesthesia in healthy volunteers. Anesthesiology. 1993;79:444–453.
- Oofuvong M, Geater A, Chongsuvivatwong V, et al. Risk over time and risk factors of intraoperative respiratory events: a historical cohort study of 14,153 children. BMC Anesthesiology. 2014;14:13.
- Lerman J, Hammer, G. Response to: Airway responses to desflurane during maintenance of anesthesia and recovery in children with laryngeal mask airways. Paediatr Anaesth. 2010;20:962–963.
- Habibollahi P, Mahboobi N, Esmaeili S, et al. Halothane-induced hepatitis: a forgotten issue in developing countries. Hepat Mon. 2011;11:3–6.
- Sosis MB. Further comments on the withdrawal of rapacuronium. Anesthesia & Analgesia. 2002;95:1126–1127.
- Sloane R, Osanlou O, Lewis D, et al. Social media and pharmacovigilance: a review of the opportunities and challenges. Br J Clin Pharmacol. 2015; 80:910–920.
- Smith I, Nathanson M, White P. Sevoflurane-a long-awaited volatile anaesthetic. Br J Anaesth. 1996;76:435–445.
- Ebert T, Frink E, Kharasch E. Absence of biochemical evidence for renal and hepatic dysfunction after 8 hours of 1.25 minimum alveolar concentration sevoflurane anesthesia in volunteers. Anesthesiology. 1998;88:601–610.
- Kharasch E, Jubert C. Compound A uptake and metabolism to mercapturic acids and 3,3,3-trifluoro-2-fluoromethoxypropanoic acid during low-flow sevoflurane anesthesia. Anesthesiology. 1999;91:1267–1278.
- Bunting H, Kelly M, Milligan K. Effect of nebulized lignocaine on airway irritation and haemodynamic changes during induction of anaesthesia with desflurane. Br J Anaesth. 1995;75:631–633.
- Pacentine G, Muzi M, Ebert T. Effects of fentanyl on sympathetic activation associated with the administration of desflurane. Anesthesiology. 1995;82:823–831.
- U.S. Food and Drug Administration. 2020. Potential signals of serious risks by FAERS. [online] Available at: https://www.fda.gov/Drugs/GuidanceComplianceRegulatoryInformation/Surveillance/AdverseDrugEffects/ucm565425.htm Accessed March 9, 2020.
- Park WK, Kim MH, Ahn DS, et al. Myocardial depressant effects of desflurane: mechanical and electrophysiologic actions in vitro. Anesthesiology. 2007;106:956–966.
- Hemmerling T, Minardi C, Zaouter C, et al. Sevoflurane causes less arrhythmias than desflurane after off-pump coronary artery bypass grafting: a pilot study. Ann Card Anaesth. 2010;13:116.
- Cromheecke S, ten Broecke PW, Hendrickx E, et al. Incidence of atrial fibrillation early after cardiac surgery: can choice of the anesthetic regimen influence the incidence? Acta Anaesthesiol Belg. 2005;56:147–54.
- Day C, McComb J, Campbell R. QT dispersion: an indication of arrhythmia risk in patients with long QT intervals. Heart. 1990;63:342–344.
- Yildirim H, Adanir T, Atay A, et al. The effects of sevoflurane, isoflurane and desflurane on QT interval of the ECG. Eur J Anaesthesiol. 2004; 21: 566-570.
- Kazanci D, Unver S, Karadeniz U, et al. A comparison of the effects of desflurane, sevoflurane and propofol on QT, QTc, and P dispersion on ECG. Ann Card Anaesth. 2009;12:107.
- Stevanovic A, Rossaint R, Fritz H, et al. Airway reactions and emergence times in general laryngeal mask airway anaesthesia. Eur J Anaesthesiol. 2015;32:106–116.
- de Oliveira G, Girao W, Fitzgerald P, et al. The effect of sevoflurane versus desflurane on the incidence of upper respiratory morbidity in patients undergoing general anesthesia with a Laryngeal Mask Airway: a meta-analysis of randomized controlled trials. J Clin Anesth. 2013;25:452–458.
- Nasr G, Davis M. Anesthetic use in newborn infants: the urgent need for rigorous evaluation. Pediatr Res. 2015;78: 2–6.