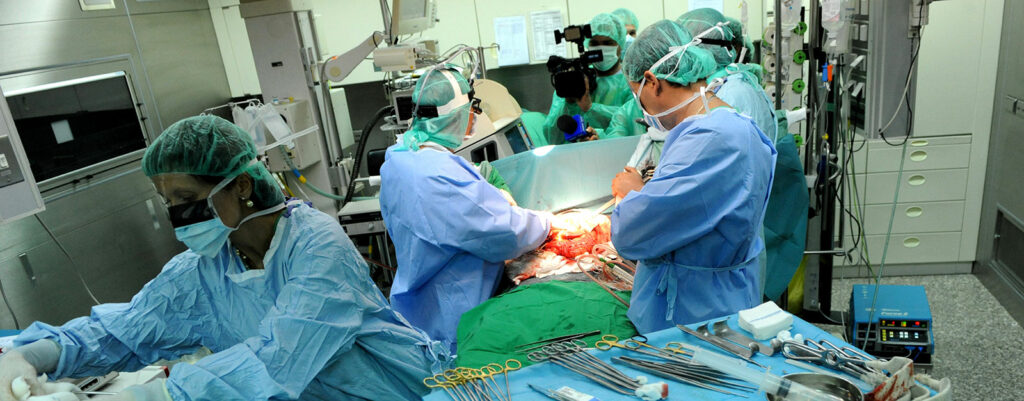
Los pacientes que se presentan para un trasplante de hígado hoy en día han evolucionado debido a la adopción de la asignación de hígado basada en MELD que ha llevado a que se priorice el trasplante para los “más enfermos”. Por lo tanto, la cirugía de trasplante de hígado desafía habitualmente a los sistemas y a los procesos implicados en la seguridad del paciente. Este artículo describe algunos de los procesos desarrollados en la institución que ayudan a contribuir a la seguridad del paciente en un campo que se torna cada vez más desafiante.
INTRODUCCIÓN
Han pasado más de 20 años desde que el Institute of Medicine publicó el informe que cambia el paradigma “To Err is Human” (Errar es humano), que concluyó que cada año ocurrían hasta 98,000 muertes en los hospitales debido a errores en la atención1 . Aunque la cifra exacta de mortalidad relacionada con la anestesia es controvertida, no hay duda de que nuestra especialidad logró avances notables en la mejora de la seguridad del paciente durante las últimas dos décadas gracias a las mejoras en la formación, el equipo y los protocolos estandarizados. Sin embargo, el manejo seguro de los pacientes con trasplante hepático ortotópico (OLT) sigue siendo uno de los casos perioperatorios más desafiantes para los profesionales de anestesia. El OLT implica una colaboración multidisciplinaria, que incluye equipos quirúrgicos, de anestesia y de enfermería, perfusionistas y otros equipos especializados (p. ej., banco de sangre, diálisis e ICU). El procedimiento es técnicamente complejo y el camino intraoperatorio se asocia con inestabilidad hemodinámica, alteraciones metabólicas y acido-básicas, complicaciones de la coagulación, amplios cambios de líquidos y aún se asocia con más muertes intraoperatorias que cualquier otro procedimiento quirúrgico2.
Aunque el éxito en el trasplante de hígado llevó a que se hagan más trasplantes de hígado cada año, la cantidad de órganos donados se estancó. La adopción del sistema basado en el modelo para enfermedad hepática en estadio final (MELD) en 2002 llevó a que el trasplante priorice a los “más enfermos primero” (Tabla 1). Se espera que los pacientes con puntuaciones MELD altas tengan niveles anormales de bilirrubina, creatinina, INR, sodio o una combinación de cada uno (consulte la Tabla 1). Las anomalías en cada uno de estos componentes MELD se asocian con un alto riesgo perioperatorio en estudios previos3 . Esto tiene un profundo efecto en los pacientes que se presentan para un trasplante de hígado, sobre todo, en áreas pobladas donde hay más centros de trasplante. Tal evolución en la elección de pacientes y la creciente gravedad de la enfermedad en pacientes sometidos a trasplante de hígado ha planteado muchos retos perioperatorios para los proveedores que atienden a estos pacientes4 . Los pacientes que se presentan hoy para un trasplante de hígado tienen puntuaciones MELD más altas y una enfermedad hepática más avanzada, una edad más avanzada y comorbilidades preoperatorias, más anomalías renales y electrolíticas, y mayores requerimientos de transfusiones intraoperatorias y de vasopresores que los pacientes que se presentaron para un trasplante de hígado hace veinte años en la era anterior al MELD3.
Tabla 1: Componentes de puntuación MELD y predicción de mortalidad a 3 meses5
Las decisiones sobre qué pacientes se incluyen en las listas de espera de trasplantes en la actualidad también pueden verse distorsionadas aún más por la intensa competencia en áreas pobladas donde hay más centros de trasplante. Nuestra institución, University of Southern California (USC), es un centro de trasplantes de alto volumen en el área metropolitana de Los Ángeles, donde hay tres centros de trasplantes en un radio de 20 millas. El volumen combinado de trasplantes de hígado hechos en el Keck Hospital y en el Children’s Hospital Los Angeles (CHLA) el año pasado se suma al segundo programa de trasplante de hígado más activo del país, según datos de la Red Unida para Compartir Órganos. Con la competencia local y el prestigio en juego, se entiende que los centros pueden estar motivados para hacer más trasplantes, lo que genera más pacientes complejos en la lista de espera. Sin embargo, la cirugía de trasplante hepático hoy desafía todas las capacidades de los sistemas y procesos involucrados en la seguridad del paciente. Este artículo describe algunos de los procesos desarrollados en nuestra institución y cómo contribuyen a la seguridad del paciente en un campo cada vez más desafiante.
DESARROLLO DE EQUIPOS DESIGNADOS DE ANESTESIA PARA TRASPLANTE DE HÍGADO
En 2011, la Red de Obtención y Trasplante de Órganos/Red Unida para Compartir Órganos (OPTN/UNOS) exigió que todos los centros de trasplante nombraran un director de anestesia para trasplante de hígado7 . Esta declaración de un organismo regulador y de gobierno reconocido a nivel nacional fue el primer paso para reconocer la anestesiología de trasplante de hígado como una subespecialidad independiente de la anestesiología. A partir de allí, siguió el desarrollo de equipos de anestesia de trasplante de hígado y becas de anestesia de trasplante. El valor de los equipos de anestesia dedicados se vio respaldado por la evidencia que mostró que estos equipos redujeron la transfusión, el tiempo de ventilación posoperatoria, la duración de la estancia en la unidad de cuidados intensivos y la mortalidad perioperatoria8.
Además de dar atención clínica, los miembros del equipo de anestesia de trasplante de hígado participan en varias funciones perioperatorias de cirugía de trasplante, como los comités de elección de pacientes. El comité multidisciplinario incluye coordinadores de trasplantes, cirujanos, hepatólogos, nefrólogos, especialistas en enfermedades infecciosas, profesionales de anestesia y trabajadores sociales. En estos comités semanales, hablamos del historial hepático del paciente y otros problemas médicos, y después debatimos sobre temas de apoyo social, abuso de sustancias y economía. A partir de allí, el proceso de toma de decisiones implica una revisión ordenada de las posibles causas de exclusión. La participación periódica del equipo de anestesia en el proceso de selección nos permite evaluar formalmente a los pacientes antes de que se presenten para un trasplante de hígado. Si es necesario, se puede remitir a los pacientes a nuestra clínica preoperatoria para permitir que un miembro del equipo de anestesia evalúe más a fondo el estado físico del paciente para el trasplante de hígado.
VERIFICACIÓN PREVIA AL TRASPLANTE Y ABO
Debido a la complejidad de la coordinación en el trasplante, se requieren más procesos de verificación de seguridad involucrados. La verificación del tipo de sangre en puntos múltiples y definidos del proceso de trasplante garantiza la seguridad y la compatibilidad de nuestros donantes y receptores de trasplantes. La información vital, como el tipo de órgano, la identificación del donante y del receptor, el tipo de sangre ABO del donante y del receptor, la fecha de nacimiento del receptor y el número de expediente médico, se verificarán durante el registro de donantes vivos, antes de la recuperación del órgano del donante vivo, antes de la recepción del órgano en el quirófano (si la cirugía del receptor empieza antes de la recepción del órgano en el quirófano) y tras la recepción del órgano en el quirófano. Se requiere que dos profesionales de la atención médica autorizados hagan la verificación. Si el receptor empezará antes de la recepción del órgano en el quirófano, la verificación debe hacerse antes de la inducción de la anestesia o antes de la incisión. Además, los componentes sanguíneos se escanean intraoperatoriamente mediante un sistema de verificación electrónica. El OLT puede requerir hasta 10 veces más unidades de derivados de la sangre que un trasplante de corazón9 . La verificación a través del escaneo de códigos de barras permite la verificación por una sola persona y aumenta la eficiencia del flujo de trabajo mientras que minimiza los errores de transfusión relacionados con la identificación errónea.
EVOLUCIÓN DEL PROGRAMA DE MANEJO DE SANGRE DEL PACIENTE EN KECK USC
Aunque las transfusiones de sangre son una terapia que salva la vida de algunos pacientes, la Joint Comission identificó las transfusiones como uno de los cinco procedimientos más usados en exceso en 201210 . El Programa de Manejo de Sangre de Pacientes y Cirugía Libre de Transfusión en Keck USC se desarrolló inicialmente en 1997 para atender las necesidades específicas de la comunidad de Testigos de Jehová (JW). Nuestro centro obtuvo reconocimiento nacional después de que nuestro equipo de trasplantes hiciera con éxito los primeros trasplantes de hígado de donantes vivos sin transfusiones en 1999 usando técnicas como la dilución normovolémica aguda. Entre 1999 y 2004, se hicieron 27 trasplantes de hígado, de donantes vivos y de donantes fallecidos, en pacientes JW en el USC-University Hospital11 . El éxito relativo del trasplante de hígado en pacientes JW ofreció la oportunidad de evaluar críticamente el uso de derivados de la sangre en la cirugía en general. Lo que comenzó en Keck USC como una iniciativa de enfoque limitado se expandió a un programa general mucho más amplio que atiende a pacientes que no son JW. El concepto de que minimizar la administración de productos sanguíneos mejora la seguridad del paciente y reduce el costo y la duración de la estancia en el hospital impulsó este desarrollo. Las tasas más altas de transfusión se asociaron con una mayor duración de la estancia hospitalaria, tasas más altas de infección, fallas del injerto y mortalidad12.
Dado que la mayor parte de la evidencia que respalda una estrategia de transfusión restrictiva se publicó en la última década, los programas de manejo de sangre del paciente han ganado popularidad recientemente. Los esfuerzos para reducir el uso excesivo de transfusiones a través de programas de manejo de sangre de pacientes en nuestra institución han tenido éxito. En la actualidad, se está haciendo un estudio retrospectivo durante la redacción de este artículo. La recopilación de datos preliminares informa de una disminución del ~20% en el uso de glóbulos rojos, plaquetas y plasma para casos de trasplante de hígado en 2021 en comparación con 2020, a pesar de un aumento en los casos. Nuestra reducción de transfusiones en LT fue el resultado de varias intervenciones clave implementadas que se analizarán. Primero, se implementó una campaña en todo el hospital para educar y promover el cambio a la cultura de la práctica liberal de uso de sangre. Una estrategia exitosa fue la adopción de la campaña “¿Por qué dar 2 cuando 1 es suficiente?” La Iniciativa “Choosing Wisely” para reducir los pedidos de transfusiones de glóbulos rojos de unidades múltiples13 . Siguió un amplio esfuerzo de comunicación en los boletines de nuestro hospital y en los protectores de pantalla de las computadoras para animar las transfusiones de una sola unidad.
Otra intervención que cambió nuestra práctica de transfusión en nuestra institución fue la implementación de la tromboelastografía (TEG) intraoperatoria. A pesar de la falta de grandes estudios clínicos aleatorizados, las pruebas viscoelásticas han sido un armamento crítico para el control hemostático en el trasplante de hígado desde que Thomas Starzl, MD, hizo el primer LT en la década de 196014 . Muchas instituciones de trasplante adoptaron pruebas viscoelásticas como TEG en su práctica clínica. Sin embargo, fue solo recientemente que la TEG en nuestro centro se hizo conveniente y eficiente, intraoperatoria y posoperatoriamente en la ICU, para permitir una evaluación cualitativa rápida y en tiempo real de los diferentes componentes de la hemostasia. Por último, y quizás lo más importante, creemos que nuestro éxito en el manejo de la sangre es el resultado de una mejor comunicación entre los equipos quirúrgicos y de anestesia hepática sobre el progreso del caso. Por ejemplo, la mejora en la comunicación y el uso de TEG nos permitió distinguir mejor el sangrado quirúrgico del sangrado por coagulopatía, lo que ayudó a reducir las transfusiones intraoperatorias. En general, esperamos demostrar cómo los equipos multidisciplinarios pueden reducir significativamente la utilización total de derivados de la sangre en el OLT.
EL PAPEL DE LA HEMODIÁLISIS (HD) INTRAOPERATORIA EN EL TRASPLANTE DE HÍGADO
El trasplante de hígado para pacientes con disfunción renal a menudo se complica por cambios importantes de líquidos, acidosis y anormalidades electrolíticas y de la coagulación que requieren grandes volúmenes de derivados de la sangre y soluciones cristaloides. En los primeros años de la OLT, los profesionales de anestesia en trasplante de hígado solían manejar los casos de falla renal con un manejo estricto de líquidos y ajustes metabólicos continuos sin la ayuda de la hemodiálisis (HD) intraoperatoria. Sin embargo, a pesar de la vigilancia atenta de la hemodinámica y los trastornos metabólicos del paciente, el trayecto intraoperatorio en muchos casos se complicó por los abrumadores cambios metabólicos y de líquidos que ocurren en pacientes con insuficiencia o falla renal. La justificación detrás del uso de la terapia de reemplazo renal intraoperatoria durante el trasplante de hígado para pacientes con falla renal es que la cirugía generalmente se complica por inestabilidad hemodinámica importante, anomalías de la coagulación y trastornos metabólicos. En nuestro centro, el trasplante de hígado sigue siendo el único caso que usa de forma rutinaria HD intraoperatoria en el manejo de la anestesia15. Nuestra institución fue una de las primeras en demostrar la seguridad y viabilidad de la HD intraoperatoria y adoptar su uso en pacientes en estado crítico con puntuaciones altas del MELD (media ~37) sometidos a LT16.
La decisión de usar HD intraoperatoria durante el OLT es una decisión colaborativa entre el cirujano, el equipo de anestesia y el nefrólogo, según el grado de disfunción renal y el cuadro clínico general, incluyendo la necesidad de terapia de reemplazo renal posoperatoria. Generalmente, la HD intraoperatoria se usará en pacientes con Tasa de Filtrado Glomerular <60 ml/min o creatinina sérica >1.4 mg/dl. Para aquellos sin acceso de diálisis permanente, se introduce un catéter HD de doble lumen en la vena yugular interna, subclavia o femoral. Previo a la cirugía, el nefrólogo decide la concentración de sodio, calcio, potasio y bicarbonato en la solución de diálisis de cada paciente en base a sus valores de laboratorio. Durante la operación, el enfermero de HD trabaja en estrecha colaboración con el equipo de anestesia. Se extraen gases sanguíneos cada media hora a cada hora para ayudar a guiar los cambios en el dializado según sea necesario (principalmente ajustes en los niveles de bicarbonato y potasio)17 . El uso de HD intraoperatoria ayuda en el manejo de la temperatura, la acidosis, la hiperpotasemia y la sobrecarga de volumen, todos los que se asocian con morbilidad y mortalidad intraoperatoria en pacientes sometidos a trasplante de hígado15 . El profesional de la anestesia está familiarizado con las diversas opciones de tratamiento disponibles (Tabla 2). Con una evaluación minuciosa, monitorización e intervenciones apropiadas continuas, la HD intraoperatoria se puede usar de forma segura y eficaz en pacientes en estado crítico sometidos a LT con puntuaciones MELD elevadas y disfunción renal.
Tabla 2: Resumen de las variaciones del tratamiento durante la HD intraoperatoria
CONCLUSIÓN
Las diferentes variantes de los pacientes que se presentan para un trasplante de hígado en la actualidad plantearon muchos retos a los sistemas y procesos involucrados en la seguridad del paciente. En este artículo, revisamos algunos de los procesos implementados en nuestro centro que nos permitieron mejorar las medidas de seguridad y los resultados en pacientes gravemente enfermos con MELD alto que se someten a un trasplante de hígado. Para continuar mejorando la seguridad del paciente en el trasplante de hígado, se requieren datos y estudios más completos para caracterizar aún más la evolución de los retos en la seguridad en el trasplante de hígado en la actualidad.
Khoa Tran, MD, es becaria de Anestesiología de trasplante de hígado en la USC Keck School of Medicine en Los Ángeles, CA.
Ashraf Sedra, MD, es el jefe de Anestesiología para trasplantes y profesor asociado de Anestesiología en USC Keck School of Medicine en Los Ángeles, CA.
Joseph W. Szokol, MD, JD, MBA, es profesor en el Departamento de Anestesiología, University of Southern California Keck School of Medicine, Los Ángeles, CA.
Los autores no tienen ningún conflicto de interés.
Referencias
- Kohn LT, Corrigan J, Donaldson MS. To err is human : building a safer health system. National Academy Press; 2000, p. 87. PMID: 25077248.
- Butt Z, Parikh ND, Skaro AI, et al. Quality of life, risk assessment, and safety research in liver transplantation: new frontiers in health services and outcomes research. Curr Opin Organ Transplant. Jun 2012;17:241–247. PMID: 22476225.
- Xia VW, Taniguchi M, Steadman RH. The changing face of patients presenting for liver transplantation. Curr Opin Organ Transplant. Jun 2008;13:280–284. PMID: 18685318.
- Zarrinpar A, Busuttil RW. Liver transplantation: past, present and future. Nat Rev Gastroenterol Hepatol. July 2013;10:434–440. PMID: 23752825.
- Kremers WK, van IJperen M, Kim WR, et al. MELD score as a predictor of pretransplant and posttransplant survival in OPTN/UNOS status 1 patients. Hepatology. 2004;39:764–769. PMID: 14999695.
- OPTN 2016 MELD Policy Changes 2016. https://optn.transplant.hrsa.gov/news/meld-serum-sodium-policy-changes/. https://optn.transplant.hrsa.gov/media/eavh5bf3/optn_policies.pdf. Both accessed December 14, 2022.
- Nguyen-Buckley C, Wray CL, Zerillo J, et al. Recommendations from the Society for the Advancement of Transplant Anesthesiology: liver transplant anesthesiology fellowship core competencies and milestones. Semin Cardiothorac Vasc Anesth. 2019;23:399–408. PMID: 31402752.
- Hevesi ZG, Lopukhin SY, Mezrich JD, et al. Designated liver transplant anesthesia team reduces blood transfusion, need for mechanical ventilation, and duration of intensive care. Liver Transpl. 2009;15:460–465. PMID: 19399745.
- Nedelcu E, Wright MF, Karp S, Cook M, et al. Quality improvement in transfusion practice of orthotopic liver transplantation reduces blood utilization, length of hospital stay, and cost. Am J Clin Pathol. 2019;151:395–402. PMID: 30535323.
- Sadana D, Pratzer A, Scher LJ, et al. Promoting high-value practice by reducing unnecessary transfusions with a patient blood management program. JAMA Intern Med. 2018;178:116–122. PMID: 29159367.
- Jabbour N, Gagandeep S, Mateo R, et al. Transfusion free surgery: single institution experience of 27 consecutive liver transplants in Jehovah’s Witnesses. J Am Coll Surg. 2005;201:412–417. PMID: 16125075.
- Tokin C, Almeda J, Jain S, et al. Blood-management programs: a clinical and administrative model with program implementation strategies. Perm J. Winter 2009;13:18–28. PMID: 21373242.
- Podlasek SJ, Thakkar RN, Rotello LC, et al. Implementing a «Why give 2 when 1 will do?» Choosing Wisely campaign. Transfusion. 2016;56:2164. PMID: 27624209.
- Sakai T. Viscoelastic testing in liver transplantation. Transfusion. 2020;60 Suppl 6:S61–S69. PMID: 33089935.
- Sedra AH, Strum E. The role of intraoperative hemodialysis in liver transplant patients. Curr Opin Organ Transplant. 2011;16:323–325. PMID: 21543980.
- Nadim MK, Annanthapanyasut W, Matsuoka L, et al. Intraoperative hemodialysis during liver transplantation: a decade of experience. Liver Transpl. 2014;20:756–764. PMID: 24634344.
- Henson A, Carpenter S. Intra-operative hemodialysis during liver transplantation: an expanded role of the nephrology nurse. Nephrol Nurs J. 2010;37:351–353, 356; quiz 354. PMID: 20830942.
- Vitin A, Muczynski K, Bakthavatsalam R, et al. Treatment of severe lactic acidosis during the pre-anhepatic stage of liver transplant surgery with intraoperative hemodialysis. J Clin Anesth. 2010;22:466–472. PMID: 20868970.


 Issue PDF
Issue PDF