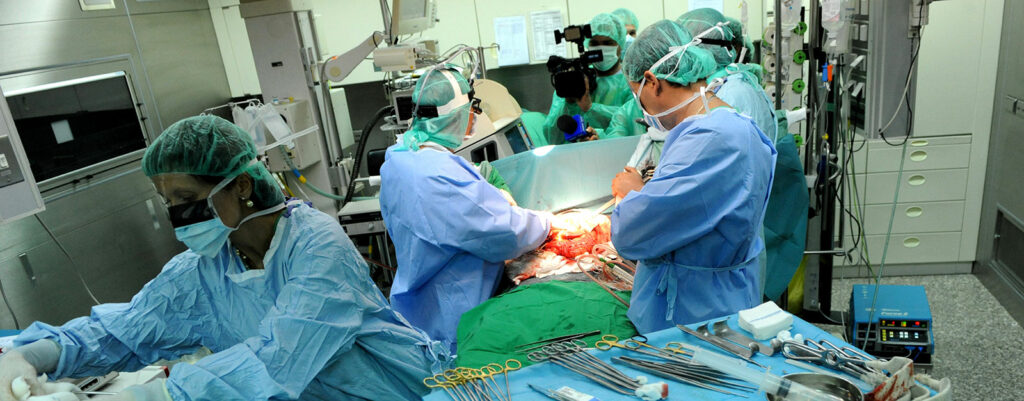
由于采用基于 MELD 的肝脏分配方法,导致优先给“最严重患者”进行移植,当今接受肝移植的患者已经发生了变化。因此,肝移植手术经常给涉及到患者安全的系统和程序带来挑战。本文描述了本机构制定的几项流程,这些流程可以在更具挑战性的领域内促进患者安全。
引言
20 多年前,美国医学研究所(Institute of Medicine)发表了《人非圣贤孰能无过》(To Err is Human),从该报告可知每年有多达 98,000 例患者死于医疗差错。1尽管麻醉相关死亡的确切数字尚有争议,但毫无疑问,在过去的二十年里,由于改进了培训、设备,并对方案进行了标准化,麻醉专业在改善患者安全方面取得了显著进展。但是,对于麻醉专业人士来说,原位肝移植 (OLT) 患者的安全管理仍然是最具挑战性的围手术期情况之一。OLT 涉及多学科协作,包括外科、麻醉、护理团队,以及灌注专家和其他专业团队(例如,血库、透析和 ICU)。该手术在技术上很复杂,术中可能出现血流动力学不稳定性、酸碱和代谢失衡、凝血并发症、大范围体液转移等相关问题,术中死亡率也超过其他手术。2
尽管肝移植方面的成功使每年开展的肝移植手术增加,但捐献的器官数量已达到平台期。2002 年开始采用基于终末期肝病模型 (MELD) 的系统,这样一来移植会优先考虑“病情最严重的患者”(表 1)。MELD 高评分患者可能会出现胆红素、肌酐、INR 和钠水平异常,或多项数值同时异常(见表 1)。既往研究发现,MELD 中每一项指标异常均与高围手术期风险有关。3这对接受肝移植的患者有极大影响,特别是在人口稠密、移植中心较多的地区。患者选择的演变以及肝移植患者的疾病严重程度增加给照护这些患者的医生带来了许多围手术期挑战。4与二十年前在前 MELD 时代接受肝移植的患者相比,现在接受肝移植的患者 MELD 评分更高、处于肝脏疾病晚期、年龄更大、术前合并症更多、更严重的肾脏和电解质异常情况以及术中输血和血管加压类药物需求更高。3
表 1:MELD 评分系统和 3 月期死亡率预测5
如今,在人口稠密、有更多移植中心的地区,关于哪些患者被列入移植等待名单也可能会因为激烈竞争而受到影响。本机构——南加州大学 (USC) 是洛杉矶市区的一个体量较大的移植中心,方圆 20 英里范围内有三个移植中心。根据器官共享联合网络(United Network for Organ Sharing )的数据,去年在凯克医院和洛杉矶儿童医院 (CHLA) 实施的肝移植手术加起来在全美排名第二。为应对当地竞争和维护声誉,这些医疗中心可能会实施更多的移植手术,这样一来越来越多更具挑战性的患者会被列入等候名单。不过,当今的肝移植手术对医疗系统的整体能力和涉及到患者安全的流程提出了挑战。本文描述了本机构制定的几项流程,以及这些流程如何在一个越来越具有挑战性的领域内促进患者安全。
指定肝脏移植麻醉团队的发展
2011 年,器官获取和移植网络/器官共享联合网络 (OPTN/UNOS) 要求所有移植中心指定一名肝移植麻醉负责人。7国家公认的监督管理机构作出这项声明,等同于率先承认了肝移植麻醉学是麻醉学中的一个独立的麻醉亚专业。以此为起点,肝移植麻醉团队和移植麻醉研究基金也逐渐发展起来。有证据表明,专门的移植团队减少了输血、术后通气时间、重症监护室住院时间以及围手术期死亡率,这进一步证实了专门的麻醉团队的价值所在。8
除提供临床照护外,肝移植麻醉团队成员还参与到肝移植围手术期的多个环节,如患者选择委员会等。该多学科委员会的成员包括移植协调员、手术医生、肝病医师、肾病医师、传染病专科医师、麻醉专业人员和社会工作者。在每周一次的委员会会议上,我们讨论患者的肝病史和其他医学问题,然后再讨论社会支持、药物滥用和财务等方面的问题。从这里开始,决策过程包括对可能的排除理由进行审查。麻醉团队例参与这一环节,使我们能够在患者进行肝移植之前对其进行正式评估。如需要,患者可以转诊至我们的术前诊所,以便麻醉团队成员进一步评估患者的生理状态是否适合肝移植。
移植前和 ABO 血型核验
由于移植协调工作的复杂性,还会涉及到额外的安全程序。在移植过程中的多个规定时点鉴定血型核验可确保移植供体和受体的安全和兼容性。在活体捐赠者登记期间、活供体器官摘取之前、在手术室接收器官之前(如果受体手术在手术室接收器官之前开始)以及在手术室接收器官时核验重要信息,如器官类型、捐赠者和接受者 ID、捐赠者和受体的 ABO 血型,以及受体的出生日期和病例号等。核验需要由两名具备相应执照的医疗照护人员进行。如果受体手术将在手术室接收器官之前开始,则核验必须在麻醉诱导之前或切口之前进行。此外,还要在术中使用电子核验系统扫描血液成分。OLT 需要的血液制品单位可能是心脏移植手术的十倍。9通过条形码扫描来进行核验允许执行单人核验,可提高工作流程效率,并最大限度减少与误识别相关的输血差错。
Keck USC 患者血液管理项目的发展
尽管输血对于某些患者来说是一种挽救生命的治疗方法,但在 2012 年的联合委员会的过度使用峰会上认定输血为五大过度使用的治疗之一。10Keck USC 的无输血手术和患者血液管理项目于 1997 年制定,最初是为服务于耶和华见证人 (JW) 社区的特殊需求。1999 年,我们的移植团队于使用急性等容稀释等技术首次成功施行了无输血活体肝移植,使本中心在美国得到了广泛认可。在 1999–2004 年之间,USC 大学医院对 JW 患者实施了27 例肝移植,包括活供体和死亡供体肝移植。11JW 患者中相对成功的肝移植使我们有机会对术中血液制品的使用进行关键性评估。这最初只是 Keck USC 的一项应用范围有限的举措,现在已扩展成为范围更广的主流项目,将非 JW 患者也纳入了服务范围。这一进展由以下理念推动,即最大限度减少血液制品的使用可提高患者安全,并减少住院成本和天数。较高的输血率已被发现与住院时间延长、较高的感染率、移植失败率和死亡率有关12。
由于多数支持限制性输血策略的证据是在过去十年中发表的,患者血液管理项目近年才流行起来。本机构通过患者血液管理计划减少过度使用输血的努力已经取得了成功。在撰写本文期间,本机构正在开展一项回顾性研究。初步收集的数据表明,较之于 2020 年,尽管病例有增加,但 2021 年用于肝移植病例的 RBC、血小板和血浆大约减少了 20%。肝移植的输血量减少得益于几项关键性干预措施的实施,我们将对这些措施加以讨论。首先,开展了全院性的活动来教育和促进自由用血实践文化的变革。一个成功的策略是采用“既然 1 单位血制品就可以,为什么要输注 2 单位?”通过相应倡议活动来减少多单位 RBC 输血申请。13随后,在我们医院的新闻通讯和电脑屏保上进行了广泛宣传,以鼓励单一单位输血。
改变本机构输血实践的另一项干预措施是执行术中血栓弹力图 (TEG) 分析。尽管缺乏大规模随机临床研究,但自上世纪六十年代Thomas Starzl 博士首次实施肝移植以来,粘弹性试验已成为肝移植中止血控制的重要手段。14许多移植机构已在其临床实践中采用了粘弹性试验,如 TEG 等。但是,直到最近,我们中心的 TEG 才在术中和术后的 ICU 中变得方便且高效,以便对不同的止血成分进行快速、实时的定性评估。最后,可能也是最重要的一点,我们相信,我们在血液管理方面取得的成功得益于肝脏麻醉团队和手术团队之间的有效沟通。例如,沟通的改善和 TEG 的使用使我们能够更好地区分手术出血和凝血病所致的出血,这有助于减少术中输血。综上,我们希望说明多学科团队如何才能显著减少 OLT 中血液制品总体输注量。
术中血液透析 (HD) 在肝脏移植中的作用
肾功不全患者的肝移植常会因为大量体液转移、酸中毒、电解质和凝血异常,需要输注大量血液制品和晶体溶液。早年开展的 OLT 中,在没有术中血液透析 (HD) 帮助的情况下,肝移植麻醉专业人士是通过严格的液体管理和持续的代谢调整来管理肾衰病例。但是,尽管对患者的血流动力学和代谢紊乱进行了严密监控,但在许多病例中,术中因肾功能受损或肾衰竭患者出现大量体液和代谢变化而变得复杂。肾衰患者在肝移植过程中使用术中肾脏替代疗法的根本原因是,手术通常会因为严重血流动力学不稳定性、凝血异常和代谢紊乱而变得复杂。在我们中心,肝移植仍然是唯一常规使用术中 HD 进行麻醉管理的病例。15本机构是首批证实术中 HD 的安全性和可行性的机构之一,并将其用于接受肝移植、高 MELD 评分(平均大约 37)重症病例。16
OL T术中是否使用术中 HD 是由手术医生、麻醉团队和肾病专家共同决定,这取决于肾功能不全的程度和整体临床状况,包括术后肾脏替代疗法的需求等。通常,术中 HD 将被用于肾小球滤过率 < 60 ml/min 或血清肌酐水平 >1.4 mg/dL 的患者。对于没有永久性透析通路的患者,将双腔 HD 导管插入颈内静脉、锁骨下静脉或股静脉。对于每名患者,在手术之前,肾病专家将根据实验室检查值,确定透析液中的钠离子、钙离子、钾离子和碳酸氢盐浓度。在手术过程中,HD 护士在麻醉团队的密切指导下工作。每半小时或一小时进行一次血气分析,以帮助指导在必要时改变透析液(主要是调整碳酸氢盐和钾离子浓度)。17使用术中 HD 可帮助管理温度、酸中毒、高血钾症以及血容量超负荷,所有这些均与肝移植患者的术中发病率和死亡率有关。15麻醉专业人士应熟悉各种可用的治疗选项(表 2)。通过全面评价、监测和持续的适当干预,术中 HD 可安全而有效地用于MELD 评分高且肾功能不全的肝移植危重症患者。
表 2:术中 HD 期间的治疗方案调整要点
结论
如今,接受肝移植的患者情况复杂,这给患者安全系统和程序带来了许多挑战。在本文中,我们回顾了本中心实施的几项措施,这些措施使我们能够改善接受肝移植的 MELD 高评分重症患者的安全性和患者归转。为了继续提高肝移植的患者的安全性,需要全面的数据和研究来进一步揭示当今肝移植中不断变化的安全性挑战。
Khoa Tran (MD) 是南加州大学凯克医学院(加州洛杉矶)的肝移植麻醉学研究员。
Ashraf Sedra (MD) 是南加州大学凯克医学院的移植麻醉学主任和麻醉学副教授。
Joseph W. Szoko (MD、JD、MBA) 是南加州大学凯克医学院(加州洛杉矶)麻醉学系的教授。
作者没有利益冲突。
参考文献
- Kohn LT, Corrigan J, Donaldson MS.To err is human : building a safer health system.National Academy Press; 2000, p. 87.PMID:25077248.
- Butt Z, Parikh ND, Skaro AI, et al. Quality of life, risk assessment, and safety research in liver transplantation: new frontiers in health services and outcomes research.Curr Opin Organ Transplant.Jun 2012;17:241–247.PMID:22476225.
- Xia VW, Taniguchi M, Steadman RH.The changing face of patients presenting for liver transplantation.Curr Opin Organ Transplant.Jun 2008;13:280–284.PMID: 18685318.
- Zarrinpar A, Busuttil RW.Liver transplantation: past, present and future.Nat Rev Gastroenterol Hepatol.July 2013;10:434–440.PMID:23752825.
- Kremers WK, van IJperen M, Kim WR, et al. MELD score as a predictor of pretransplant and posttransplant survival in OPTN/UNOS status 1 patients.Hepatology.2004;39:764–769.PMID:14999695.
- OPTN 2016 MELD Policy Changes 2016. https://optn.transplant.hrsa.gov/news/meld-serum-sodium-policy-changes/. https://optn.transplant.hrsa.gov/media/eavh5bf3/optn_policies.pdf.Both accessed December 14, 2022.
- Nguyen-Buckley C, Wray CL, Zerillo J, et al. Recommendations from the Society for the Advancement of Transplant Anesthesiology: liver transplant anesthesiology fellowship core competencies and milestones.Semin Cardiothorac Vasc Anesth.2019;23:399–408.PMID:31402752.
- Hevesi ZG, Lopukhin SY, Mezrich JD, et al. Designated liver transplant anesthesia team reduces blood transfusion, need for mechanical ventilation, and duration of intensive care.Liver Transpl.2009;15:460–465.PMID:19399745.
- Nedelcu E, Wright MF, Karp S, Cook M, et al. Quality improvement in transfusion practice of orthotopic liver transplantation reduces blood utilization, length of hospital stay, and cost.Am J Clin Pathol.2019;151:395–402.PMID:30535323.
- Sadana D, Pratzer A, Scher LJ, et al. Promoting high-value practice by reducing unnecessary transfusions with a patient blood management program.JAMA Intern Med.2018;178:116–122.PMID:29159367.
- Jabbour N, Gagandeep S, Mateo R, et al. Transfusion free surgery: single institution experience of 27 consecutive liver transplants in Jehovah’s Witnesses.J Am Coll Surg.2005;201:412–417.PMID:16125075.
- Tokin C, Almeda J, Jain S, et al. Blood-management programs: a clinical and administrative model with program implementation strategies. Perm J. Winter 2009;13:18–28.PMID:21373242.
- Podlasek SJ, Thakkar RN, Rotello LC, et al. Implementing a “Why give 2 when 1 will do?”Choosing Wisely campaign.Transfusion.2016;56:2164.PMID:27624209.
- Sakai T. Viscoelastic testing in liver transplantation.Transfusion.2020;60 Suppl 6:S61–S69.PMID:33089935.
- Sedra AH, Strum E. The role of intraoperative hemodialysis in liver transplant patients.Curr Opin Organ Transplant.2011;16:323–325.PMID:21543980.
- Nadim MK, Annanthapanyasut W, Matsuoka L, et al. Intraoperative hemodialysis during liver transplantation: a decade of experience.Liver Transpl.2014;20:756–764.PMID:24634344.
- Henson A, Carpenter S. Intra-operative hemodialysis during liver transplantation: an expanded role of the nephrology nurse.Nephrol Nurs J. 2010;37:351–353, 356; quiz 354.PMID:20830942.
- Vitin A, Muczynski K, Bakthavatsalam R, et al. Treatment of severe lactic acidosis during the pre-anhepatic stage of liver transplant surgery with intraoperative hemodialysis.J Clin Anesth.2010;22:466–472.PMID:20868970.


 Issue PDF
Issue PDF