Le sévoflurane et le desflurane ont été introduits sur le marché américain au début des années 90, source de préoccupations en matière de sécurité. Le sévoflurane s’accompagnait d’une réduction de débit de gaz frais, en raison d’inquiétudes quant à la formation de composé A, associée à une nécrose tubulaire rénale constatée dans un modèle réalisé sur des rats.1 Il a été noté que le desflurane irritait les voies aériennes, favorisait les laryngospasmes, et entraînait une activation du système sympathique, une tachycardie et une hypertension.2–6 Nous avons étudié le système de signalement d’évènements indésirables de la Food and Drug Administration (FDA) afin de déterminer si ces préoccupations initiales s’étaient avérées légitimes après 25 ans d’utilisation clinique du sévoflurane et du desflurane.
Introduction
 Nous avons exploré la base de données du Système de signalement des évènements indésirables de la FDA (FAERS) à la recherche de preuves (ou d’absence de preuves) d’un lien entre le sévoflurane ou le desflurane et l’apparition d’évènements indésirables pendant l’utilisation clinique de ces deux anesthésiques volatils. La sécurité des anesthésiques volatiles modernes est généralement acceptée, mais les préoccupations liées à leur sécurité ont fait débat à l’époque de leur introduction pour une utilisation clinique et par conséquent, ils méritent une évaluation plus approfondie. Nous justifions notre décision d’utiliser la base de données FAERS par les évènements indésirables historiques, liés à l’utilisation des anciens anesthésiques volatils et des drogues qui induisent un bloc neuromusculaire, qui ont été révélés après leur introduction dans la pratique clinique.7, 8 Lorsque de nouveaux médicaments sont approuvés pour une utilisation courante dans un cadre clinique, avec une population de patients divers et des comorbidités multiples, le processus éprouvé de pharmacovigilance peut permettre de constater de nouvelles inquiétudes en matière de sécurité.9 Par exemple, la toxicité hépatique de l’halothane et les défauts de concentration des urines induits par l’enflurane ont été identifiés après l’introduction de ces gaz anesthésiques dans le cadre clinique.
Nous avons exploré la base de données du Système de signalement des évènements indésirables de la FDA (FAERS) à la recherche de preuves (ou d’absence de preuves) d’un lien entre le sévoflurane ou le desflurane et l’apparition d’évènements indésirables pendant l’utilisation clinique de ces deux anesthésiques volatils. La sécurité des anesthésiques volatiles modernes est généralement acceptée, mais les préoccupations liées à leur sécurité ont fait débat à l’époque de leur introduction pour une utilisation clinique et par conséquent, ils méritent une évaluation plus approfondie. Nous justifions notre décision d’utiliser la base de données FAERS par les évènements indésirables historiques, liés à l’utilisation des anciens anesthésiques volatils et des drogues qui induisent un bloc neuromusculaire, qui ont été révélés après leur introduction dans la pratique clinique.7, 8 Lorsque de nouveaux médicaments sont approuvés pour une utilisation courante dans un cadre clinique, avec une population de patients divers et des comorbidités multiples, le processus éprouvé de pharmacovigilance peut permettre de constater de nouvelles inquiétudes en matière de sécurité.9 Par exemple, la toxicité hépatique de l’halothane et les défauts de concentration des urines induits par l’enflurane ont été identifiés après l’introduction de ces gaz anesthésiques dans le cadre clinique.
Pour resituer le contexte, le sévoflurane a été introduit en pratique clinique aux États-Unis en 1995.10 La préoccupation initiale la plus importante en matière de sécurité du sévoflurane était la formation de pentafluoro-isopropanyl-fluorométhyl éther (composé A), un produit de dégradation formé par l’interaction entre le sévoflurane et les absorbants de dioxyde de carbone. Les effets du composé A n’avaient pas fait l’objet de recherches approfondies chez les patients dans les essais de phases 1 à 3 de la FDA.
Cela a donné lieu à la recommandation de réduire le débit de gaz frais (DGF) à 2 litres par minute (lpm), afin de réduire l’exposition des patients au composé A. Les études menées sur des modèles réalisés sur des rats ont indiqué que le composé A pouvait produire des lésions rénales dépendantes des doses, caractérisées par une nécrose tubulaire proximale à des concentrations de gaz inspirés aussi faibles que 114 ppm.1
Des essais de phase IV ont ensuite été réalisés sur des volontaires et des patients soumis à une anesthésie longue au sévoflurane, afin d’examiner le degré d’exposition au composé A et de rechercher les effets nocifs basés sur les marqueurs cliniques de la fonction rénale. Dans l’une de ces études, conçue spécifiquement pour examiner l’exposition prolongée au sévoflurane à un débit de gaz frais de 1 lpm, les concentrations maximales de composé A ont atteint 34 ± 6 ppm, mais aucun changement significatif clinique des marqueurs biochimiques de dysfonction rénale n’a été constaté.11 Des travaux plus approfondis ont permis de découvrir que les humains étaient quasiment dépourvus d’une enzyme appelée β-lyase rénale, une enzyme clé qui transforme la biodégradation du composé A en thiol rénal toxique chez le rat.12
Le desflurane a été introduit en 1992 et sa faible solubilité dans le sang présentait l’avantage clinique d’une induction d’anesthésie et d’un réveil plus rapides, ainsi que potentiellement, un titrage plus rapide pour l’obtention de la profondeur d’anesthésie souhaitée par rapport à d’autres anesthésiques volatils utilisés. Cependant, après le lancement du desflurane, il a été découvert qu’il pouvait activer les réflexes des voies respiratoires en raison de son odeur très âcre.2
Les travaux précliniques avec le desflurane ont également permis de constater une tachycardie et une hypertension occasionnelles inexpliquées et, chez les enfants, un bronchospasme. En raison de la puissance insuffisante du desflurane, des concentrations plus fortes sont nécessaires pour obtenir l’efficacité clinique souhaitée, favorisant ainsi un effet indésirable sur les voies respiratoires en raison de son odeur âcre. Les effets indésirables sur les voies respiratoires étaient associés à une activation du système sympathique pendant l’exposition initiale des voies respiratoires, après l’induction de l’anesthésie et lors des augmentations de concentrations peropératoires.2,3 Notre laboratoire avait démontré la multiplication par 2,5 de l’activité du nerf sympathique, avec une hypertension et une tachycardie survenant lors de l’administration du desflurane après l’induction de l’anesthésie et une activation neurocirculatoire accrue lors de l’augmentation de la concentration de 1,0 à 1,5 CAM.4 Par la suite, les travaux ont indiqué que la lidocaïne nébulisée ne diminuait pas la réponse du réflexe des voies respiratoires, mais que les opiacés présentaient un effet dose dépendant de réduction de l’activation neurocirculatoire.13,14
Dans ce rapport, nous avons exploré la base de données (FAERS) à la recherche d’évènements indésirables associés au sévoflurane et au desflurane après un quart de siècle d’utilisation clinique chez des millions de patients.
Nous nous sommes efforcés de déterminer si l’auto-signalement d’évènements indésirables à la FDA validait les inquiétudes initiales entourant la sécurité du sévoflurane et du desflurane et si de nouvelles préoccupations liées à la sécurité avaient émergé lors de leur utilisation clinique dans une population très large de patients.
Méthodes
Afin de surveiller la sécurité des médicaments dans la pratique clinique, la Food and Drug Administration (FDA) a développé le système FDA Adverse Event Reporting System (FAERS).15 Le FAERS est une base de données en ligne que la FDA utilise pour surveiller tous les médicaments et produits biologiques thérapeutiques approuvés, en évaluant la quantité, la gravité et les suites globales des nouveaux médicaments, dont les anesthésiques volatils. La base de données FAERS a été interrogée à la recherche des évènements indésirables (EI) signalés pour le sévoflurane et pour le desflurane entre 1996 et décembre 2019. À l’aide de filtres démographiques, les EI ont été analysés pour les deux anesthésiques volatils, avec chacune des catégories de groupes d’âges suivantes : 0 à 1 mois, 2 mois à 2 ans, 3 à 11 ans, 12 à 17 ans, 18 à 64 ans, 65 à 85 ans, plus de 85 ans et âge non précisé. Les EI ont été triés par type de réactions. Par exemple, le type de réactions des Troubles cardiaques incluait des réactions spécifiques telles que l’arrêt cardiaque, la dissociation électromécanique (PEA) et la tachycardie ventriculaire entre autres. Pour le présent article, les réactions générales Troubles cardiaques, Troubles rénaux et urinaires et Troubles respiratoires, thoraciques et médiastinaux ont été signalées en plus des réactions spécifiques, par ex. tachyarythmies ventriculaires (tachycardie ventriculaire, fibrillation ventriculaire, torsades de pointes). Les troubles rénaux spécifiques (oligurie, anurie, lésion rénale aiguë, troubles rénaux/défaillance rénale, trouble/dysfonctionnement de la fonction tubulaire rénale et nécrose tubulaire aiguë) ont été additionnés pour réduire l’incidence d’autres réactions urinaires moins robustes, par exemple la rétention urinaire. Tous les EI ont été cités en pourcentage du nombre total de groupes de réactions de l’anesthésique concerné dans chaque groupe d’âges.
Résultats
L’utilisation du desflurane a conduit au signalement de 1140 EI, la catégorie la plus courante (type de réactions) étant « Lésions, empoisonnement et complications liées aux procédures » (24,9 %). Les quatre sous-catégories principales dans ce type de réactions comprenaient les complications postopératoires, l’exposition fœtale pendant la grossesse, les complications neurologiques de l’anesthésie et la reprise de conscience. Les EI cardiaques étaient classés en seconde position, à 23,9 %, les sous-catégories les plus courantes étant la bradycardie, l’arrêt cardiaque, la tachycardie et la tachycardie ventriculaire. Les EI respiratoires/thoraciques représentaient 19,4 %, où la principale sous-catégorie du bronchospasme comptait pour 2,9 % de l’ensemble des EI liés au desflurane. Les autres EI les plus courants étaient l’hypoxie, la dyspnée et le laryngospasme.
L’utilisation du sévoflurane a conduit au signalement de 4977 EI, avec pour type de réactions le plus courant « Lésions, empoisonnement et complications liés aux procédures » (30,4 %). Les quatre sous-catégories principales comprenaient les complications liées à l’anesthésie, les complications postopératoires, les complications neurologiques de l’anesthésie et la reprise de conscience. Comme avec le desflurane, les EI cardiaques étaient aussi le deuxième type de réactions le plus courant, à 24,4 %. Les sous-catégories les plus courantes comprenaient l’arrêt cardiaque, la bradycardie, la tachycardie et la fibrillation ventriculaire. Les évènements respiratoires/thoraciques représentaient 18,7 % des EI, semblables au desflurane. Les quatre sous-catégories étaient l’œdème pulmonaire, l’hypoxie, l’apnée et le bronchospasme (1,6 % de l’ensemble des EI liés au sévoflurane). Le laryngospasme était la sixième catégorie la plus courante dans les complications respiratoires/thoraciques. Il convient de noter que les troubles rénaux spécifiques représentaient seulement 4,4 % de l’ensemble des réactions signalées concernant le sévoflurane, par rapport à 5,3 % pour le desflurane.
La Figure 1 représente les principaux EI dans le cadre du présent rapport. Le desflurane et le sévoflurane étaient associés à des pourcentages très élevés d’EI cardiaques rapportés dans le groupe d’âges de 85 ans et plus (80 % et 63,6 %). La tachyarythmie ventriculaire était plus fréquemment présente dans la fourchette d’âges comprise entre 12 et 17 ans à 26,8 % pour le desflurane par rapport à 8,2 % pour le sévoflurane. Il y avait très peu d’évènements indésirables dans le groupe d’âges néonataux pour le desflurane, toutefois il tend à ne pas être utilisé pour les patients de moins de 2 ans en raison des recommandations du fabriquant. Le pourcentage d’évènements respiratoires de l’ensemble des EI pour le desflurane par rapport au sévoflurane était considérablement plus élevé dans les tranches d’âges de 2 mois à 2 ans et de 3 à 11 ans.
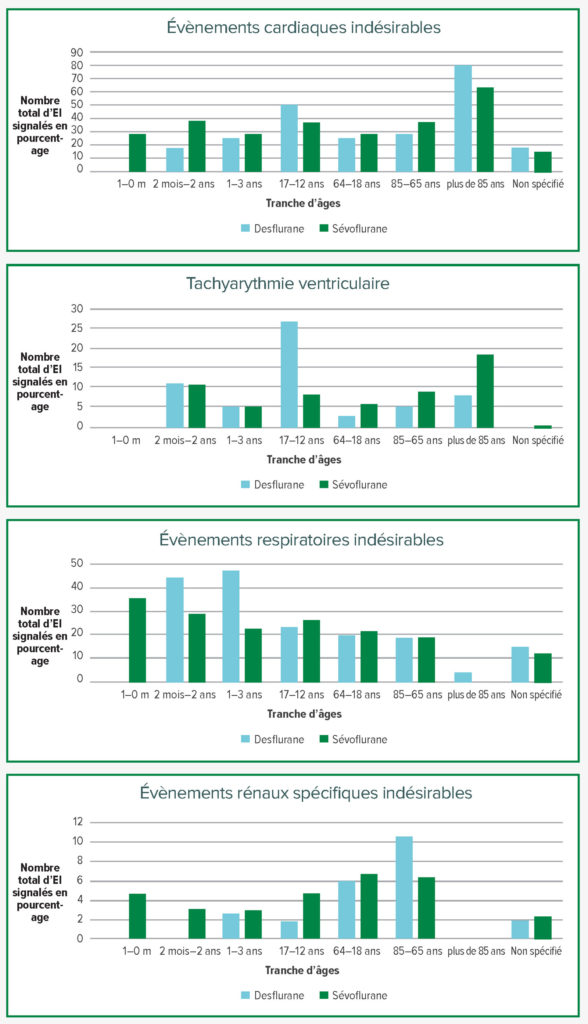
Figure 1 : Évènements indésirables (EI) causés par le desflurane et le sévoflurane par tranche d’âges.
Discussion
La base de données FAERS contenait 1140 évènements indésirables signalés pour le desflurane et 4977 pour le sévoflurane. La fréquence des signalements d’EI est liée au nombre total d’administrations de chacun de ces anesthésiques dans la pratique clinique. Cependant le signalement des EI confirme, par la prévalence des EI pour chaque anesthésique, un certain nombre de domaines susceptibles de susciter des préoccupations à propos de ces deux anesthésiques volatils dans le cadre d’une utilisation clinique. Les EI cardiaques étaient le deuxième type de réactions le plus fréquemment signalé pour les deux anesthésiques. Le pourcentage de tachyarythmies ventriculaires était plus élevé avec le desflurane dans une population plus jeune, mais était plus élevé dans une population plus âgée avec le sévoflurane. Les évènements respiratoires étaient plus fréquents que les autres évènements indésirables chez les patients plus jeunes anesthésiés au desflurane. Le plus grand pourcentage dans le type d’EI « Lésions, empoisonnement et complications liées aux procédures » correspondait à la reprise de conscience et aux EI neurologiques, comprenant probablement l’agitation postopératoire et le déclin cognitif.
Il existe un certain nombre de liens entre la base de données FAERS et la science clinique de chaque anesthésique.
Arythmies et anesthésiques volatils : Les études in vitro ont permis de démontrer que le desflurane pourrait augmenter la libération de catécholamines intra myocardique,16 entraînant le déclenchement d’arythmies. Il a été démontré que le desflurane était lié à un plus grand nombre d’arythmies que le sévoflurane lors d’une chirurgie pour pontage aortocoronarien sans circulation extra corporelle,17 et à un taux plus élevé de fibrillations atriales postopératoires après une chirurgie cardiaque sous circulation extracorporelle.18 La variabilité inter-dérivations de l’intervalle QT, appelée « dispersion QT (QTd) », est un marqueur d’anomalies régionales de la repolarisation ventriculaire qui est davantage lié au risque de dysrythmie que l’intervalle QT proprement dit.19 Chez les adultes en bonne santé qui subissent une chirurgie non cardiaque, l’induction de l’anesthésie au desflurane seul (sans prémédication) semblait augmenter considérablement la QTd, alors que l’induction au sévoflurane seul n’influait pas sur la QTd 20. Cependant, lorsque le midazolam et le vécuronium étaient utilisés avant l’intubation, le desflurane et le sévoflurane prolongeaient tous les deux la QTd sans différence notable entre les deux.21 Alors qu’une QTd prolongée peut entraîner diverses arythmies, son lien avec l’activation du système sympathique, plus souvent associée au desflurane, est inconnu.
Troubles respiratoires et anesthésiques volatils : Le pourcentage d’EI respiratoires était élevé dans le groupe de patients plus jeunes. Comme indiqué précédemment, au cours des premières années d’utilisation du desflurane dans la pratique clinique, des préoccupations ont été soulevées concernant son odeur âcre et l’irritation des voies respiratoires. Comme l’ont démontré les études précédentes relatives aux effets respiratoires du desflurane, la différence entre les adultes et les enfants est claire. Dans une étude d’une grande cohorte de 14 000 enfants, les chercheurs ont constaté que l’utilisation du desflurane constituait un facteur de risque d’évènements peropératoires en tous genres, ainsi que de laryngospasme en particulier.5 Dans un essai clinique portant sur 400 enfants en bonne santé, randomisés pour recevoir du desflurane ou de l’isoflurane, ceux qui avaient reçu le desflurane présentaient une fréquence beaucoup plus élevée d’évènements indésirables liés aux voies respiratoires de gravités diverses, allant de la toux au laryngospasme.6 Néanmoins, les résultats sont très différents chez les adultes. Une méta-analyse de 13 essais contrôlés randomisés a montré qu’il n’y avait aucune différence entre le sévoflurane et le desflurane en matière de nombres d’évènements indésirables concernant les voies aériennes supérieures, le laryngospasme, ou la toux au réveil.22 Une autre méta-analyse de sept essais contrôlés randomisés n’a pas retrouvé de différence entre le sévoflurane et le desflurane en matière d’incidence de toux ou de laryngospasme chez les adultes.23
Limitations
La FAERS s’appuie sur le signalement volontaire des évènements indésirables par les soignants et les consommateurs aux États-Unis. Pour cette raison, cette base de données présente d’importantes limites. Premièrement, il n’existe aucune certitude que l’évènement indésirable signalé ait été causé par le médicament en question, car la FDA ne demande pas la preuve d’une relation de cause à effet. Deuxièmement, la FDA ne reçoit pas chacun des évènements indésirables survenant pour un médicament donné. De nombreux facteurs déterminent si un signalement sera déposé, tels que la gravité ou la notoriété liée à l’évènement. Il est attendu que les effets indésirables plus graves, tels que les arythmies cardiaques, seront probablement signalées plus fréquemment que d’autres réactions moins graves, telles que les nausées postopératoires. Pour cette raison, la base de données ne peut pas être utilisée pour calculer l’incidence d’un évènement indésirable donné au sein de la population. La fréquence de l’utilisation du sévoflurane est plus élevée que celle du desflurane chez les patients pédiatriques et adultes.24 Par conséquent, le nombre total d’évènements indésirables d’un anesthésique volatil n’est pas pertinent sans connaître exactement le dénominateur.
Conclusions : Contrairement à d’autres anesthésiques pour lesquels l’utilisation clinique a révélé des inquiétudes nouvelles ou inattendues en matière de sécurité, telles que l’hépatite causée par l’halothane ou l’anaphylaxie induite par le rapacuronium, il ne semble pas qu’après près de 30 années d’utilisation du desflurane et du sévoflurane, on puisse constater des phénomènes indésirables nouveaux ou inattendus. Les études qui identifiaient des modifications neurocirculatoires causées par les effets irritants des voies respiratoires du desflurane, ou l’absence de lésions rénales du sévoflurane, ont été approfondies pour expliquer les conclusions tirées des données auto-signalées dans la FAERS. Le desflurane présentait une forte incidence d’évènements indésirables des voies aériennes chez les populations plus jeunes que l’on ne retrouvait pas chez les patients plus âgés. Des arythmies cardiaques ont été constatées avec les deux anesthésiques et une plus forte prévalence de tachycardie ventriculaire a été notée avec le desflurane chez les patients plus jeunes.
Le Dr Thomas Ebert, PhD, est professeur d’anesthésiologie au Medical College of Wisconsin, Milwaukee, WI, et chef du service d’anesthésie au Clement J. Zablocki Veterans Affairs Medical Center, Milwaukee WI.
Le Dr Alex Ritchay est résident anesthésiste au Medical College of Wisconsin dans le service d’anesthésiologie, Milwaukee, WI.
Aaron Sandock, BA, est étudiant en médecine au Medical College of Wisconsin, Milwaukee, WI.
Shannon Dugan, BS, est assistante de recherche au Medical College of Wisconsin, Milwaukee, WI.
Les auteurs ne signalent aucun conflit d’intérêts.
Documents de référence
- Gonsowski C, Laster M, Eger E, et al. Toxicity of compound A in rats. Anesthesiology. 1994;80:566–573.
- Muzi M, Lopatka C, Ebert T. Desflurane-mediated neurocirculatory activation in humans: effects of concentration and rate of change on responses. Anesthesiology. 1996;84: 1035–1042.
- Welskopf R, Moore M, Eger E, et al. Rapid increase in desflurane concentration is associated with greater transient cardiovascular stimulation than with rapid increase in isoflurane concentration in humans. Anesthesiology. 1994;80:1035–1045.
- Ebert T, Muzi M. Sympathetic hyperactivity during desflurane anesthesia in healthy volunteers. Anesthesiology. 1993;79:444–453.
- Oofuvong M, Geater A, Chongsuvivatwong V, et al. Risk over time and risk factors of intraoperative respiratory events: a historical cohort study of 14,153 children. BMC Anesthesiology. 2014;14:13.
- Lerman J, Hammer, G. Response to: Airway responses to desflurane during maintenance of anesthesia and recovery in children with laryngeal mask airways. Paediatr Anaesth. 2010;20:962–963.
- Habibollahi P, Mahboobi N, Esmaeili S, et al. Halothane-induced hepatitis: a forgotten issue in developing countries. Hepat Mon. 2011;11:3–6.
- Sosis MB. Further comments on the withdrawal of rapacuronium. Anesthesia & Analgesia. 2002;95:1126–1127.
- Sloane R, Osanlou O, Lewis D, et al. Social media and pharmacovigilance: a review of the opportunities and challenges. Br J Clin Pharmacol. 2015; 80:910–920.
- Smith I, Nathanson M, White P. Sevoflurane-a long-awaited volatile anaesthetic. Br J Anaesth. 1996;76:435–445.
- Ebert T, Frink E, Kharasch E. Absence of biochemical evidence for renal and hepatic dysfunction after 8 hours of 1.25 minimum alveolar concentration sevoflurane anesthesia in volunteers. Anesthesiology. 1998;88:601–610.
- Kharasch E, Jubert C. Compound A uptake and metabolism to mercapturic acids and 3,3,3-trifluoro-2-fluoromethoxypropanoic acid during low-flow sevoflurane anesthesia. Anesthesiology. 1999;91:1267–1278.
- Bunting H, Kelly M, Milligan K. Effect of nebulized lignocaine on airway irritation and haemodynamic changes during induction of anaesthesia with desflurane. Br J Anaesth. 1995;75:631–633.
- Pacentine G, Muzi M, Ebert T. Effects of fentanyl on sympathetic activation associated with the administration of desflurane. Anesthesiology. 1995;82:823–831.
- U.S. Food and Drug Administration. 2020. Potential signals of serious risks by FAERS. [online] Available at: https://www.fda.gov/Drugs/GuidanceComplianceRegulatoryInformation/Surveillance/AdverseDrugEffects/ucm565425.htm Accessed March 9, 2020.
- Park WK, Kim MH, Ahn DS, et al. Myocardial depressant effects of desflurane: mechanical and electrophysiologic actions in vitro. Anesthesiology. 2007;106:956–966.
- Hemmerling T, Minardi C, Zaouter C, et al. Sevoflurane causes less arrhythmias than desflurane after off-pump coronary artery bypass grafting: a pilot study. Ann Card Anaesth. 2010;13:116.
- Cromheecke S, ten Broecke PW, Hendrickx E, et al. Incidence of atrial fibrillation early after cardiac surgery: can choice of the anesthetic regimen influence the incidence? Acta Anaesthesiol Belg. 2005;56:147–54.
- Day C, McComb J, Campbell R. QT dispersion: an indication of arrhythmia risk in patients with long QT intervals. Heart. 1990;63:342–344.
- Yildirim H, Adanir T, Atay A, et al. The effects of sevoflurane, isoflurane and desflurane on QT interval of the ECG. Eur J Anaesthesiol. 2004; 21: 566-570.
- Kazanci D, Unver S, Karadeniz U, et al. A comparison of the effects of desflurane, sevoflurane and propofol on QT, QTc, and P dispersion on ECG. Ann Card Anaesth. 2009;12:107.
- Stevanovic A, Rossaint R, Fritz H, et al. Airway reactions and emergence times in general laryngeal mask airway anaesthesia. Eur J Anaesthesiol. 2015;32:106–116.
- de Oliveira G, Girao W, Fitzgerald P, et al. The effect of sevoflurane versus desflurane on the incidence of upper respiratory morbidity in patients undergoing general anesthesia with a Laryngeal Mask Airway: a meta-analysis of randomized controlled trials. J Clin Anesth. 2013;25:452–458.
- Nasr G, Davis M. Anesthetic use in newborn infants: the urgent need for rigorous evaluation. Pediatr Res. 2015;78: 2–6.

