Nous présentons deux cas de lésions thermiques liées à l’utilisation d’un système de réchauffement par convection. Dans les deux cas, les alarmes audibles et visuelles de « surchauffe » ne se sont pas déclenchées. Dans l’un des cas, le collecteur d’air avait été oublié. Nous avons demandé au fabricant, Smiths Medical, de donner son opinion sur ces cas et de proposer des suggestions aux anesthésistes à propos de l’utilisation des appareils de réchauffement par convection en toute sécurité. D’autre part, nous avons mis en évidence les défis cliniques associés à certaines des recommandations du mode d’emploi.
Réponse rapide,
Deux patients consécutifs ont subi des lésions thermiques semblables aux extrémités supérieures et au torse après l’utilisation d’un système de réchauffement par convection. Les deux patients étaient opérés d’une prostatectomie laparoscopique robot-assistée en position de Trendelenburg, les bras le long du corps. Les interventions ont été réalisées l’une après l’autre dans le même bloc opératoire, avec le même personnel. Dans les deux cas, un système de réchauffement par convection Smiths Medical EQUATOR® Level 1® a été utilisé, associé à une petite couverture chauffante par convection pour le haut du corps Snuggle Warm®. La couverture chauffante pour le haut du corps a été fixée sur le patient grâce aux bandes adhésives intégrées, placées juste en dessous de la ligne des tétons. Aucune autre couverture n’a été posée par-dessus (ou en dessous) de la couverture chauffante. Les « bras » de la couverture chauffante ont été glissés dans le creux entre la table du bloc opératoire et les coussins puisque les bras du patient étaient le long du corps. Le conduit a ensuite été connecté à la couverture chauffante, sur le port de connexion de la couverture près de l’épaule gauche et il a été suspendu par un clip de maintien (Figure 1). Remarque : dans l’un des cas, il a été confirmé que le collecteur d’air avait été oublié par erreur. Le collecteur d’air est un tube en plastique en forme de « coude » connecté à l’extrémité du conduit de réchauffement, avec plusieurs ouvertures à l’extrémité distale, afin de disperser uniformément l’air chaud sur le patient (Figure 2, Image A). Le dispositif de chauffage a été réglé à la température de 44° C (réglage haut) dans les deux cas. Pendant l’opération, le dispositif chauffant a semblé fonctionner correctement, sans alarme sonore ou visuelle. Les deux patients étaient hémodynamiquement stables et normothermiques par surveillance nasopharyngée de la température pendant toute la durée de l’intervention. En salle de réveil, il a été noté que les deux patients présentaient un érythème diffus de l’extrémité supérieure gauche et du torse, à proximité de la connexion du port de la couverture. Le premier jour après l’intervention, des cloques sont apparues sur l’épaule et le torse des deux patients (Figure 3), qui ont fini par se résorber avec une gestion conservatrice.
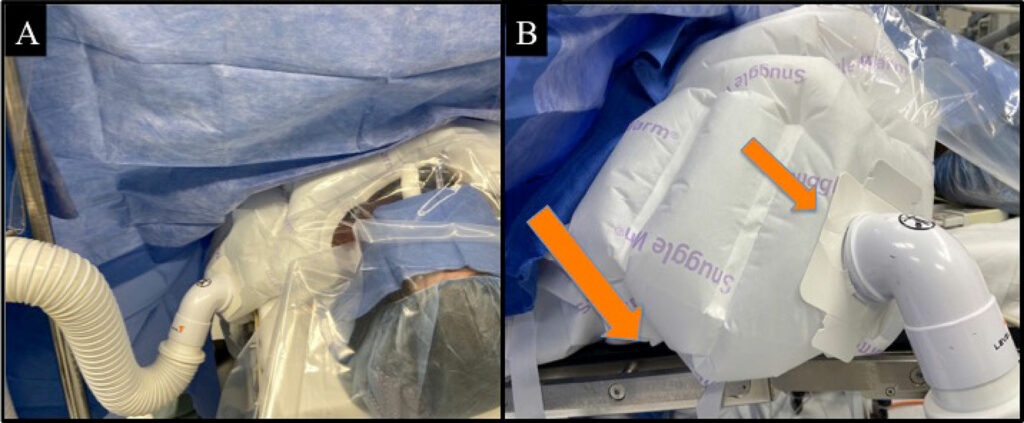
Figure 1 : L’image A présente la configuration du réchauffeur dans ces cas, avec le conduit de réchauffement connecté au port de connexion de la couverture chauffante du haut du corps, à proximité de l’épaule gauche. Le conduit de réchauffement est suspendu à l’aide d’une pince. Les flèches orange de l’image B indiquent les « bras » de la couverture chauffante glissés dans le creux entre la table du bloc opératoire et les coussins et le port de connexion à proximité de l’épaule gauche du patient.
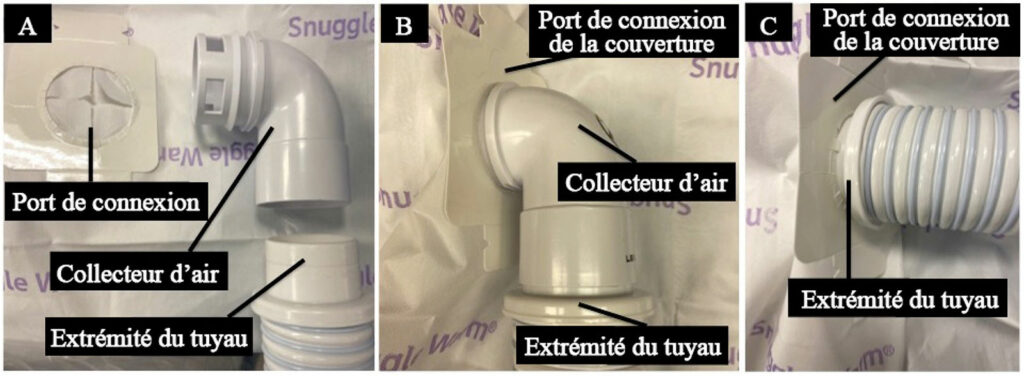
Figure 2 : L’image A représente l’extrémité du conduit démonté du collecteur d’air. Il convient de noter les perforations à l’extrémité distale du collecteur d’air, qui distribuent le flux d’air à travers la couverture chauffante. L’image B représente la connexion correcte de l’extrémité du conduit sur le collecteur d’air, qui se connecte ensuite sur le port de la couverture. L’image C représente la manière d’insérer (accidentellement) l’extrémité du conduit directement dans le port de la couverture si le collecteur d’air est absent.
Discussion
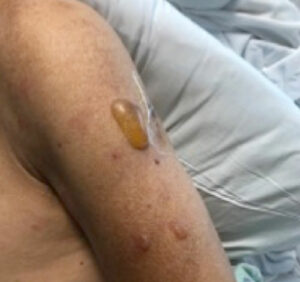
Figure 3 : Cloques constatées le lendemain de l’opération (le patient a donné son consentement à l’utilisation de cette image).
Les systèmes de réchauffement par convection sont couramment utilisés pour éviter l’hypothermie.1,2 L’hypothermie majore les infections du site, les pertes de sang et les évènements cardiaques. Les Centers of Medicare & Medicaid Services ont récemment ajouté la « gestion périopératoire de la température » comme mesure essentielle de l’anesthésie, nécessitant des températures post-opératoires supérieures à 35,5°C pour les procédures d’une durée supérieure à 60 minutes.
Les brûlures sont rares lorsque les consignes du fabricant sont respectées.3 Les lésions thermiques qui surviennent sont souvent le résultat d’une mauvaise utilisation du dispositif.4-6 La forme la plus courante d’une mauvaise utilisation survient lorsque le conduit est placé en contact ou à proximité de la peau du patient, sans utiliser de couverture chauffante. Le système de réchauffement par convection Smiths Medical EQUATOR® Level 1® est doté de plusieurs sécurités pour réduire le risque de brûlures, notamment des alarmes de « surchauffe », un indicateur d’entretien et un indicateur d’occlusion.
Dans les cas présentés ici, la cause des brûlures est encore à l’étude. Le type de lésion suggère une zone focale de surchauffe à l’endroit où le tube se connecte à la couverture chauffante. Nous pensons que l’alarme de « surchauffe » était éventuellement défectueuse. D’après le mode d’emploi, « la thermistance de sécurité s’active et déclenche une alarme si la température atteint 3°C au-dessus du point de consigne…le circuit fournit un moyen indépendant de coupure, qui coupe l’alimentation du réchauffeur et du ventilateur. » Bien que de nombreux facteurs contribuent au développement d’une brûlure ( température, durée d’exposition, etc.), une explication potentielle dans ces cas pourrait être que la température de l’air était supérieure au point de consigne de 47°C de l’alarme. Un autre facteur contributif possible est l’absence involontaire du collecteur d’air (confirmée dans l’un des deux cas). D’après le mode d’emploi, le collecteur d’air « distribue de l’air chaud aux conduits de manière à promouvoir le transfert de chaleur au patient…des perforations côté patient du conduit d’air dispersent l’air chaud sur le patient, afin de maintenir la température du patient ». Il est possible que l’absence de collecteur d’air ait causé la concentration d’un apport d’air chaud sur une petite surface du patient, ce qui expliquerait le type de lésion. Étant donné que deux dispositifs identiques étaient présents au bloc opératoire le jour où les lésions ont été causées, ils ont été renvoyés à Smiths Medical pour une investigation plus poussée (bien que nous suspections que le coupable ait été le même appareil dans les deux cas). Les résultats de cette investigation n’ont pas encore été publiés.
Ces cas permettent de déclencher le dialogue avec Smiths Medical dans un effort d’amélioration de la sécurité des patients. Premièrement, nous demandons à Smiths Medical de commenter l’importance du collecteur d’air. La Figure 2 montre comment le conduit et le collecteur d’air peuvent être démontés et comment le conduit peut se connecter directement à la couverture chauffante, sans le collecteur d’air. Si le collecteur d’air est essentiel au fonctionnement du dispositif en toute sécurité, pourquoi peut-il être démonté ? S’il doit être démontable, faudrait-il apposer une « étiquette d’avertissement » autour de l’extrémité du conduit pour alerter l’utilisateur du danger potentiel de la connexion directe sur le port de la couverture (Figure 2, Image C) ? D’autre part, le fabricant a-t-il envisagé une « fonction de forçage » qui empêcherait la connexion du conduit au port de la couverture sans collecteur d’air (c.-à-d. semblable au dispositif qui empêche d’insérer une pompe à diesel dans un réservoir d’essence standard) ?
Ensuite, nous avons demandé à Smiths Medical de répondre à plusieurs questions concernant le mode d’emploi du réchauffeur par convection EQUATOR® Level 1®, qui contient une longue liste d’avertissements destinés à éviter les lésions des patients. Ces avertissements sont majoritairement intuitifs et font partie des précautions habituelles, mais certains sont difficiles à concilier avec la réalité des soins cliniques, à savoir :
« Pour prévenir les lésions thermiques, ne pas utiliser le réglage de température le plus élevé pour traiter des patients qui ont une diminution de la sensation, qui n’ont aucune sensation ou qui ont une mauvaise perfusion. »
Les patients sous anesthésie générale n’ont pas de sensation par définition, cependant il faut leur procurer un réchauffement actif pour éviter l’hypothermie. Le fabricant suggère-t-il qu’il faut éviter totalement le réglage à la température la plus élevée chez les patients sous anesthésie générale ?
« Toujours débuter la thérapie au réglage de température non ambiante la plus basse pour éviter les lésions thermiques. Augmenter la température, le cas échéant, en utilisant comme indicateurs la température corporelle centrale et la réponse cutanée de la peau en contact avec la couverture chauffante par convection. »
Le réchauffeur par convection est généralement démarré au réglage le plus élevé pour éviter une perte de chaleur rapide causée par le rayonnement, la conduction, la convection et l’évaporation. Le fabricant conseille-t-il de proscrire cette pratique ? Dans ce cas, y a-t-il des exceptions où le démarrage au réglage le plus élevé serait justifié (par ex. un patient victime d’un traumatisme subissant une intervention chirurgicale importante et présentant le risque d’hypothermie et de coagulopathie associée) ? Faut-il respecter un délai minimum à chaque palier de réglage avant de passer au suivant ?
« …Observer la réponse cutanée à intervalles réguliers pour éviter les lésions thermiques. En cas d’apparition d’un érythème ou d’une instabilité des signes vitaux, réduire le réglage de la température ou arrêter l’utilisation de la thérapie de réchauffement par convection. »
Il peut être difficile, voire impossible de reconnaître une brûlure en cours de développement, même pour le plus vigilant des anesthésistes, car les signes cliniques peuvent rester absents alors que la lésion est déjà survenue. En outre, le site est souvent inaccessible ou couvert par la couverture chauffante ou les champs chirurgicaux. Par ailleurs, l’éclairage dans un bloc opératoire peut être tamisé, rendant la détection d’un érythème léger d’autant plus difficile.
La suggestion du fabricant qu’une instabilité des signes vitaux mérite l’arrêt de la thérapie chauffante est probablement une simplification excessive des perturbations physiologiques complexes qui surviennent pendant l’anesthésie et la chirurgie. Le diagnostic différentiel d’une instabilité des signes vitaux pendant une intervention est large et l’arrêt de la thérapie chauffante peut être contre-indiquée dans certaines situations (par ex. un patient qui est en hypotension artérielle en raison d’un choc hémorragique, où la coagulopathie peut être aggravée par l’hypothermie).
« Pour prévenir les lésions thermiques, ne pas laisser une partie du corps du patient en contact avec l’entrée du conduit »
La conception de la couverture Snuggle Warm® place automatiquement l’entrée du conduit à proximité de l’épaule du patient. Le fabricant a-t-il envisagé de modifier la conception de la couverture chauffante, de sorte que le port de connexion soit plus éloigné du patient (c.-à-d. en créant une rallonge du type « trompe d’éléphant ») ? Lorsque les bras du patient sont placés le long de son corps, il est courant de glisser les bords de la couverture chauffante du haut du corps dans le creux entre la table du bloc opératoire et les coussins. Cette pratique restreint-elle le débit d’air et augmente-t-elle le risque de lésions thermiques ? Dans ce cas, quelles sont les recommandations du fabricant au titre de l’utilisation de la couverture du haut du corps pour un patient avec les bras placés le long du corps ?
Notre service a pris de nombreuses mesures pour renforcer la sensibilisation au sujet de ces problèmes de sécurité et communiqué les recommandations suivantes aux membres de l’équipe d’anesthésie :
- Toujours confirmer la présence du collecteur d’air avant de connecter le conduit à la couverture chauffante.
- Démarrer à température moyenne (40°C) sauf indication contraire.
- Prendre soin de ne pas restreindre le débit d’air dans la couverture chauffante.
Nous invitons Smiths Medical à répondre à ce rapport et apprécierons leurs suggestions concernant l’utilisation des systèmes de réchauffement par convection en toute sécurité.
Cordialement,
Luke S. Janik, MD
Ryan Lewandowski, SRNA
Article de réponse : Systèmes de réchauffement par convection – Maintenir la normothermie au bloc opératoire
Article de réponse : Réchauffeurs par convection et brûlures — Toujours un danger immédiat
Luke Janik, MD, est actuellement professeur assistant clinique du Département d’anesthésie-réanimation de l’Université de Chicago et anesthésiste-réanimateur du Département d’anesthésie-réanimation et médecine de la douleur du NorthShore University HealthSystem à Evanston, Illinois.
Ryan Lewandowski, SRNA, est actuellement étudiant infirmier-anesthésiste à la School of Nurse Anesthesia de NorthShore University HealthSystem à Evanston, Illinois.
Les auteurs ne signalent aucun conflit d’intérêts.
Documents de référence
- Ohki K, Kawano R, Yoshida M, et al. Normothermia is best achieved by warming above and below with pre-warming adjunct: a comparison of conductive fabric versus forced-air and water. Surg Technol Int. 2019;34:40–45.
- Nieh HC, Su SF. Meta-analysis: effectiveness of forced-air warming for prevention of perioperative hypothermia in surgical patients. J Adv Nurs. 2016;72:2294–2314.
- Bräuer A, Quintel M. Forced-air warming: technology, physical background and practical aspects. Curr Opin Anaesthesiol. 2009;22:769–774.
- Chung K, Lee S, Oh SC, et al. Thermal burn injury associated with a forced-air warming device. Korean J Anesthesiol. 2012;62:391–392.
- Uzun G, Mutluoglu M, Evinc R, et al. Severe burn injury associated with misuse of forced-air warming device. J Anesth. 2010;24:980–981.
- Truell KD, Bakerman PR, Teodori MF, Maze A. Third-degree burns due to intraoperative use of a Bair Hugger warming device. Ann Thorac Surg. 2000;69:1933–1934.
Ces informations sont fournies à des fins de formation liée à la sécurité et ne doivent pas être interprétées comme un avis médical ou légal. Les réponses individuelles ou de groupe ne sont que des commentaires fournis à des fins de formation ou de discussion et ne sont ni des déclarations d’avis ni des opinions de l’APSF. Il n’est pas dans l’intention de l’APSF de fournir un avis médical ou légal spécifique ni de se porter garante des points de vue ou recommandations exprimés en réponse aux questions postées. L’APSF ne pourra en aucun cas être tenue responsable, directement ou indirectement, des dommages ou des pertes causés ou présumés avoir été causés par, ou en rapport avec la confiance accordée à, ces informations.


 Issue PDF
Issue PDF