| 本文曾发布在 APSF 在线门户网站上。 本版本将由本期 APSF Newsletter 的作者进行更新和修改。 |
尊敬的快速答复栏目,
因 COVID-19 所导致的全球危机已经渗透到我们医疗照护系统的每个方面。有关 SARS-CoV-2 的生物危害、如何向患者、医疗照护人员、环境和设备传播和接触传染等问题已被广泛宣传,尤其是产气溶胶(AGP)操作的问题。1-3病毒主要是呼吸性传播。SARS-CoV-2 病毒粒子的直径约为 120 纳米 (0.06–0.14 μm),可通过生物载体微粒(如飞沫或气溶胶等)进行人际间传播。2,3 关于进行充足的 PPE、洗手、表面清洁、去污以及气道管理过程中的注意事项等建议,已经在全球大流行期间进行了广泛讨论。4-6 与其他的呼吸道传播疾病一样,我们依赖于两种重要的过滤系统:回路式过滤器(当在手术室和/或重症监护室 (ICU) 内使用人工呼吸系统时)和面罩式呼吸器。
但往往没有这么简单:
- 麻醉机和人工呼吸机需要过滤器来净化空气和预防交叉污染。这种过滤器的过滤效率标准被称为具有高效微粒空气/高效微粒吸收能力的 HEPA。7ASA 建议在呼吸回路的 Y-形片和患者的通气面罩、气管导气管或喉罩气道之间放置 HEPA 过滤器。8
- 欧洲与美国用于确定过滤器过滤效率的标准并不相同:欧洲标准使用 99.95% 的微粒(直径为 0.3 μm)去除率,而美国标准则使用 99.97% 的微粒去除率。9
- 可通过微粒的透过水平来确定口罩过滤效率。例如,N95 口罩至少可以去除 95% 的 300 nm 微粒 – 使用的气流速率为 85 升/分钟。10 面罩式呼吸器可根据美国国家职业安全与卫生研究所 (NIOSH) 和国际上认可的标准和测试方法来进行监管。
- 呼吸回路和麻醉机中的过滤器并未受到监管。没有针对呼吸回路中的过滤器的国家或国际标准检验方法。由于没有标准测试,因此在讨论过滤效率水平时,结果是否都与制造商报告的相同?11
- 当前可以使用的过滤器是否足以应对 COVID-19?
- 由于许多 COVID-19 患者需要长时间机械通气,因此在 ICU 中,这些过滤器应当多久更换一次?
- 如遇过滤器短缺,医疗照护人员应该怎么办?
这些是一些关于 HEPA 过滤器的紧迫问题,我希望看到讨论。
谢谢。
Felipe Urdaneta
临床麻醉学教授
弗洛里达大学/NFSGVHS
弗洛里达州盖恩斯维尔市
作者是美敦力公司的顾问和 Vyaire 公司的咨询委员会成员,并已经收到了作为公司代言人的酬金。
参考文献
- Canova V, Lederer Schlpfer H, Piso RJ, et al. Transmission risk of SARS-CoV-2 to healthcare workers—observational results of a primary care hospital contact tracing. Swiss Medical Weekly. 2020;150:1–5.
- Asadi S, Bouvier N, Wexler AS, et al. The coronavirus pandemic and aerosols: Does COVID-19 transmit via expiratory particles? Aerosol Sci Technol. 2020;0:1–4.
- van Doremalen N, Bushmaker T, Morris DH, et al. Aerosol and surface stability of SARS-CoV-2 as compared with SARS-CoV-1. N Engl J Med. 2020;382:1564–1567.
- Asenjo JF. Safer intubation and extubation of patients with COVID-19. Can J Anaesth. 2020:1–3.
- Chia SE, Koh D, Fones C, et al. Appropriate use of personal protective equipment among healthcare workers in public sector hospitals and primary healthcare polyclinics during the SARS outbreak in Singapore. Occup Environ Med. 2005;62:473–477.
- Sorbello M, El-Boghdadly K, Di Giacinto I, et al. The Italian coronavirus disease 2019 outbreak: recommendations from clinical practice. Anaesthesia. 2020;75:724–732.
- First MW. Hepa filters. Appl Biosaf. 1998;3:33–42.
- American Society of Anesthesiologists. Information for health care professionals. Published 2020. https://www.asahq.org/about-asa/governance-and-committees/asa-committees/committee-on-occupational-health/coronavirus. Accessed June, 2020.
- Wikipedia. HEPA. https://en.wikipedia.org/wiki/HEPA. Accessed June 9, 2020.
- Haghighat F, Bahloul A, Lara J, et al. Development of a procedure to measure the effectiveness of N95 respirator filters against nanoparticles. 2012.
- NIOSH-Approved Particulate Filtering Facepiece Respirators. https://www.cdc.gov/niosh/npptl/topics/respirators/disp_part/default.html. Accessed June 9, 2020.
回复:
我们感谢 Felipe Urdaneta(医学博士)着重回答了有关使用麻醉呼吸系统过滤器以应对 COVID-19 全球大流行的疑难问题。APSF 网站有一个页面 (https://www.apsf.org/faq-on-anesthesia-machine-use-protection-and-decontamination-during-the-covid-19-pandemic/) 总结了当前为保护麻醉机免受潜在感染患者污染而采取的策略。但其并未提供这些建议所蕴含的某些细节问题。本文将提供相关细节,如患者通过呼吸系统被传染-感染的风险、病毒传播的模式、过滤作用的物理知识、过滤器的类型以及标准化的检验方法和过滤器的质量标准等,以回答 Felipe Urdaneta 的提问,并明晰本刊读者中出现的类似疑问。
患者通过呼吸系统被交叉感染的风险
由于重新呼吸之前被呼出的气体,因此回路式呼吸系统理论上存在患者交叉感染的风险。上世纪九十年代以前,尚未常规使用麻醉呼吸系统过滤器,因为通过呈碱性的二氧化碳吸附剂来传送呼出的气体,这被认为可以防止患者被交叉感染。1但在上世纪九十年代,在报告了被污染的麻醉呼吸系统导致的九个丙型肝炎交叉感染病例以后2,使用麻醉呼吸系统过滤器的情况日益增多。3存在相互矛盾的潜在交叉感染证据;几乎没有任何案例得到了证实,但体外试验证实有这种可能性。4-6在许多案例中,很多麻醉协会均建议使用呼吸系统过滤器,但仅仅是在患者间重复使用呼吸回路时。7,8
呼吸道病毒的传播模式
与严重急性呼吸系统综合征 (SARS-CoV)、中东呼吸综合征相关性冠状病毒 (MERS-CoV) 和其他冠状病毒一样,COVID-19 (SARS-CoV-2) 主要是通过呼吸途径传播。该病通过直径大于 20 微米的飞沫以及直径小于 5–10 微米的气溶胶进行传播。9飞沫因重力倾向于落地,而气溶胶微粒则会漂浮在空气中,并随着气流流动。中等大小的微粒具有与飞沫和气溶胶相同的某些特性。小飞沫的快速蒸发会导致产生更小的飞沫核,也会随着气流流动。飞沫、气溶胶和中等大小的微粒均是在咳嗽、打喷嚏和谈话过程中产生的,而气溶胶则主要是在被动呼吸过程中产生的。过滤病原体中的一个重要理念是,呼吸道病毒不会通过漂浮在空气中的单个病毒微粒进行传播,但可以通过较大微粒中包含的多个病毒进行传播。飞沫和某些中等大小的微粒可以停留在表面,有可能导致表面转播。
尚没有任何研究表明 SARS-CoV-2 感染者到底能呼出多少病毒微粒。但有一项研究定量分析了呼出的其他呼吸道病毒微粒,结果发现,季节性冠状病毒感染患者每小时呼出和咳出了 0 – 200,000 个病毒微粒。10
尽管单个病毒微粒在理论上可以导致系统性感染,但是感染的几率随着病毒暴露的时间和幅度增加而增加。11
过滤作用的物理学原理
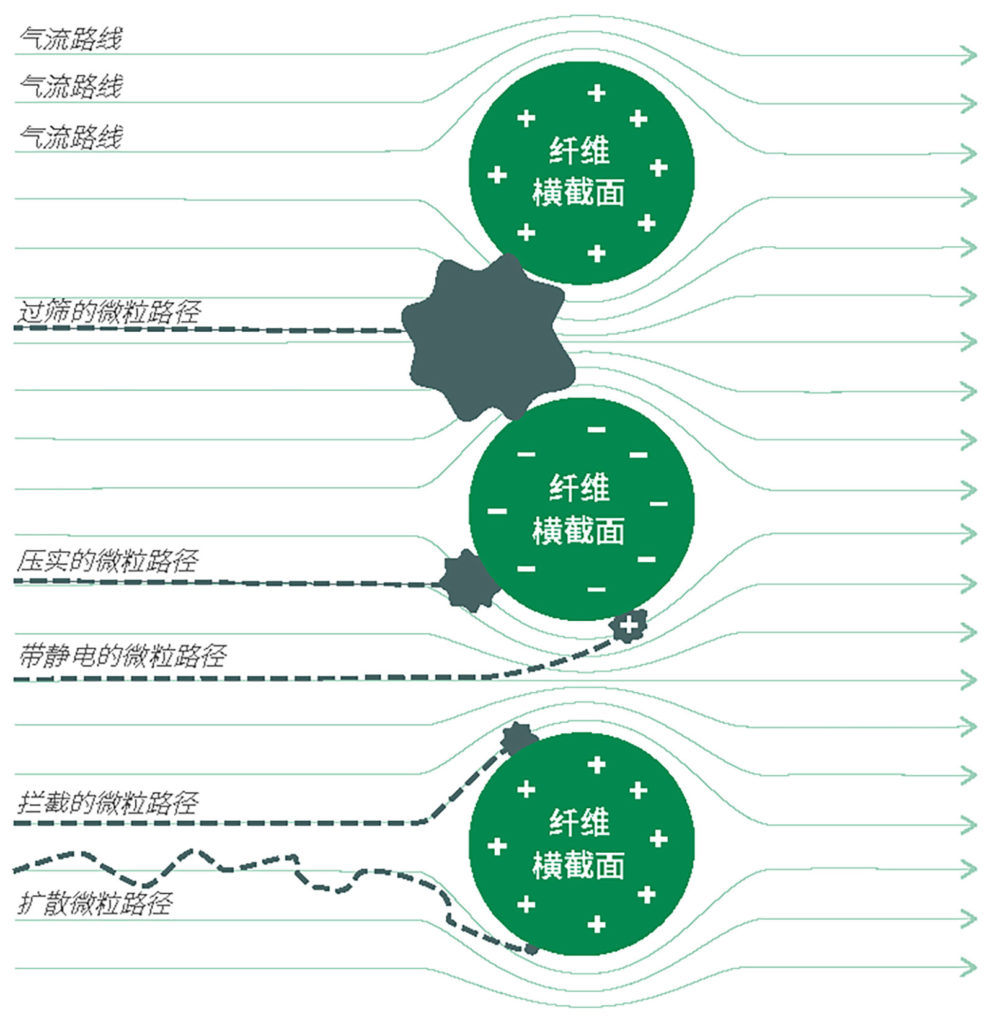
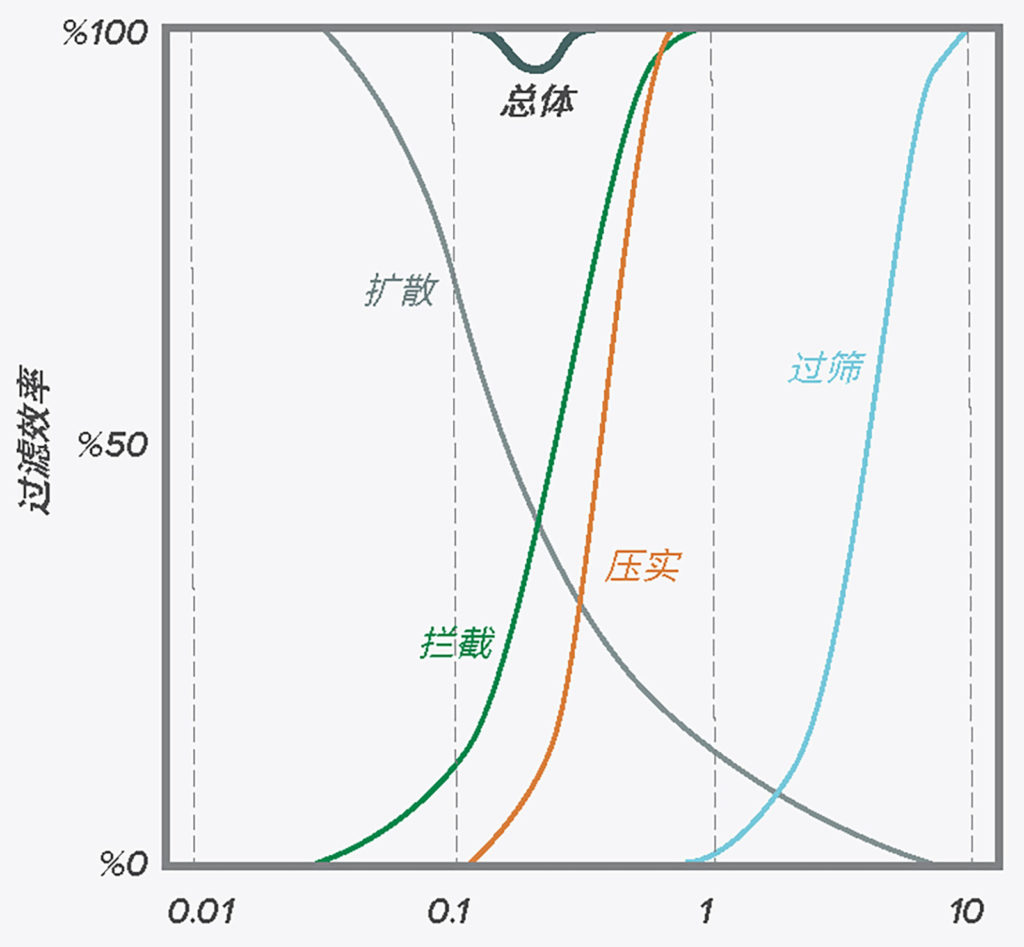
人们通常懂得筛网过滤的物理学原理,这种现象可在过滤器中观察到,如果过滤器中的某个颗粒尺寸大于最小的网眼,则不能通过过滤器。但是,其他的力量会与非常小的微粒(例如,直径 < 2 微米)发生相互作用。12一旦其相互接触,即便非常小的微粒无法穿过滤器的网眼,也会尝试粘附在过滤器材料上。在微粒与过滤器材料的接触过程中,存在四种基本机制:粒径在 0.11 微米范围内的微粒可以通过一个名为“惯性碰撞”的过程,直接影响过滤器网线。粒径在 0.05–1 微米范围内的微粒可以通过一个名为“拦截”的过程,成切线地接触过滤器网线。随着微粒变小,其更多地表现出布朗运动,加之随气流移动 – 并能通过一个名为“扩散”的过程,接触过滤器材料,作为该不稳定运动的结果。最后,带电的小微粒可以通过一个名为“静电相吸”的过程,被带电的滤器材料表面所吸引。图 1 显示了其中的每种现象,图 2 显示了所有这些现象的总和是如何影响过滤器的总体过滤效率的。请注意,对于多数空气过滤器,粒径约为 0.3 微米(即 300 纳米)的微粒是最难捕获的微粒 – 比其更大或更小的微粒更容易捕获。
麻醉呼吸系统中使用的过滤器类型
褶型机械过滤器
褶型机械过滤器包含一层厚的、致密的、随机朝向、结合在一起的疏水纤维片,可以捕获过滤器深处的微粒。将过滤器材料折皱是为了增大滤器的表面积,并减小气流阻力。典型情况下,其具有非常高的过滤效率,同时也可以提供一定程度的湿热交换(当放置在气道附近,放在一个双向气流的地方时)。当用于潮湿环境时,其过滤效率和气流阻力可变好或变差;当环境潮湿时,其效率仍很高。13液体不容易穿过褶型机械过滤器。14机械过滤器的成本通常较高,并具有比静电过滤器更高的内体积。
静电过滤器
静电过滤器包含一层薄的、致密性较低的、编织的静电纤维。对于特定的表面积,其气流阻力较低,因此不能被折褶。静电纤维的过滤效率通常比褶型机械过滤器低 1000 倍。13在潮湿环境中,其过滤效率和气流阻力可变好或变差。液体容易穿过静电过滤器。14
热湿交换过滤器 (HMEF)
热湿交换 (HME) 设备不能通过其自身来提供过滤作用。将含有静电或折皱机械过滤器的 HME 设备称为 HMEF。HME 和 HMEF 仅对加湿有效 – 当放至气道附近的双向气流位置,在这个地方,其可以在呼气过程吸收水分,并在吸气过程释放水分。15
膜过滤器
在呼吸气体分析仪中,使用了一类完全不同的过滤器,以防液体进入分析仪舱室。尽管未将其归类为呼吸系统过滤器,但水分捕获装置中通常包含有疏水性膜过滤器,因为其在干燥时允许气体通过,但在湿润时变堵塞。膜过滤器具有超级小的孔眼和通道,主要通过筛分作用阻止微粒通过。
标准化的检验方法和过滤器的质量标准
微粒过滤作用
有一种简单的国际标准可用于检测呼吸系统过滤器的过滤效率 – ISO 23328-1:用于麻醉和呼吸目的的呼吸系统过滤器。16 该标准描述了一种方法 – 盐检验法,可定量分析在短期挑战过程中、以既定用途中可能遇到的空气流速穿透过滤器的、粒径大小在 0.1 – 0.3 微米之间的气源性氯化钠微粒数量。使用 0.1 mg 或 0.2 mg 的氯化钠微粒、分别以 15 L/min 或 30 L/min 的流速,对儿童和成人用过滤器进行挑战。在对其进行检验之前,在加湿的空气中对过滤器进行预处理,以模拟其临床使用的时段。使用不带静电的盐微粒来进行挑战,因为其非常难以捕获。该方法既不评估对于飞沫和气溶胶的过滤性能,也不检测对于微生物的过滤性能。其仅用于比较目的,且没有经证实的临床相关性。该标准未包含呼吸系统过滤器效率的最低性能阈值。将检验结果表示为百分过滤效率,这是在挑战试验中未穿过过滤器的微粒百分比。例如,如果使用 1 千万个 (107) 微粒对过滤器进行挑战,如果在另一面检出了 1000 个 (103) 微粒,则百分过滤效率为 100 × (1 – 103/ 107) = 99.99%。
其他类型过滤器的测试和评级则使用完全不同的标准。需要注意的是,美国国家职业卫生与安全研究所制定了 NIOSH 42 CFR 第 84 部分: 呼吸防护器械17,作为非电动空气净化呼吸器的检验和评级方法。使用 200 mg 不带静电的干燥氯化钠微粒(粒径在 0.1 – 0.3 微米之间)、以 85 L/min 的流速,对用于医疗照护行业的 N-系列呼吸器进行挑战。18 这是与 ISO 23328-1 相似但挑战性更高的一种检测方法,因为有较高的微粒数量和流速。另一项重要的过滤测试标准是 IEST-RP-CC001:HEPA 和ULPA 过滤器,19 该标准可检验用于洁净空气设备和洁净室的过滤器性能。HEPA 是指可去除 99.97% 微粒(粒径等于 0.3 微米)的高效空气微粒过滤器。由于检验方式不同,将该术语不适用于呼吸系统过滤器。
微生物过滤作用
某些呼吸系统过滤器产品资料包含了有关细菌和/或病毒过滤效率的声明。尚没有标准检验方法可用于确定呼吸系统过滤器的细菌和/或病毒过滤效率,但有标准方法可用于测定其他类型过滤器的这种指标。其中的一种方法是 ASTM F2101–19:使用金黄色酿脓葡萄球菌构成的生物学气溶胶评价医用口罩材料细菌过滤效率 (BFE) 的标准检验方法。20 Wilkes 等人描述了一种相似的方法,可使用枯草芽孢杆菌或 MS-2 大肠杆菌噬菌体构成的生物学气溶胶来检验呼吸系统过滤器,21 该方法与 BS EN 13328-1 征求意见稿中(尚未经过征求意见阶段)的方法相同。在两种方法中,将细菌或病毒悬液气溶胶化,使其成为平均粒径为 3.0 微米的液态微粒,并通过下游一个真空泵进行抽吸,使其通过过滤器材料 。将通过过滤器的任何东西捕获在营养肉汤中或捕获在培养平板上。通过将下游过滤器中培养的微粒数量除以上游挑战中的微粒数量,计算出百分过滤效率。从表面上看,这些方法似乎比盐检验法更具临床相关性。其使用的液态微粒粒径大于盐检验法。液态微粒可能带有静电。仅对活细菌进行计数。但这些方法的再现性较低。通常,相同过滤器对于细菌的百分过滤效率大于病毒、大于盐微粒。
泡点试验
膜过滤器可按孔径(这可以使用泡点试验来间接测定)进行分级。泡点试验是根据一个原理所建立,即液体通过表面张力和毛细管引力而留存在滤器的小孔中,迫使液体离开小孔所需的最小压力与孔径有关。不过,不能将孔径用作微粒或病原体过滤效率的替代指标。通常使用疏水性 0.22 微米膜过滤器来对药物进行除菌过滤、保持硬膜外输液的无菌性,但尚未检验其过滤气源性微粒的效率。已对某些 0.2 微米疏水性膜过滤器(如 GE D-Fend Pro、Dräger WaterLock® 2 和 Covidien FilterLine® 水过滤产品中使用的膜过滤器)进行了独立检验,其对气源性病毒的过滤效率在 99.99% 以上。
临床建议
2003 年,美国疾控中心提出,“有关在呼吸系统或麻醉设备的患者呼吸回路中放置细菌过滤器的问题,无法给出任何建议”,因为他们引用了现在已有 40 年历史的研究,该研究显示,无菌的呼吸回路或呼吸系统过滤器无法减少术后肺炎的发生率。22,当前没有关于将呼吸系统过滤器用于麻醉机的监管法规。不过,在这次 COVID-19 全球大流行期间,应尽可能预防 SARS-CoV-2 患者交叉感染。在 SARS、MERS 和 COVID-19 发生之前,已有关于被污染的麻醉机导致交叉感染的零星报告,但目前尚不清楚这些病原体导致的风险。由于需要采取足够谨慎的态度,以及通过现有知识获取的信息,APSF 和 ASA 建议使用呼吸系统过滤器,承认科学并不完整。(https://www.apsf.org/faq-on-anesthesia-machine-use-protection-and-decontamination-during-the-covid-19-pandemic/)。
添加呼吸系统过滤器并非没有风险。23,24根据放置的位置不同,其可以增加死腔,这会增加重新吸入的二氧化碳量,并减缓吸入诱导和苏醒的速度。其可增加吸入和/或呼出气流的阻力,从而导致自发性呼吸做功增加,并影响肺部力学机制(测试方法请参见国际标准 ISO 9360-1)。25过滤器可逐渐变堵塞,从而导致发生危及生命的通气不足和气压伤。过滤器可增加呼吸回路的重量,并增加意外脱离的连接点数量。
尚不清楚预防呼出的病毒通过呼吸系统感染患者所需的过滤效率。如果患者每小时呼出 200,000 个病毒微粒,则能捕获其中 99.9% 的静电过滤器将仅允许 200 个病毒微粒通过。按顺序放置两个过滤器(例如,一个放置在气道上,一个放置在呼吸管路上)将使过滤效率倍增至 99.9999%,从而使病毒通过风险降低到接近于零,但也会使气流阻力增加两倍。在气道上使用一个较高效率(例如,99.9999%)的折皱式机械呼吸过滤器将捕获相同数量的病毒,并引入较低的气流阻力(与连续放置的两个静电过滤器相比),但可能会增加死腔。
临床医生应当知道提供给他们的呼吸系统过滤器的质量标准。这些质量标准可以在制造商的网站、帮助热线、产品资料、在线或杂志文章中找到。13,14 重要的质量标准是:
- 细菌和病毒过滤效率(% – 越高越好),
- NaCl 或盐过滤效率(% – 越高越好),
- 气流阻力(特定流速(单位 L/min)下的压力降低值(单位 Pa 或 cmH2O) – 越低越好)。
- 过滤器在潮湿环境中预处理对于之前的质量标准有何影响,
- 内体积(ml – 越低越好),以及
- 加湿
- (空气中的失水,单位 mgH2O/L- 越低越好),或
- (空气中的水分输出,单位 mgH2O/L- 越高越好)。
请注意,有些发表文章列出了在 10 或 20 年前进行的评价,产品可能有变化,或是由不同的公司制造或分销。
Robert G. Loeb(医学博士)是弗洛里达大学医学院(弗洛里达州盖恩斯维尔市)的临床麻醉学教授。
他是弗洛里达大学的雇员、美国麻醉医师协会设备和设施委员会主席,同时他也任职于 Masimo, Inc. 公司技术咨询委员会。
参考文献
- Murphy PM, Fitzgeorge RB, Barrett RF. Viability and distribution of bacteria after passage through a circle anaesthetic system. Br J Anaesth. 1991;66:300–304.
- Atkinson MC, Girgis Y, Broome IJ. Extent and practicalities of filter use in anaesthetic breathing circuits and attitudes towards their use: a postal survey of UK hospitals.Anaesthesia. 1999;54:37–41.
- Chant K, Kociuba K, Munro R, et al. Investigation of possible patient-to-patient transmission of hepatitis C in a hospital. New South Wales Public Health Bulletin. 1994;5:47–51.
- Spertini V, Borsoi L, Berger J, et al. Bacterial contamination of anesthesia machines’ internal breathing-circuit-systems. GMS Hyg Infect Control. 2011;6(1).
- Lloyd G, Howells J, Liddle C, et al. Barriers to hepatitis C transmission within breathing systems: efficacy of a pleated hydrophobic filter. Anaesth Intensive Care. 1997;25:235–238.
- Heinsen A, Bendtsen F, Fomsgaard A. A phylogenetic analysis elucidating a case of patient-to-patient transmission of hepatitis C virus during surgery. J Hosp Infect. 2000;46:309–313.
- Australian & New Zealand College of Anaesthetists.PS28 Guideline on infection control in anaesthesia 2015.Available at: https://www.anzca.edu.au/safety-advocacy/standards-of-practice/policies,-statements,-and-guidelines Accessed July 6, 2020.
- Association of Anaesthetists of Great Britain & Ireland. Guidelines: infection prevention and control 2020. https://anaesthetists.org/Portals/0/PDFs/Guidelines%20PDFs/Infection_Control_Guideline_FINAL%202020.pdf?ver=2020-01-20-105932-143 Accessed July 6, 2020.
- Tellier R, Li Y, Cowling BJ, Tang JW. Recognition of aerosol transmission of infectious agents: a commentary. BMC Infect Dis. 2019;19:101.
- Leung NH, Chu DK, Shiu EY, et al. Respiratory virus shedding in exhaled breath and efficacy of face masks. Nat Med. 2020;26:676–680.
- Nicas M, Hubbard AE, Jones RM, Reingold AL. The infectious dose of variola (smallpox) virus. Appl Biosaf. 2004;9:118–127.
- Hakobyan NA. Introduction to basics of submicron aerosol particles filtration theory via ultrafine fiber media. Armen J Phys. 2015;8:140–151.
- Wilkes A. Breathing system filters: an assessment of 104 breathing system filters. MHRA Evaluation 04005. March 2004 https://www.psnetwork.org/wp-content/uploads/2018/01/An-assessment-of-104-breathing-system-filters-MHRA-Evaluation-04005-2004-.pdf Accessed July 6, 2020.
- Wilkes AR. The ability of breathing system filters to prevent liquid contamination of breathing systems: a laboratory study* APPARATUS. Anaesthesia. 2002;57:33–39.
- Wilkes AR. Heat and moisture exchangers and breathing system filters: their use in anaesthesia and intensive care. Part 1–history, principles and efficiency. Anaesthesia. 2011;66:31–9.
- International Organization for Standardization. Breathing system filters for anaesthetic and respiratory use — Part 1:Salt test method to assess filtration performance. (ISO 23328-1:2003) https://www.iso.org/standard/35330.html Accessed July 6, 2020.
- Department of Health and Human Services. 42 CFR Part 84 Respiratory protective devices; final rules and notice. Federal Register Volume 60, Number 110 (Thursday, June 8, 1995). https://www.govinfo.gov/content/pkg/FR-1995-06-08/html/95-13287.htm Accessed July 6, 2020.
- National Institute for Occupational Safety and Health. Determination of particulate filter efficiency level for N95 series filters against solid particulates for non-powered, air-purifying respirators standard testing procedure (STP). https://www.cdc.gov/niosh/npptl/stps/pdfs/TEB-APR-STP-0059-508.pdf Accessed July 6, 2020.
- Institute for Environmental Sciences and Technology.HEPA and ULPA Filters. (IEST-RP-CC001) https://www.iest.org/Standards-RPs/Recommended-Practices/IEST-RP-CC001 Accessed July 6, 2020.
- ASTM International.Standard test method for evaluating the bacterial filtration efficiency (BFE) of medical face mask materials, using a biological aerosol of Staphylococcus aureus. (F2101 – 19) https://compass.astm.org/EDIT/html_annot.cgi?F2101+19 Accessed July 6, 2020.
- Wilkes AR, Benbough JE, Speight SE, et al. The bacterial and viral filtration performance of breathing system filters.Anaesthesia. 2000;55:458–465.
- CDC Healthcare Infection Control Practices Advisory Committee. Guidelines for preventing health-care–associated pneumonia, 2003. MMWR 53(RR03); 1–36, 2004.
- Lawes EG. Hidden hazards and dangers associated with the use of HME/filters in breathing circuits. Their effect on toxic metabolite production, pulse oximetry and airway resistance. Br J Anaesth. 2003;91:249–264.
- Wilkes AR. Heat and moisture exchangers and breathing system filters: their use in anaesthesia and intensive care. Part 2–practical use, including problems, and their use with paediatric patients. Anaesthesia. 2011;66:40–51.
- International Standards Organization. Anaesthetic and respiratory equipment—heat and moisture exchangers (HMEs) for humidifying respired gases in humans—part 1: HMEs for use with tracheostomized patients having minimal tidal volume of 250 ml (ISO 9360-2: 2001).
本专栏内提供的信息仅可用于与安全相关教育,不作为医学或法律建议。个人或团体针对提问给出的回复仅作为评论信息,仅可用于教育或讨论目的,不得作为 APSF 的声明、建议或意见。APSF 并非旨在针对问题答复提供任何具体意见或建议,或提供具体的医学或法律建议。在任何情况下,APSF 均不对因任何人依赖任何此类信息造成或声称造成的任何损害或损失承担任何直接或间接责任。