| Este artigo foi publicado anteriormente no portal on-line da APSF. A presente versão foi atualizada e modificada pelo autor para este Boletim da APSF. |
Caros editores da “Resposta rápida”:
A crise global devido à COVID-19 permeou todos os aspectos de nossos sistemas de saúde. As preocupações com o risco biológico do SARS-CoV-2 e a disseminação e transmissão por contato para pacientes, profissionais de saúde, ambiente e equipamentos têm sido generalizadas, especialmente no que diz respeito aos procedimentos que geram aerossóis.1-3 A transmissão do vírus é principalmente de natureza respiratória. O vírion SARS-CoV-2 tem aproximadamente 120 nanômetros de diâmetro (0,06-0,14 μm) e passa de pessoa para pessoa em partículas de portadores biológicos, como gotículas ou aerossóis.2,3 Recomendações sobre níveis adequados de EPI, lavagem das mãos, limpeza de superfícies, descontaminação e precauções durante os procedimentos de manejo das vias aéreas foram amplamente discutidas durante a pandemia.4-6 Como com outras doenças respiratórias transmissíveis, contamos com dois sistemas de filtragem importantes: filtros de circuito quando sistemas de ventilação artificial são usados na sala de cirurgia e/ou unidades de terapia intensiva (UTI) e respiradores de máscara facial.
Contudo, as coisas são um pouco mais complicadas:
- Máquinas de anestesia e ventiladores mecânicos requerem filtros para purificação da qualidade do ar e prevenção de contaminação cruzada. O padrão de eficiência desses filtros é denominado HEPA, uma referência à capacidade de absorção de partículas de alta eficiência/ar particulado de alta eficiência.7 A ASA recomenda a colocação de filtros HEPA entre a peça em Y do circuito respiratório e a máscara, tubo endotraqueal ou máscara laríngea do paciente.8
- Os padrões europeus e americanos para determinar a eficiência do filtro não são os mesmos: Padrões europeus usam 99,95% de remoção de partículas com diâmetro de 0,3 μm, já os EUA usam 99,97%.9
- A eficiência da máscara facial é determinada pelo nível de penetração das partículas. Uma máscara N95, por exemplo, remove pelo menos 95% das partículas de 300 nm usando uma taxa de fluxo de ar de 85 litros/min.10 Os respiradores de máscara facial são regulamentados de acordo com o National Institute for Occupational Safety and Health (NIOSH) dos EUA e padrões e testes reconhecidos internacionalmente.
- Filtros em circuitos respiratórios e máquinas de anestesia não são regulamentados. Não há nenhum teste padrão nacional ou internacional para filtros em circuitos respiratórios. Como não há um teste padrão, será que todos os fabricantes relatam o mesmo ao discutir o nível de eficiência?11
- Os filtros disponíveis atualmente são adequados para COVID-19?
- Como muitos pacientes com COVID-19 requerem ventilação mecânica prolongada, com que frequência esses filtros devem ser trocados na UTI?
- O que os profissionais de saúde devem fazer em caso de falta de filtros?
Essas são algumas das perguntas urgentes em relação aos filtros HEPA que gostaria de ver discutidas.
Obrigado.
Felipe Urdaneta
Professor de anestesiologia
University of Florida/NFSGVHS
Gainesville, Florida, EUA
O autor é consultor da Medtronic e integrante do Conselho Consultivo da Vyaire e recebeu honorários de palestrante em seu nome.
Referências
- Canova V, Lederer Schlpfer H, Piso RJ, et al. Transmission risk of SARS-CoV-2 to healthcare workers—observational results of a primary care hospital contact tracing. Swiss Medical Weekly. 2020;150:1–5.
- Asadi S, Bouvier N, Wexler AS, et al. The coronavirus pandemic and aerosols: Does COVID-19 transmit via expiratory particles? Aerosol Sci Technol. 2020;0:1–4.
- van Doremalen N, Bushmaker T, Morris DH, et al. Aerosol and surface stability of SARS-CoV-2 as compared with SARS-CoV-1. N Engl J Med. 2020;382:1564–1567.
- Asenjo JF. Safer intubation and extubation of patients with COVID-19. Can J Anaesth. 2020:1–3.
- Chia SE, Koh D, Fones C, et al. Appropriate use of personal protective equipment among healthcare workers in public sector hospitals and primary healthcare polyclinics during the SARS outbreak in Singapore. Occup Environ Med. 2005;62:473–477.
- Sorbello M, El-Boghdadly K, Di Giacinto I, et al. The Italian coronavirus disease 2019 outbreak: recommendations from clinical practice. Anaesthesia. 2020;75:724–732.
- First MW. Hepa filters. Appl Biosaf. 1998;3:33–42.
- American Society of Anesthesiologists. Information for health care professionals. Published 2020. https://www.asahq.org/about-asa/governance-and-committees/asa-committees/committee-on-occupational-health/coronavirus. Accessed June, 2020.
- Wikipedia. HEPA. https://en.wikipedia.org/wiki/HEPA. Accessed June 9, 2020.
- Haghighat F, Bahloul A, Lara J, et al. Development of a procedure to measure the effectiveness of N95 respirator filters against nanoparticles. 2012.
- NIOSH-Approved Particulate Filtering Facepiece Respirators. https://www.cdc.gov/niosh/npptl/topics/respirators/disp_part/default.html. Accessed June 9, 2020.
Resposta:
Agradecemos a Felipe Urdaneta, MD, por destacar uma certa confusão sobre o uso de filtros de sistema de respiração de anestesia em resposta à pandemia da COVID-19. O site da APSF tem uma página (https://www.apsf.org/faq-on-anesthesia-machine-use-protection-and-decontamination-during-the-covid-19-pandemic/) que resume as estratégias atuais para proteger a máquina de anestesia contra contaminação por um paciente possivelmente infectado. Porém, ela não oferece alguns dos detalhes por trás das recomendações. Este artigo fornece detalhes, como o risco de trans-infecção do paciente por meio do sistema de respiração, modos de transmissão do vírus, a física da filtração, tipos de filtros e testes padronizados e especificações de filtros, em um esforço para responder às perguntas de Felipe Urdaneta e esclarecer confusões semelhantes entre nossos leitores.
Risco de infecção cruzada de pacientes por meio do sistema de respiração
Os sistemas de respiração circulares apresentam um risco hipotético de infecção cruzada do paciente devido à reinalação de gases previamente exalados. Antes da década de 1990, não era comum usar filtros no sistema de respiração de anestesia e acreditava-se que a infecção cruzada dos pacientes era evitada pela passagem do gás exalado por um absorvente alcalino de dióxido de carbono.1 No entanto, tais filtros passaram a ser cada vez mais usados na década de 19902 após um relato de nove casos de infecção cruzada por hepatite C atribuídos a sistemas de respiração de anestesia contaminados.3 Há evidências conflitantes para o potencial de infecção cruzada: quase nenhum caso foi documentado, mas testes in-vitro demonstram essa possibilidade.4-6 Em todo caso, o uso de filtros no sistema de respiração é recomendado por várias sociedades de anestesia, mas apenas quando os circuitos respiratórios são reutilizados entre os pacientes.7,8
Modos de transmissão de vírus respiratórios
A COVID-19 (SARS-CoV-2) é transmitida principalmente pela via respiratória, assim como a Síndrome Respiratória Aguda Grave (SARS-CoV), o coronavírus associado à Síndrome Respiratória do Oriente Médio (MERS-CoV) e outros coronavírus. É transmitida por gotículas, que têm mais de 20 mícrons de diâmetro, e por aerossóis, que têm menos de 5-10 mícrons de diâmetro.9 As gotículas tendem a cair devido à gravidade, enquanto as partículas de aerossol flutuam no ar e seguem as correntes de ar. Partículas de tamanho intermediário compartilham algumas das propriedades das gotículas e dos aerossóis. A rápida evaporação de pequenas gotículas resulta em núcleos de gotículas ainda menores que também seguem correntes de ar. Gotículas, aerossóis e partículas de tamanho intermediário são gerados durante a tosse, espirros e a fala, enquanto os aerossóis são gerados principalmente durante a respiração passiva. Um conceito importante na filtragem de patógenos é que os vírus respiratórios não são transmitidos por partículas virais isoladas flutuando no ar, mas por vírus contidos em partículas maiores. Gotículas e algumas partículas de tamanho intermediário podem se depositar nas superfícies, levando à transmissão superficial.
Nenhum estudo estimou quantas partículas de vírus os pacientes infectados com SARS-CoV-2 exalam. No entanto, um estudo que quantificou a exalação de outras partículas de vírus respiratórios, descobriu que os pacientes infectados com coronavírus sazonal exalaram e tossiram de 0 a 200.000 partículas de vírus por hora.10
Embora uma única partícula viral possa teoricamente resultar em infecção sistêmica, a chance de infecção aumenta com a duração e magnitude da exposição viral.11
Física da filtração
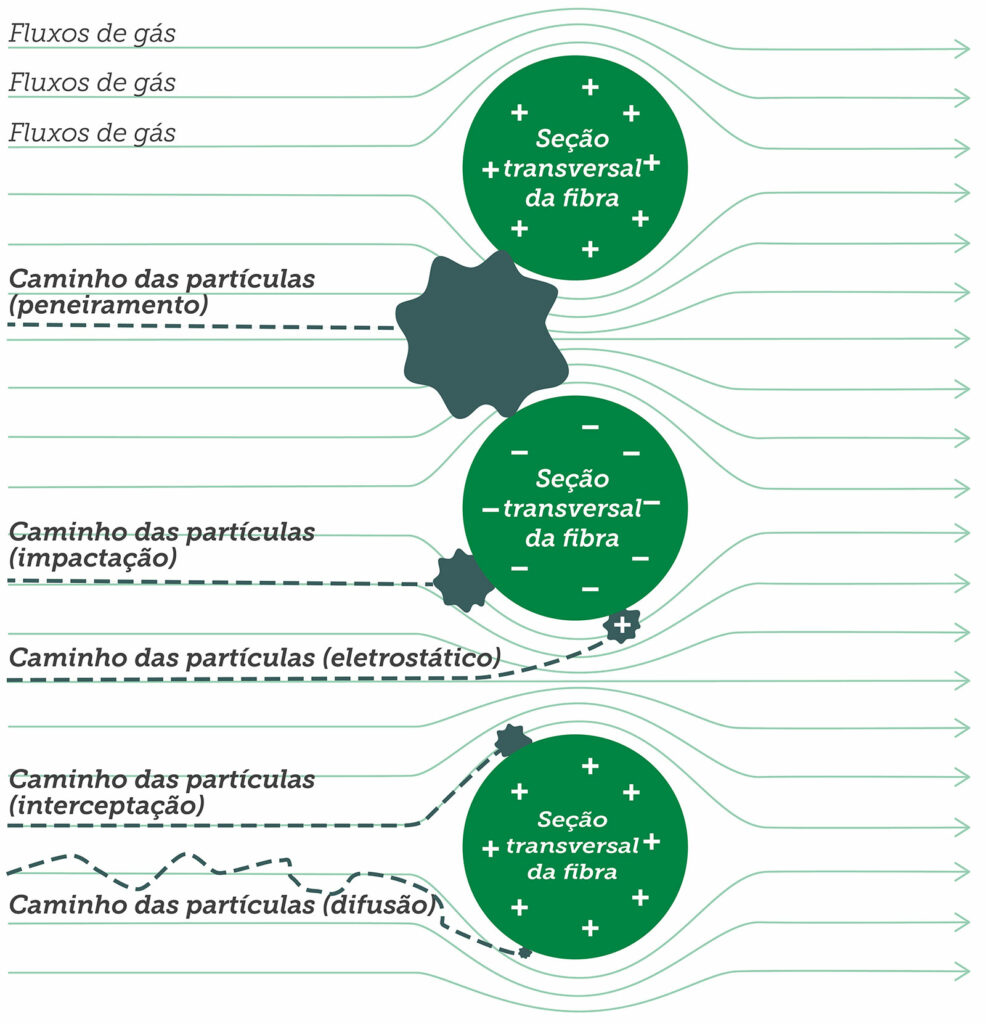
As pessoas geralmente entendem a física da filtração por peneira, um fenômeno observável em filtros, por meio do qual uma partícula maior do que os menores orifícios não pode passar pelo filtro. No entanto, outras forças entram em ação quando se trata de partículas muito pequenas (por exemplo, diâmetro <2 mícrons).12 Partículas muito pequenas tendem a aderir ao material do filtro assim que entram em contato com ele, mesmo que possam passar pelas aberturas. Existem quatro mecanismos básicos pelos quais as partículas entram em contato com o material do filtro. Partículas na faixa de 0,11 mícron podem impactar diretamente as fibras do filtro por meio de um processo denominado impactação inercial. Partículas na faixa de 0,05–1 mícron podem entrar em contato tangencial com as fibras do filtro por meio de um processo denominado interceptação. À medida que ficam menores, as partículas exibem cada vez mais movimento browniano, além de se moverem com o fluxo de ar, e podem entrar em contato com o material do filtro como consequência desse movimento errático por meio de um processo chamado difusão. Por fim, pequenas partículas carregadas podem ser atraídas para a superfície carregada do material do filtro por meio de um processo chamado atração eletrostática. A Figura 1 ilustra cada um desses fenômenos e a Figura 2 mostra como a soma desses fenômenos afeta a eficiência geral do filtro. Observe que, para a maioria dos filtros de ar, partículas em torno de 0,3 mícrons (ou seja, 300 nanômetros) em tamanho são as mais difíceis de capturar – partículas maiores ou menores são mais fáceis de capturar.
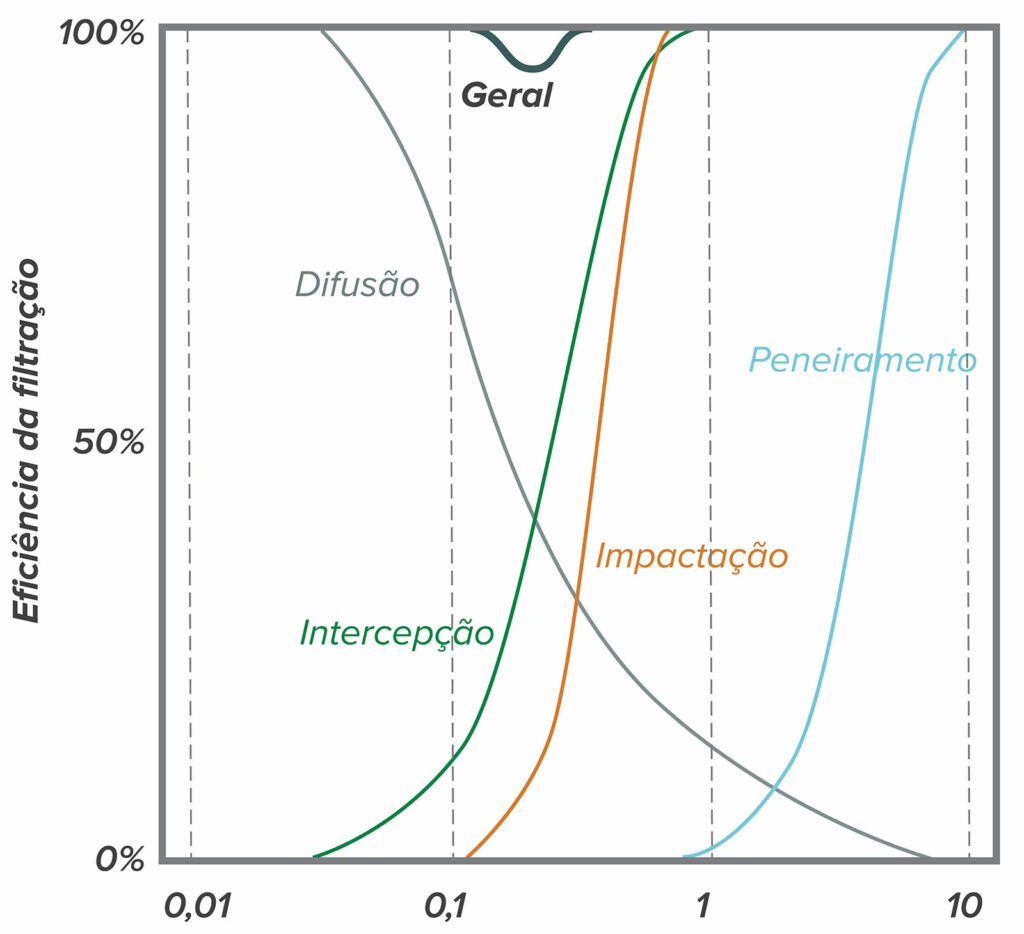
Figura 2: Os fenômenos de filtração individual somam-se para produzir a filtração geral para partículas de tamanhos diferentes. Observe que a eficiência mais baixa é de cerca de 0,3 mícrons.
Tipos de filtros usados em sistemas de respiração de anestesia
Filtros mecânicos plissados
Os filtros mecânicos plissados contêm uma folha espessa de fibras hidrofóbicas ligadas, bem compactadas e orientadas aleatoriamente que capturam partículas na profundidade do filtro. O material do filtro é plissado para aumentar a área de superfície e diminuir a resistência ao fluxo de ar. Eles normalmente têm uma eficiência de filtração muito alta e também podem fornecer alguma troca de calor e umidade quando colocados perto das vias aéreas, em um local de fluxo de ar bidirecional. Quando usados em um ambiente úmido, sua eficiência de filtração e resistência ao fluxo de ar podem melhorar ou piorar; eles ainda tendem a ser altamente eficazes quando úmidos.13 Os líquidos não passam facilmente pelos filtros mecânicos plissados.14 Os filtros mecânicos tendem a custar mais e ter um volume interno maior do que os filtros eletrostáticos.
Filtros eletrostáticos
Os filtros eletrostáticos contêm uma folha fina de fibras eletrostáticas entrelaçadas de maneira menos rígida. Sua resistência ao fluxo de ar é menor para uma determinada área de superfície, portanto, eles não são plissados. Os filtros eletrostáticos normalmente têm eficiências de filtração 1.000 vezes menores do que os filtros mecânicos plissados.13 A eficiência de filtração e a resistência ao fluxo de ar podem melhorar ou piorar em um ambiente úmido. Os líquidos passam facilmente por um filtro eletrostático.14
Filtros trocadores de calor e umidade (HMEF)
Por si só, os dispositivos trocadores de calor e umidade (HME) não fornecem filtragem. Os HMEs que contêm um filtro eletrostático ou mecânico plissado são denominados HMEF. HMEs e HMEFs só são eficazes para umidificação quando colocados próximos às vias aéreas, em um local de fluxo de ar bidirecional, onde absorvem água durante a expiração e a liberam durante a inspiração.15
Filtros de membrana
Um tipo completamente diferente de filtro é usado em analisadores de gases respiratórios para evitar a entrada de fluido na câmara do analisador. Embora não sejam classificados como filtros de sistema de respiração, os filtros de membrana hidrofóbica são comumente incluídos em coletores de água porque permitem que o gás passe quando seco, mas se tornam oclusivos quando úmidos. Os filtros de membrana têm poros e canais ultrapequenos que podem impedir a passagem de partículas principalmente por peneiramento.
Testes padronizados e especificações de filtros
Filtração de partículas
Existe uma única norma internacional para testar a eficiência de filtração dos filtros de sistemas de respiração, a ISO 23328-1: Filtros para sistemas respiratórios utilizados em anestesia e cuidados respiratórios.16 A norma descreve um método, o método de ensaio salino, que quantifica o número de partículas de cloreto de sódio de 0,1 a 0,3 mícron no ar que passam pelo filtro durante um desafio de curto prazo em taxas de fluxo de ar prováveis de serem encontradas durante o uso pretendido. Filtros pediátricos e adultos são desafiados com 0,1 mg ou 0,2 mg de partículas de cloreto de sódio a 15 L/min ou 30 L/min, respectivamente. Os filtros são pré-condicionados em ar umidificado para simular um período de uso clínico antes de serem testados. Partículas de sal seco não eletrostaticamente carregadas são usadas para o desafio, porque são muito difíceis de capturar. O método não avalia o desempenho de filtração para gotículas e aerossóis, nem se propõe a testar o desempenho de filtração para microrganismos. Serve apenas para fins de comparação e não tem relevância clínica comprovada. A norma não contém um limite para desempenho mínimo da eficiência do filtro do sistema de respiração. Os resultados do teste são expressos como o percentual de eficiência de filtração, que é o percentual de partículas no desafio que não passam pelo filtro. Por exemplo, se o filtro for desafiado com 10 milhões (107) de partículas e 1.000 (103) partículas forem detectadas no outro lado, então a eficiência de filtração percentual será 100 * (1-103/ 107) = 99,99%.
Padrões totalmente diferentes são usados para testar e classificar outros tipos de filtros. Notavelmente, o National Institute for Occupational Health and Safety desenvolveu o NIOSH 42 CFR Seção 84: Dispositivos de proteção respiratória17 como um método para testar e avaliar respiradores purificadores de ar não alimentados. Os respiradores da série N usados na área de saúde são desafiados com 200 mg de partículas secas de cloreto de sódio não eletrostaticamente carregadas com 0,1 a 0,3 mícron de tamanho a uma taxa de fluxo de 85 L/min.18 Este é um teste semelhante, mas mais desafiador do que o ISO 23328-1 devido à maior massa de partículas e taxa de fluxo. Outra norma de teste de filtração notável é a IEST-RP-CC001: filtros HEPA e ULPA,19 que testa o desempenho de filtros usados em dispositivos de ar limpo e salas limpas. A abreviação HEPA é usada para designar filtros de alta eficiência para partículas de ar que removem 99,97% das partículas cujo diâmetro é igual a 0,3 mícron. No entanto, não é apropriado aplicar esse termo aos filtros de sistema de respiração porque os métodos de teste são diferentes.
Filtração de microrganismos
Algumas publicações sobre produtos de filtro de sistemas de respiração contêm declarações sobre a eficiência da filtração bacteriana e/ou viral. Não existe um teste padrão para determinar a eficiência de filtração bacteriana e/ou viral dos filtros de sistemas de respiração, mas existem métodos padrões para determinar isso para outros tipos de filtros. Um deles é o ASTM F2101–19: método de teste padrão para avaliar a eficiência de filtração bacteriana (BFE) de materiais de máscara facial médica usando um aerossol biológico de Staphylococcus aureus.20 Um procedimento semelhante usando aerossóis biológicos de Bacillus subtilis ou colifago MS-2 para testar os filtros de sistemas de respiração é descrito por Wilkes et al.21 e é o mesmo que no Projeto BS EN 13328-1 (que nunca passou da fase de projeto). Nos dois procedimentos, suspensões de bactérias ou vírus são aerossolizadas até um tamanho médio de partícula de líquido de 3,0 mícrons e puxadas através do material de filtro por um vácuo a jusante. Qualquer coisa que passa pelo filtro é capturada em caldo de nutrientes ou em placas de cultura. A eficiência de filtração percentual é calculada dividindo o número de partículas cultivadas a jusante do filtro pelo número no desafio a montante. À primeira vista, esses métodos podem parecer mais clinicamente relevantes do que o método de ensaio salino. Eles usam partículas de fluido de tamanho maior do que o método de ensaio salino. As partículas de fluido podem ser eletrostaticamente carregadas. Apenas microrganismos viáveis são contados. No entanto, esses métodos são menos reproduzíveis. Em geral, o mesmo filtro terá maior eficiência de filtragem percentual para bactérias, em seguida para vírus e, em seguida, para partículas de sal.
Teste de ponto de bolha
Os filtros de membrana são avaliados pelo tamanho dos poros, que é indiretamente determinado usando o teste de ponto de bolha. O teste do ponto de bolha é baseado no princípio de que o líquido é retido nos poros do filtro pela tensão superficial e forças capilares, e que a pressão mínima necessária para forçar o líquido para fora dos poros está relacionada ao diâmetro dos poros. No entanto, o tamanho do poro não pode ser usado como substituto para a eficiência de filtração de partículas ou patógenos. Filtros de membrana hidrofílicos de 0,22 mícron são comumente usados para esterilizar produtos farmacêuticos e para manter a esterilidade de infusões epidurais, mas sua eficiência na filtragem de partículas transportadas pelo ar não foi testada. Alguns filtros de membrana hidrofóbicos de 0,2 mícron (como aqueles nos coletores de água GE D-Fend Pro, Dräger WaterLock® 2 e Covidien FilterLine®) foram testados de forma independente e têm uma eficiência de filtração viral aerotransportada de 99,99% ou superior.
Recomendações clínicas
Em 2003, o Centro de Controle de Doenças dos Estados Unidos declarou: “nenhuma recomendação pode ser feita para a colocação de um filtro bacteriano no sistema de respiração ou circuito do paciente do equipamento de anestesia”, citando agora estudos de 40 anos que mostraram falha de circuitos respiratórios estéreis ou filtros de sistemas de respiração para reduzir a incidência de pneumonia pós-operatória.22 Não há regulamentação atual para o uso de filtros de sistemas de respiração em máquinas de anestesia. No entanto, parece prudente prevenir, da melhor forma possível, a infecção cruzada de pacientes com SARS-CoV-2 durante a pandemia da COVID-19. Existem relatos esparsos de infecção cruzada de máquinas de anestesia contaminadas antes da SARS, MERS e COVID-19, mas o risco desses patógenos não é conhecido atualmente. Por excesso de cautela e informados pelo conhecimento existente, a APSF e a ASA recomendam o uso de filtros de sistemas de respiração, reconhecendo que a ciência é incompleta (https://www.apsf.org/faq-on-anesthesia-machine-use-protection-and-decontamination-during-the-covid-19-pandemic/).
Usar filtros em sistemas de respiração não é um procedimento isento de riscos.23,24 Dependendo da colocação, eles podem adicionar espaço morto, o que aumenta a reinalação de dióxido de carbono e retarda a indução e a emergência da inalação. Eles aumentam a resistência ao fluxo inspiratório e/ou expiratório, o que aumenta o trabalho respiratório espontâneo e afeta a mecânica pulmonar (os métodos de teste são descritos na norma internacional ISO 9360-1).25 Os filtros podem ficar obstruídos, levando à hipoventilação e barotrauma com risco de vida Eles adicionam peso ao circuito respiratório e adicionam locais para desconexão acidental.
A eficiência de filtração necessária para prevenir a infecção de vírus exalados pelo sistema de respiração não é conhecida. Se um paciente exalar 200.000 partículas de vírus por hora, um filtro eletrostático que captura 99,9% delas só permitirá que 200 passem. Colocar dois desses filtros em série (por exemplo, um nas vias aéreas e um no ramo expiratório) multiplicará a eficiência de filtração para 99,9999%, tornando o risco de passagem do vírus quase nulo, mas dobrará a resistência ao fluxo. O uso de um único filtro de sistema de ventilação mecânico plissado de maior eficiência (por exemplo, 99,9999%) nas vias aéreas capturará o mesmo número de vírus e introduzirá menos resistência das vias aéreas do que dois filtros eletrostáticos em série, mas pode aumentar o espaço morto.
Os médicos devem conhecer as especificações dos filtros do sistema de respiração disponíveis. Eles podem ser encontrados no site do fabricante ou na linha de ajuda, nas publicações do produto, on-line e em artigos de periódicos.13,14 As especificações importantes são:
- eficiência de filtração bacteriana e viral (% – quanto mais alta, melhor),
- eficiência de filtração de NaCl ou sal (% – quanto mais alta, melhor),
- resistência ao fluxo (queda de pressão em Pa ou cmH2O a uma determinada taxa de fluxo de ar em L/min – quanto mais baixa, melhor),
- como as especificações anteriores são afetadas pelo condicionamento do filtro na umidade,
- volume interno (ml – quanto mais baixa, melhor) e
- umidificação
- (perda de umidade em mgH2O/L de ar – quanto mais baixa, melhor) ou
- (saída de umidade em mgH2O/L de ar – quanto mais alta, melhor).
Observe que algumas publicações listam avaliações que foram feitas há 10 ou 20 anos e que os produtos podem mudar ou ser fabricados ou distribuídos por empresas diferentes.
Robert G. Loeb, MD, é professor de anestesiologia na Faculdade de Medicina da University of Florida, Gainesville, FL, EUA.
Ele é funcionário da University of Florida, presidente do Comitê de Equipamentos e Instalações da American Society of Anesthesiologists e faz parte do Conselho Consultivo Técnico da Masimo, Inc.
Referências
- Murphy PM, Fitzgeorge RB, Barrett RF. Viability and distribution of bacteria after passage through a circle anaesthetic system. Br J Anaesth. 1991;66:300–304.
- Atkinson MC, Girgis Y, Broome IJ. Extent and practicalities of filter use in anaesthetic breathing circuits and attitudes towards their use: a postal survey of UK hospitals. Anaesthesia. 1999;54:37–41.
- Chant K, Kociuba K, Munro R, et al. Investigation of possible patient-to-patient transmission of hepatitis C in a hospital. New South Wales Public Health Bulletin. 1994;5:47–51.
- Spertini V, Borsoi L, Berger J, et al. Bacterial contamination of anesthesia machines’ internal breathing-circuit-systems. GMS Hyg Infect Control. 2011;6(1).
- Lloyd G, Howells J, Liddle C, et al. Barriers to hepatitis C transmission within breathing systems: efficacy of a pleated hydrophobic filter. Anaesth Intensive Care. 1997;25:235–238.
- Heinsen A, Bendtsen F, Fomsgaard A. A phylogenetic analysis elucidating a case of patient-to-patient transmission of hepatitis C virus during surgery. J Hosp Infect. 2000;46: 309–313.
- Australian & New Zealand College of Anaesthetists. PS28 Guideline on infection control in anaesthesia 2015. Available at: https://www.anzca.edu.au/safety-advocacy/standards-of-practice/policies,-statements,-and-guidelines Accessed July 6, 2020.
- Association of Anaesthetists of Great Britain & Ireland. Guidelines: infection prevention and control 2020. https://anaesthetists.org/Portals/0/PDFs/Guidelines%20PDFs/Infection_Control_Guideline_FINAL%202020.pdf?ver=2020-01-20-105932-143 Accessed July 6, 2020.
- Tellier R, Li Y, Cowling BJ, Tang JW. Recognition of aerosol transmission of infectious agents: a commentary. BMC Infect Dis. 2019;19:101.
- Leung NH, Chu DK, Shiu EY, et al. Respiratory virus shedding in exhaled breath and efficacy of face masks. Nat Med. 2020;26:676–680.
- Nicas M, Hubbard AE, Jones RM, Reingold AL. The infectious dose of variola (smallpox) virus. Appl Biosaf. 2004;9:118–127.
- Hakobyan NA. Introduction to basics of submicron aerosol particles filtration theory via ultrafine fiber media. Armen J Phys. 2015;8:140–151.
- Wilkes A. Breathing system filters: an assessment of 104 breathing system filters. MHRA Evaluation 04005. March 2004 https://www.psnetwork.org/wp-content/uploads/2018/01/An-assessment-of-104-breathing-system-filters-MHRA-Evaluation-04005-2004-.pdf Accessed July 6, 2020.
- Wilkes AR. The ability of breathing system filters to prevent liquid contamination of breathing systems: a laboratory study* APPARATUS. Anaesthesia. 2002;57:33–39.
- Wilkes AR. Heat and moisture exchangers and breathing system filters: their use in anaesthesia and intensive care. Part 1–history, principles and efficiency. Anaesthesia. 2011;66:31–9.
- International Organization for Standardization. Breathing system filters for anaesthetic and respiratory use — Part 1: Salt test method to assess filtration performance. (ISO 23328-1:2003) https://www.iso.org/standard/35330.html Accessed July 6, 2020.
- Department of Health and Human Services. 42 CFR Part 84 Respiratory protective devices; final rules and notice. Federal Register Volume 60, Number 110 (Thursday, June 8, 1995). https://www.govinfo.gov/content/pkg/FR-1995-06-08/html/95-13287.htm Accessed July 6, 2020.
- National Institute for Occupational Safety and Health. Determination of particulate filter efficiency level for N95 series filters against solid particulates for non-powered, air-purifying respirators standard testing procedure (STP). https://www.cdc.gov/niosh/npptl/stps/pdfs/TEB-APR-STP-0059-508.pdf Accessed July 6, 2020.
- Institute for Environmental Sciences and Technology. HEPA and ULPA Filters. (IEST-RP-CC001) https://www.iest.org/Standards-RPs/Recommended-Practices/IEST-RP-CC001 Accessed July 6, 2020.
- ASTM International. Standard test method for evaluating the bacterial filtration efficiency (BFE) of medical face mask materials, using a biological aerosol of Staphylococcus aureus. (F2101 – 19) https://compass.astm.org/EDIT/html_annot.cgi?F2101+19 Accessed July 6, 2020.
- Wilkes AR, Benbough JE, Speight SE, et al. The bacterial and viral filtration performance of breathing system filters. Anaesthesia. 2000;55:458–465.
- CDC Healthcare Infection Control Practices Advisory Committee. Guidelines for preventing health-care–associated pneumonia, 2003. MMWR 53(RR03); 1–36, 2004.
- Lawes EG. Hidden hazards and dangers associated with the use of HME/filters in breathing circuits. Their effect on toxic metabolite production, pulse oximetry and airway resistance. Br J Anaesth. 2003;91:249–264.
- Wilkes AR. Heat and moisture exchangers and breathing system filters: their use in anaesthesia and intensive care. Part 2–practical use, including problems, and their use with paediatric patients. Anaesthesia. 2011;66:40–51.
- International Standards Organization. Anaesthetic and respiratory equipment—heat and moisture exchangers (HMEs) for humidifying respired gases in humans—part 1: HMEs for use with tracheostomized patients having minimal tidal volume of 250 ml (ISO 9360-2: 2001).
As informações fornecidas são somente para fins educacionais relacionados à segurança e não constituem aconselhamento médico ou legal. Respostas individuais ou de grupo são somente comentários, fornecidos para fins de conhecimento ou para debate, e não constituem declarações nem opiniões da APSF. Não é intenção da APSF fornecer aconselhamento médico ou legal específico ou apoiar quaisquer pontos de vista ou recomendações em resposta às questões propostas. Em hipótese alguma a APSF será responsável, direta ou indiretamente, por qualquer dano ou perda causados por ou supostamente causados por ou em conexão com a confiança nas informações mencionadas.