| 编者按:本社评点评了全世界读者浏览次数最多的一篇根据我们在前新冠肺炎时代的分析数据的 APSF 文章。 |
总结
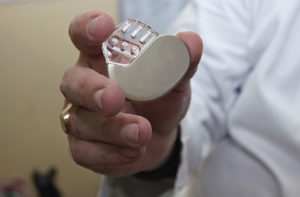 心血管植入式电子器械 (CIED) 是针对起搏器、植入型心律转复除颤器 (ICD) 以及心脏再同步治疗 (CRT) 器械的一个通用术语。来自 2013“围术期照护期间的 CIED 管理”的 APSF 文章旨在为麻醉专业人员提供关于围手术期内管理 CIED 患者的总体框架。1基于 APSF 文章发表的 2011 心脏节律协会 (HRS)/美国麻醉医师协会 (ASA) 共识声明2 是明确许多 CIED 围术期照护是非问题的关键范本。这些问题总结如下:
心血管植入式电子器械 (CIED) 是针对起搏器、植入型心律转复除颤器 (ICD) 以及心脏再同步治疗 (CRT) 器械的一个通用术语。来自 2013“围术期照护期间的 CIED 管理”的 APSF 文章旨在为麻醉专业人员提供关于围手术期内管理 CIED 患者的总体框架。1基于 APSF 文章发表的 2011 心脏节律协会 (HRS)/美国麻醉医师协会 (ASA) 共识声明2 是明确许多 CIED 围术期照护是非问题的关键范本。这些问题总结如下:
从围术期的观点看,许多 CIED 患者在手术前并不需要进行新的评估。带有起搏器的患者需要每年评估一次,带有 ICD 或 CRT 器械的患者需要每 6 个月复查一次。2 CIED 的围术期评价主要关注麻醉医师、手术医生以及 CIED 团队(心脏病医师、执业护士和/或制造商代表)之间的沟通。所有团队成员均有必要了解所需的患者和手术因素,以便为每名患者制定个性化的治疗方法。针对麻醉专业人员的关键信息包括上一次复查的日期、器械类型、器械放置的适应症、电池寿命、当前的设置、起搏器依赖性以及磁力反应(请参见来自原文的表 1 – https://www.apsf.org/article/managing-cardiovascular-implantable-electronic-devices-cieds-during-perioperative-care/)。1
CIED 计划必须包括电磁干扰 (EMI) 评价。虽然 EMI 有多种原因,但手术室内最常见的原因在是单极电灼术。1如果 EMI 位于脉冲发生器周围 6 英寸内,则会抑制起搏和/或导致不当的心动过速治疗 – 视 CIED 的类型而定。损坏脉冲发生器的情况是罕见的,尽管有可能。尽管 CIED 具有最小化不当感知和起搏的算法,但是,EMI 仍可能会导致感知过度。起搏器感知过度将会导致起搏器将 EMI 解读为固有的心脏活动,防止在起搏器依赖性患者体内传输起搏刺激信号。ICD 感知过度将会导致 EMI 被解读为快速性心律失常,并可能会导致不当除颤。对于脐下手术,HRS/ASA 共识文件建议,至少需要重新设置 CIED 或放置一个磁力体,因为只要接地垫定位合适,感知过度的风险就很小。为最大限度减少电磁干扰,应对离散电极(接地垫)进行定位,以确保电流通路不会经过或靠近心脏植入式电子设备发生器或导联。
在围术期环境中,许多医务人员经常会使用磁力体,因为很容易应用;但是,根据器械类型、电池年龄以及器械程序设置方式的不同,CIED 对磁力体的反应也不一样。此外,放置磁力体可能会使患者处于异步模式,但起搏速率可能不满足患者的生理需求。一个重要的警告是,尽管将磁力体用于 ICD 会关闭快速性心律失常功能,但它不会对起搏器产生任何影响。麻醉团队成员有必要证实磁力体对于患者植入的 CIED 的影响。
Neelankavil 等在 2013 年发表的 APSF 文章简要列出了一个原则,适用于接受择期和紧急手术的 CIED 患者的围术期管理。1 针对择期手术的原则主要关注 EMI 对器械的风险、如何区分起搏器与 ICD,并根据起搏器依赖性提出了不同的管理方法(请参见来自原文的图 1 – https://www.apsf.org/article/managing-cardiovascular-implantable-electronic-devices-cieds-during-perioperative-care/)。
2020 年有什么新的发展?
自原文发表以来,CIED 技术已经有了发展,但是许多以前建议的围手术期方法仍然适用于今天。对于麻醉专业人员来说,CIED 的管理仍然是一种常见的临床场景,特别是因为这些器械在人群中的普及程度越累越高。考察 1993–2009 年间美国起搏器植入情况的一项研究显示,起搏器的使用率增加了 55%。3国家 ICD 登记数据库发现,单在美国,放置的器械就超过了 170 万只。4
我们是否过于关注围手术期的 CIED 管理?自上一篇 APSF 文章发表以来,技术进步的程度是否大到足以不再让麻醉专业人员担心围手术期 CIED 照护了?Schulman 等开展的一项临床相关性研究得出结论认为,对于接受有 EMI 的手术的 CIED 患者,EMI 仍是一个重大风险。对于接受多种手术的患者,他们的前瞻性研究使 ICD 处于“监控模式”。
在 20% 的患者在脐上非心脏手术过程中、29% 的患者在心脏手术过程中、0% 的患者如手术在脐下进行中,单极电灼术导致了临床上重大的 EMI(如果器械未识别出,EMI 将导致 ICD 产生不当的抗心动过速起搏或除颤)。本研究使用了方案规定的、按 ASA 和 HRS 建议定位的电手术离散电极。5 这项研究的强度确定了个体化照护计划对 CIED 患者的重要性 – 基于心脏器械的类型、CIED 位置和手术部位,因为即使现代 CIED 技术得到改进,仍然存在临床上重大的 EMI 风险。
自 2013 文章发表以来,1更新型的起搏器和 ICD 已获得了 FDA 批准,并被用于临床。对于麻醉专业人员来说,这些器械具有特殊的 CIED 围术期考量。Medronic Micra™ 是无导联的起搏器,已在美国获准使用。Micra 起搏器是一个独立的发生器和电极单室器械,通过股静脉放置在右心室内。其模式包括 VVIR(心室起搏、心室感知、为应对感知的事件而抑制起搏、速率调节)、VVI、VOO(异步心室起搏)和 OVO(仅心室感知),且没有除颤能力。无导联起搏器的优点是可以消除与经静脉导联相关的重大(有时甚至是毁灭性的)并发症:器械袋感染/血肿、血管内导联感染、血管血栓形成、导联脱出和导联折断。这些器械因为其体积很小,没有磁力传感器,因此将不会对磁力体作出反应。建议将这些器械设置为 VOO 模式,以减少预期有 EMI 时的感知过度。6
Boston Scientific 公司生产的皮下 ICD (S-ICD) 是另一种更新型的、在临床实践中遇到的 ICD。这种器械将被用于不需要心动过缓或抗心动过速起搏的、有室性心律失常风险的患者。7 尽管这种器械不能提供长期起搏,但是,如果患者治疗后出现了严重的心率减慢,其能在除颤电击以后30 秒钟内以 50 次脉冲/分钟的方式起搏。8 S-ICD 包含一个脉冲发生器和一根皮下导联。脉冲发生器和导联均被植入皮下组织,且均在胸外。9 脉冲发生器通常被植入前腋线和中腋线之间,位于第 6 肋间隙水平面上。导联则从脉冲发生器包埋袋向中间穿过,直达剑突,然后沿着左胸骨边缘向上穿行。与 Micra 起搏器类似,S-ICD 起搏器也没有经静脉导联。S-ICD 起搏器具有与传统 ICD 相同的磁力反应。将磁力体应用于脉冲发生器将关闭器械的抗心动过速功能,去除磁力体将恢复器械之前的设置状态。可确保正确定位磁力体的、S-ICD 具有的功能特点是“哔哔”声,这种声音表示已经检测到心律失常,并暂停了电击疗法。如果在应用磁力体时没有听到哔哔声,则建议重新将磁力体定位在器械上,直至出现哔哔声为止。它可能很难使磁力体保持在发生器上;根据手术类型和患者体位,重新设置器械可能更实用。
ASA 最近公布了有关围术期 CIED 管理的 2020 更新版实践咨询意见。10该文件强调了与 2011 ASA/HRS 共识声明相似的原则,包括围术期评估的重要性以及确定 EMI 所致风险的重要性。实践咨询意见中包含有几项新的建议,进一步说明了特殊的临床情形。该文件说明了如果 CIED 患者在需要紧急心脏复律或除颤时应该做什么。在这种情况下,咨询意见建议终止所有的 EMI,去除磁力体(如有应用),并观察患者是否有适当的、来自 CIED 的抗心动过速治疗。如果 CIED 被设置为关闭抗心动过速治疗,则确定是否需要重新设置器械。如果去除磁力体并未恢复 CIED 抗心动过速治疗,或如果不能快速设置器械,则进行紧急体外复律或除颤。新的实践咨询意见也强调了越来越多使用的 MRI 条件性 CIED 和这些器械的围手术期管理。该实践咨询意见特别不鼓励“不加区分地”将磁力体应用于 CIED,这与 2011 HRS/ASA 声明一致,建议在使用磁铁之前要知道患者 CIED 的磁力体反应。
自 2013 APSF 原文发表以来,技术已经有了变化;不过,重要文章中列出的基本原则今天仍然适用。在某些患者中,EMI 和 CIED 的感知过度仍然是麻醉专业人员关注的一个临床问题。随着新型起搏器和 ICD 的出现,麻醉专业人员将继续看到无数的器械,我们有能力为所有 CIED 患者制定周到的个性化计划。
Jacques Prince Neelankavil (医学博士)是加州大学洛杉矶分校医疗中心麻醉和围手术期医学系的麻醉学副教授和心脏麻醉部门首席专家。
Annemarie Thompson (医学博士)是杜克大学医疗中心心胸麻醉学和重症监护部门的麻醉、医学和人口健康科学教授以及麻醉住院医师培训项目总监
Aman Mahajan(医学博士、哲学博士、工商管理硕士)是匹兹堡大学和匹兹堡大学医学中心的 Peter 和 Eva Safar 教授、麻醉学和围术期医学系主任、生物医学信息学和生物工程学教授,以及匹兹堡大学医学中心围术期和外科服务部门的执行总监
作者没有利益冲突。
参考文献
- Neelankavil JP, Thompson A, Mahajan A. Managing cardiovascular implantable electronic devices (cieds) during perioperative care. APSF Newsletter. 2013;28:29,32–35. https://www.apsf.org/article/managing-cardiovascular-implantable-electronic-devices-cieds-during-perioperative-care/ Accessed August 12, 2020.
- Crossley GH, Poole JE, Rozner MA, et al. The Heart Rhythm Society (HRS)/American Society of Anesthesiologists (ASA) Expert Consensus Statement on the perioperative management of patients with implantable defibrillators, pacemakers and arrhythmia monitors: facilities and patient management. This document was developed as a joint project with the American Society of Anesthesiologists (ASA), and in collaboration with the American Heart Association (AHA), and the Society of Thoracic Surgeons (STS). Heart Rhythm. 2011;8:1114–54.
- Greenspon AJ, Patel JD, Lau E, et al. Trends in permanent pacemaker implantation in the United States from 1993 to 2009: increasing complexity of patients and procedures. J Am Coll Cardiol. 2012;60:1540–1545.
- The American College of Cardiology NCDR ICD Registry. https://cvquality.acc.org/NCDR-Home/registries/hospital-registries/icd-registry Accessed August 9, 2020.
- Schulman PM, Treggiari MM, Yanez ND, et al. Electromagnetic interference with protocolized electrosurgery dispersive electrode positioning in patients with implantable cardioverter defibrillators. Anesthesiology. 2019;130:530.
- Medtronic Micra Model MC1VR01 Manual. Available at https://europe.medtronic.com/content/dam/medtronic-com/xd-en/hcp/documents/micra-clinician-manual.pdf Accessed August 9, 2020.
- Burke MC, Gold MR, Knight BP, et al. Safety and efficacy of the totally subcutaneous implantable defibrillator: 2-year results from a pooled analysis of the IDE Study and EFFORTLESS Registry. J Am Coll Cariol. 65:1605–1615, 2015.
- Weiss R, Knight BP, Gold MR, et al. Safety and efficacy of a totally subcutaneous implantable-cardioverter defibrillator. Circulation. 128:944–953,2013.
- Lambiase PD, Srinivasan NT. Early experience with the subcutaneous ICD. Curr Cardiol Rep. 2014;16:516,2014.
- Practice advisory for the perioperative management of patients with cardiac implantable electronic devices: pacemakers and implantable cardioverter defibrillators 2020. Anesthesiology. 2020;132:225–252. https://doi.org/10.1097/ALN.0000000000002821 Accessed August 9, 2020.


 Issue PDF
Issue PDF