By Fvasconcellos (Own work) [Public domain], via Wikimedia Commons
Space-filling model of sugammadex sodium
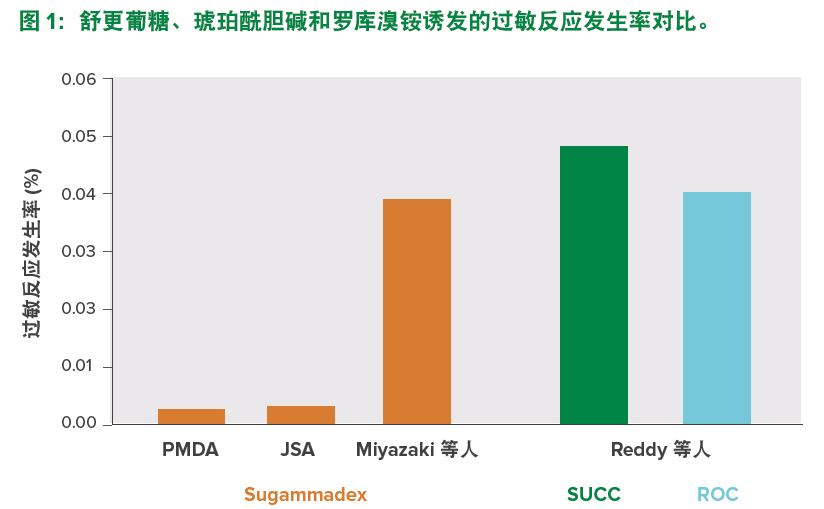
PMDA:日本药品与医疗器械管理局(Pharmaceuticals and Medical Devices Agency)
JSA:日本麻醉医师协会(Japanese Society of Anesthesiologists)
SUCC:琥珀酰胆碱
ROC:罗库溴铵在
JSA 报告的 95 个过敏反应病例中,76 例具有明确的由舒更葡糖诱发的过敏反应的发病时间。本项 JSA 研究表明,在 76 个由舒更葡糖诱发的过敏反应病例中(具有明确的发病时间),在 50(65.8%)和 66(86.8%)个病例中,由舒更葡糖诱发的过敏反应都在给药后 5-10 分钟之内发生。6 本项数据与近期进行的一次由舒更葡糖诱发的过敏反应病例回顾中的数据形成了对比。根据此次病例回顾相关数据,由舒更葡糖诱发的过敏反应的最慢发病时间为给药后 4 分钟,发病时间平均值约为 2 分钟。9 舒更葡糖的给药时间通常在手术结束后,拔除气管插管前,但是,由舒更葡糖诱发的过敏反应可能在拔除气管插管后发生。据报告,由舒更葡糖诱发的过敏反应的症状通常与呼吸系统有关,包括气道水肿和支气管痉挛。据报告,在由舒更葡糖诱发的过敏反应病例中的大约 50% 之中,动脉血氧饱和度有所降低。9 当患者在拔除气管插管后出现严重的呼吸系统症状时,医护人员可能需要对患者进行重新插管或其他支持性治疗。如果医护人员未能及时发现此类症状,患者的生命可能面临严重的风险。对于在拔管后立即将患者转移至 PACU、ICU 或其他病房的医疗机构来说,患者在某个时段内可能并未处于严密监控之下,这种情况可能导致医护人员无法及时进行诊断并对患者进行治疗。6 因此,对于使用舒更葡糖的患者来说,医护人员应当在给药之后至少 5 分钟之内在手术室里密切观察患者的情况。此外,医护人员还应在患者被转运的过程中对其进行密切监控。
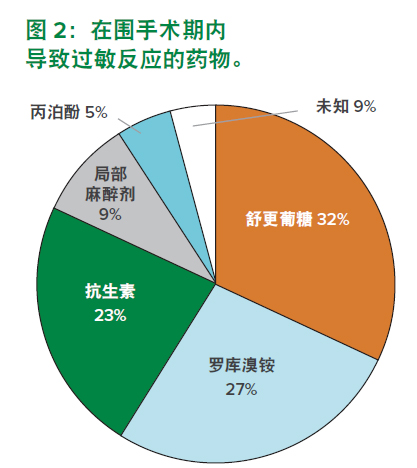
总百分比超过 100%,因为其中包括使用了多种致敏药物的患者。
过敏反应确诊必须满足以下条件:患者的症状符合临床过敏反应诊断标准、患者血液中的组胺和/或类胰蛋白酶水平较高,以及患者在皮肤测试中对诱发过敏反应的药物出现阳性过敏反应。10 本文作者在群马大学医院和附近医疗机构里对 22 名出现了围手术期过敏反应的患者进行了皮肤测试,旨在确定 2012 年 5 月至 2016 年 3 月期间(4 年)诱发过敏反应的致敏药物。在 22 个病例中,作者确定了 20 个病例中诱发围手术期过敏反应的致敏药物。诱发围手术期过敏反应的三大主要致敏药物包括舒更葡糖(8 名患者,32%)、罗库溴铵(6 名患者,27%)和抗生素(5 名患者,23%)(图 2)。我们无法得知我们所在的医疗机构内因每种药物诱发的过敏反应的发生率,因为,我们并没有跟踪使用过此类药物的患者总人数。但是,在我们的研究中,舒更葡糖的确是最常见的围手术期过敏反应致敏药物。我们在 2016 年召开的 JSA 第 63 次年会(日本福冈)上公布了此项研究结果。近期,Miyazaki 等人在日本境内进行了一项与由舒更葡糖诱发的过敏反应有关的研究并发表了研究成果,他们在研究中发现,每 6 名患者中只有 1 名出现了血浆类胰蛋白酶水平提高的情况,但是,对由舒更葡糖诱发的过敏反应的诊断依据是临床症状出现的时间。7 尽管皮肤测试是确定过敏反应致敏药物的黄金标准,但是,皮肤测试也有一些不足之处。皮肤测试可能导致过敏反应再次发生,尽管这种可能性较低。此外,患者在皮肤测试中会感到疼痛。特异性免疫球蛋白水平测量是进行过敏反应的一种替代性体外方法,但是需要使用患者血样,而且,目前尚无针对舒更葡糖-特异性免疫球蛋白水平的检测方法。近期,研究人员建议使用嗜碱粒细胞活化法诊断由舒更葡糖诱发的过敏反应。11 由于其他药物也可能导致过敏反应,所以,检验人员有必要进行多次试验,以便提高诊断由舒更葡糖诱发的过敏反应的准确性。
结论
我们已经提供了由 PMDA、JSA 报告的数据以及 Miyazaki 等人提供的与由舒更葡糖诱发的过敏反应有关的数据。鉴于不同研究中由舒更葡糖诱发的过敏反应的报告发生率有所不同,并且,我们也缺少包含舒更葡糖给药剂量的真实数据,所以,我们目前无法对发生率给出准确的估算。由于 PMDA 和 JSA 提供的报告采用了一种由医生自愿报告过敏反应病例的框架,所以,此类报告不太可能囊括全部过敏反应病例,从而导致数据被低估的情形。相比之下,Miyazaki 等人进行的研究也有一些局限性,例如,数据量小、研究范围仅限于单个机构,以及测试量不足。尽管 JSA 每年都会要求成员机构提交“事故病例”发生率报告(患者出现并发症且麻醉专家无法预料此类并发症),但是,他们提交报告的主要目的并不是估算由某些药物诱发的过敏反应的发生率。因此,我们需要通过进一步研究确定在日本境内和全世界范围内由舒更葡糖诱发的过敏反应的发生率。舒更葡糖在日本迅速得到广泛应用的原因可能是很多麻醉专业人士确信其有效性。但是,为了安全地使用舒更葡糖,麻醉专业人士仍应意识到舒更葡糖诱发过敏反应的可能性,至少在给药后 5 分钟内密切观察患者的情况。Takazawa 博士是群马大学医院(Gunma University Hospital)(日本群马)特护病房助理教授。Miyasaka 是圣路加国际大学(St. Luke’s International University)(日本东京)围麻醉期护理系教授。 Sawa 博士是帝京大学(Teikyo University)(日本帝京)麻醉学系教授。Iida 博士是岐阜大学(Gifu University)(日本岐阜)医学研究生院麻醉学与疼痛医学系教授和系主任。
上述所有作者均为日本麻醉医师协会安全委员会成员。上述作者没有与本文有关的其他需公开信息。
参考文献
- Takazawa T, Tomita Y, Yoshida N, et al. Three suspected cases of sugammadex-induced anaphylactic shock.BMC Anesthesiol 2014;14:92.
- Godai K, Hasegawa-Moriyama M, Kuniyoshi T, et al. Three cases of suspected sugammadex-induced hypersensitivity reactions.Br J Anaesth 2012;109:216–8.
- Obara S, Kurosawa S, Honda J, et al. Cardiac arrest following anaphylaxis induced by sugammadex in a regional hospital.J Clin Anesth 2017;44:62–3.
- Nakanishi T, Ishida K, Utada K, et al. Anaphylaxis to sugammadex diagnosed by skin prick testing using both sugammadex and a sugammadex-rocuronium mixture.Anaesth Intensive Care 2016;44:122–4.
- Johansson SG, Bieber T, Dahl R, et al. Revised nomenclature for allergy for global use:Report of the Nomenclature Review Committee of the World Allergy Organization, October 2003.J Allergy Clin Immunol 2004;113:832–6.
- Takazawa T, Mitsuhata H, Mertes PM.Sugammadex and rocuronium-induced anaphylaxis.J Anesth 2016;30:290–7.
- Miyazaki Y, Sunaga H, Kida K, et al. Incidence of anaphylaxis associated with sugammadex.Anesth Analg 2017; Oct 19. doi:10.1213/ANE.0000000000002562. [Epub ahead of print]
- Reddy JI, Cooke PJ, van Schalkwyk JM, et al. Anaphylaxis is more common with rocuronium and succinylcholine than with atracurium.Anesthesiology 2015;122:39–45.
- Tsur A, Kalansky A. Hypersensitivity associated with sugammadex administration: a systematic review.Anaesthesia 2014;69:1251–7.
- Dewachter P, Mouton-Faivre C, Emala CW.Anaphylaxis and anesthesia: controversies and new insights.Anesthesiology 2009;111:1141–50.
- Takazawa T, Horiuchi T, Yoshida N, et al. Flow cytometric investigation of sugammadex-induced anaphylaxis.Br J Anaesth 2015;114:858–9.

