 Lorsque les patients arrivent dans l’unité de soins postopératoire après avoir subi une intervention chirurgicale lourde non cardiaque, les familles pensent qu’ils ont survécu à la partie la plus risquée de leur parcours périopératoire. Cette présomption est fausse. La mortalité dans les 30 jours qui suivent la chirurgie est 100 fois plus élevée que la mortalité pendant l’intervention proprement dite.1,2 En fait, si le mois qui suit la chirurgie était considéré comme une maladie, il serait la troisième plus grande cause de décès aux États-Unis.3
Lorsque les patients arrivent dans l’unité de soins postopératoire après avoir subi une intervention chirurgicale lourde non cardiaque, les familles pensent qu’ils ont survécu à la partie la plus risquée de leur parcours périopératoire. Cette présomption est fausse. La mortalité dans les 30 jours qui suivent la chirurgie est 100 fois plus élevée que la mortalité pendant l’intervention proprement dite.1,2 En fait, si le mois qui suit la chirurgie était considéré comme une maladie, il serait la troisième plus grande cause de décès aux États-Unis.3
Trois-quarts du taux de mortalité postopératoire surviennent pendant l’hospitalisation initiale, autrement dit sous surveillance médicale directe dans nos établissements les plus réputés.4 Les deux causes comparables les plus courantes de la mortalité à 30 jours après une chirurgie non cardiaque sont une hémorragie majeure et des lésions myocardiques.5,6
Lésions myocardiques
Un infarctus du myocarde (IM), selon la quatrième définition universelle, se caractérise par une élévation de la troponine et des symptômes ou des signes d’ischémie myocardique.7 Les lésions myocardiques après une chirurgie non cardiaque (MINS) se caractérisent par une élévation de la troponine présumée d’origine ischémique et sont fortement associées à la mortalité à 30 jours8 et à un an9. La MINS comprend l’infarctus du myocarde et d’autres lésions myocardiques ischémiques qui ne répondent pas à la définition de l’infarctus du myocarde.
Les lésions myocardiques périopératoires sont généralement des évènements de type 2, causés globalement par une diminution des apports. Le MINS et les infarctus de myocarde périopératoires sont donc différents des infarctus non opératoires, qui sont généralement la conséquence d’une rupture de plaque. Un fait donne à réfléchir. La mortalité engendrée par les évènements myocardiques périopératoires est plus élevée que les infarctus non opératoires et elle mérite donc une attention toute particulière.10,11
Détection de la troponine
Plus de 90 % des MINS et IM surviennent dans le courant des deux premiers jours postopératoires et plus de 90 % sont asymptomatiques.12 Bien qu’il soit tentant d’associer les élévations de troponine asymptomatique à une « troponite », la mortalité est quasiment aussi élevée sans symptômes qu’avec (Figure 1). Les MINS doivent donc être prises très au sérieux comme des infarctus symptomatiques classiques.
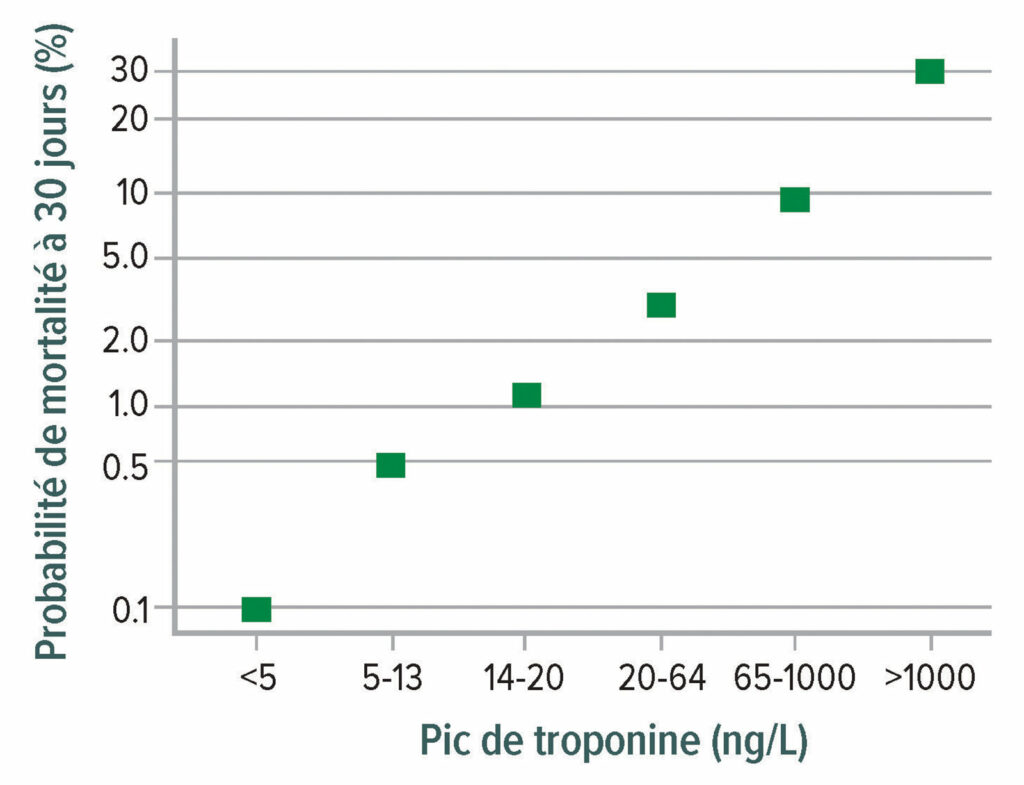
Figure 1 : Mortalité à 30 jours comme fonction du pic de troponine haute sensibilité T postopératoire. Augmentation marquée de la mortalité à partir de 0,1 % avec une concentration de troponine T <5 ng/L à une mortalité de 30 % lorsque la troponine T dépasse 1.000 ng/L.
Données provenant du Comité de rédaction pour les enquêteurs de l’étude Vision : Association des niveaux de troponine haute sensibilité postopératoires et des lésions myocardiques et la mortalité à 30 jours chez les patients opérés d’une chirurgie non cardiaque.12
Ce chiffre a été adapté à partir des données présentées dans le document de référence 12.
En l’absence de détection systématique de la troponine, la plupart des lésions myocardiques passent inaperçues. Une stratégie raisonnable consiste à mesurer la troponine avant l’intervention chirurgicale et pendant les trois premiers jours postopératoires. Les seuils des MINS diffèrent en fonction de la génération du type du test :
- Troponine non haute sensibilité (quatrième génération) T ≥0,03 ng/ml4 ;
- Troponine haute sensibilité T ≥65 ng/L, ou troponine haute sensibilité T=20–64 ng/L et une augmentation de ≥5 ng/L par rapport à la référence12 ;
- Troponine haute sensibilité I (essai d’Abbott [Abbott Park, IL]) ≥60 ng/L13 ;
- Troponine haute sensibilité I (essai de Siemens [Munich, Germany]) ≥75 ng/L (Borges, non publié) ;
- La troponine I (autres essais) a une valeur au moins deux fois supérieure au 99e percentile local ;
- Une augmentation d’au moins 20 % chez les patients qui ont des concentrations préopératoires de troponine haute sensibilité supérieures à 80 % des seuils précédemment cités.
Hypotension
Les MINS et les IM sont fortement associés aux facteurs de risque du patient non modifiables, notamment l’âge, le diabète et les antécédents cardiovasculaires. De grands essais randomisés (n=7 000–10 000) ont démontré que l’IM n’est pas prévenu par l’utilisation de bétabloquants,14 la non utilisation du protoxyde d’azote,15 par l’administration de clonidine,16 ou d’aspirine.17 Récemment, dans le cadre d’un grand essai, un patient sur sept qui avait des MINS subissait un évènement vasculaire majeur (principalement un nouvel infarctus) dans les 17 mois suivant l’intervention.11
L’hypotension pendant l’intervention chirurgicale est associée aux MINS et à un IM, le seuil de dommage étant une pression artérielle moyenne (PAM) d’environ 65 mmHg (Figure 2).18,19 L’hypotension postopératoire est aussi associée à l’infarctus du myocarde, indépendemment de l’hypotension pendant l’intervention chirurgicale (Figure 3).20,21
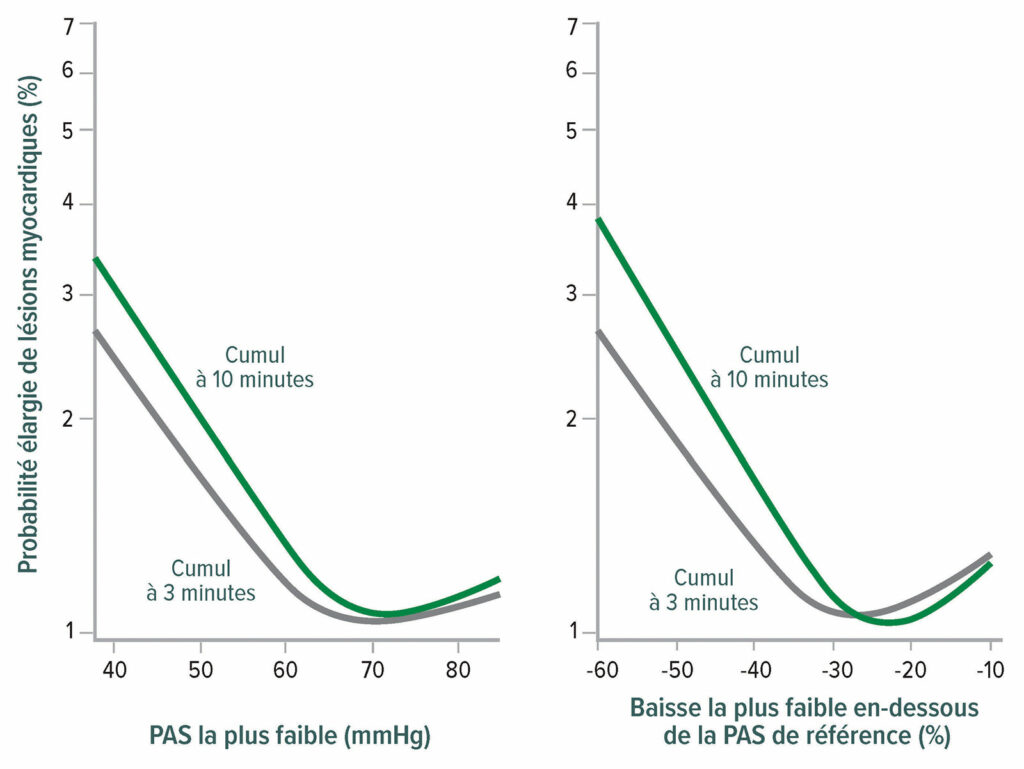
Figure 2 : Seuils inférieurs de pression artérielle moyenne (PAM) pour les risques de lésions myocardiques après une chirurgie non cardiaque. Le graphique de gauche représente la relation entre la pression artérielle moyenne absolue cumulée, la plus faible, maintenue pendant 3 et 10 minutes et les lésions myocardiques. Le graphique de droite représente la relation entre la pression artérielle moyenne relative cumulée, la plus faible, maintenue pendant 3 et 10 minutes et les lésions myocardiques. Les deux graphiques sont des régressions logistiques à variables multiples.18
Reproduit et modifié avec l’aimable autorisation des auteurs. Salmasi V, Maheshwari K, Yang D, Mascha EJ, Singh A, Sessler DI, Kurz A. Relationship between intraoperative hypotension, defined by either reduction from baseline or absolute thresholds, and acute kidney and myocardial injury after noncardiac surgery: a retrospective cohort analysis. Anesthesiology.2017;126:47–65.
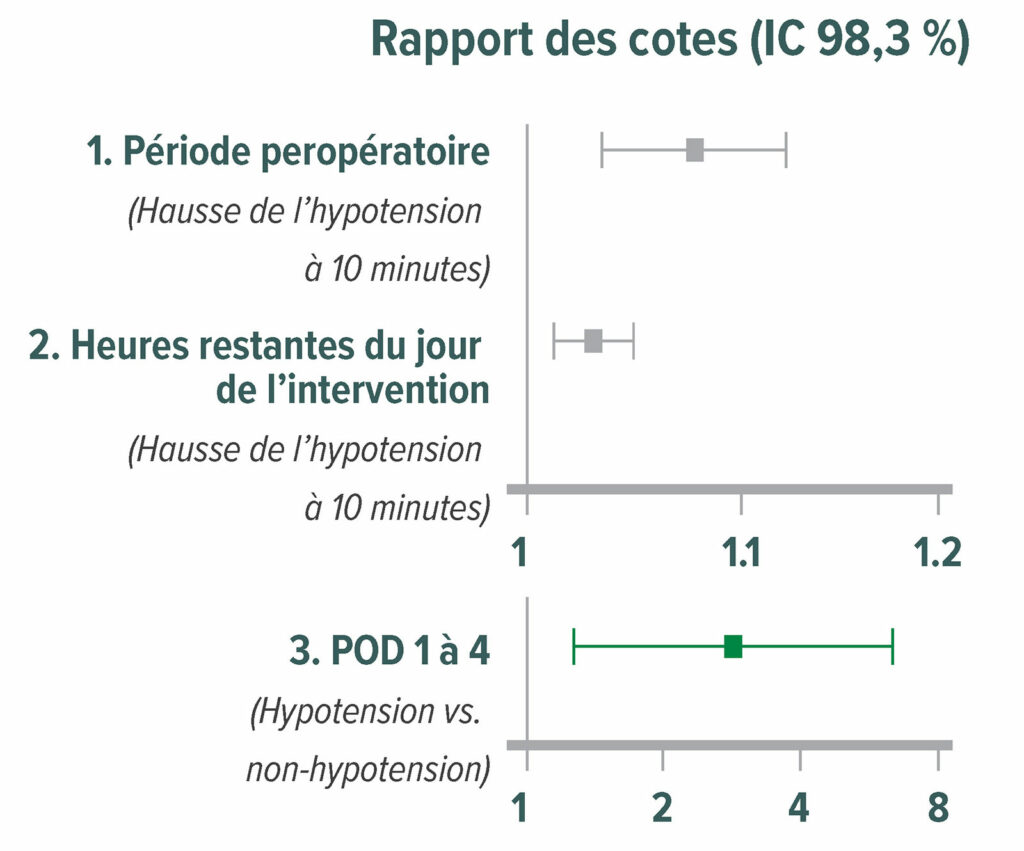
Figure 3 : Rapports des cotes (odds ratios) de l’effet relatif moyen sur le critère principal d’évaluation de l’infarctus du myocarde et de la mortalité à 30 jours pour trois périodes périopératoires : intraopératoire, les quelques heures restantes du jour de la chirurgie et les quatre premiers jours d’hospitalisation postopératoires (POD). Les intervalles de confiance pour les comparaisons multiples ont été ajustés selon la correction Bonferroni. Ainsi, P<0,017 (0,05/3) a été jugé significatif pour l’effet relatif moyen. Les carrés représentent les rapports des cotes et les lignes représentent les intervalles de confiance. POD = jour postopératoire.20
Reproduit et modifié avec l’aimable autorisation des auteurs. Sessler DI, Meyhoff CS, Zimmerman NM, Mao G, Leslie K, Vasquez SM, Balaji P, Alvarez-Garcia J, Cavalcanti AB, Parlow JL, Rahate PV, Seeberger MD, Gossetti B, Walker SA, Premchand RK, Dahl RM, Duceppe E, Rodseth R, Botto F, Devereaux PJ. Period-dependent associations between hypotension during and for four days after noncardiac surgery and a composite of myocardial infarction and death: a substudy of the POISE-2 trial. Anesthesiology. 2018;128:317–327.
Les résultats de la cohorte VISION montrent que l’hypotension postopératoire est courante (Figure 4) et est fortement associée à des évènements vasculaires majeurs. L’hypotension postopératoire est plus fortement associée à l’infarctus du myocarde et/ou au décès qu’une hypotension peropératoire (Figure 5).22 L’hypotension périopératoire est également associée à l’AVC,14,22-25 mais moins fréquemment.26
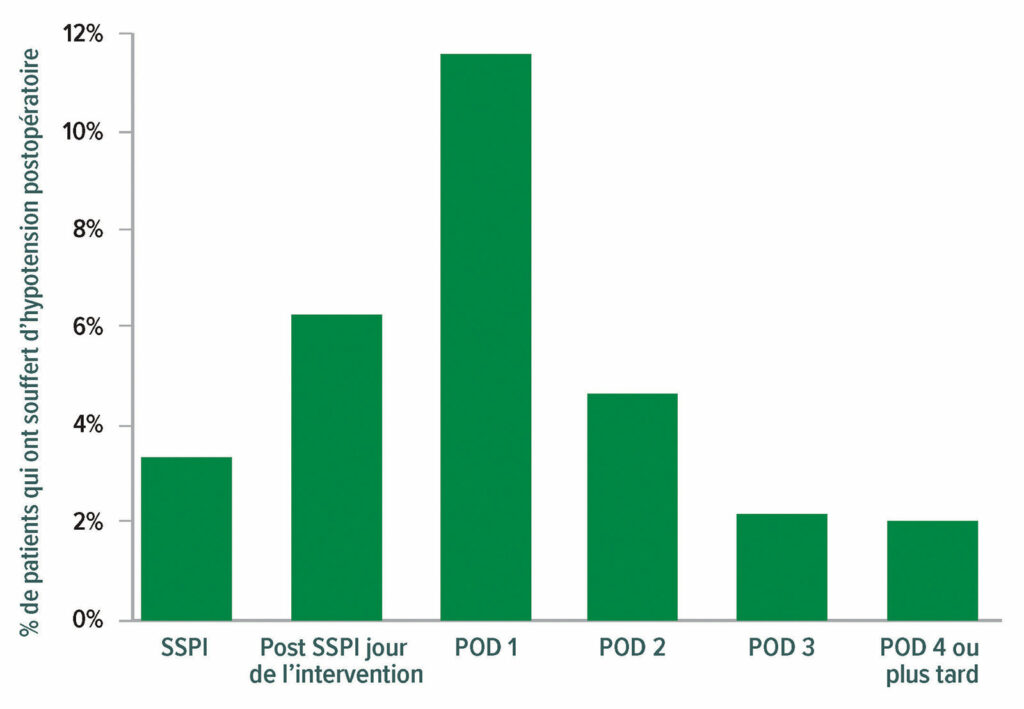
Figure 4 : Hypotension cliniquement significative (pression systolique <90 et nécessitant une intervention). Au total, sur 14 687 patients, 2860 (soit 19,5 %) ont subi au moins un épisode d’hypotension cliniquement significative après leur chirurgie ; 2728 (soit 95,4 %) de ces patients ont subi un épisode hypotensif le troisième jour postopératoire (POD). BO = bloc opératoire ; PACU = unité de soins post-anesthésie.22
Reproduit et modifié avec l’aimable autorisation des auteurs. Roshanov PS, Rochwerg B, Patel A, et al. Withholding versus continuing angiotensin-converting enzyme inhibitors or angiotensin II receptor blockers before noncardiac surgery: an analysis of the vascular events in noncardiac surgery patients cohort evaluation prospective cohort. Anesthesiology. 2017;126:16–27.
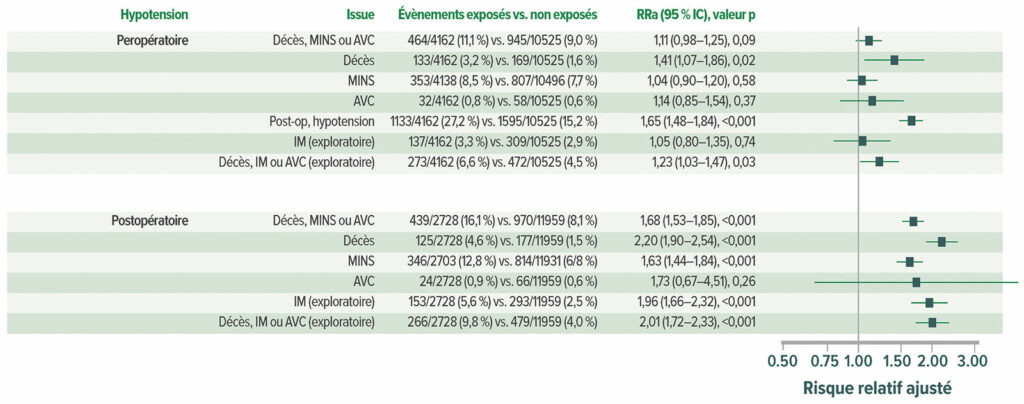
Figure 5 : Association ajustée entre l’hypotension et les décès et évènements vasculaires postopératoires chez l’ensemble des 14.687 patients. RRa = risque relatif ajusté.22
Reproduit et modifié avec l’aimable autorisation des auteurs. Roshanov PS, Rochwerg B, Patel A, et al. Withholding versus continuing angiotensin-converting enzyme inhibitors or angiotensin II receptor blockers before noncardiac surgery: an analysis of the vascular events in noncardiac surgery patients cohort evaluation prospective cohort. Anesthesiology. 2017;126:16–27.
Autres facteurs
Deux études récentes ont identifié des associations remarquablement fortes entre l’anémie postopératoire, les lésions myocardiques27 et l’infarctus,28 même après un ajustement pour tenir compte des antécédents des patients et de l’anémie préopératoire. En revanche, une fréquence cardiaque jusqu’à 100 battements/min et une hypertension systolique jusqu’à 200 mmHg ne sont pas des facteurs de risque de dommages myocardiques postopératoires.29 L’hypoxémie dans les services hospitaliers généraux est courante, profonde et prolongée30 ; toutefois, on ne sait pas si l’hypoxémie contribue aux lésions myocardiques. Heureusement, dans les services hospitaliers, l’occurrence simultanée de l’hypotension et de l’hypoxémie, qui pourrait favoriser tout particulièrement des lésions liées à une diminution des apports, est rare.
Insuffisance rénale aiguë
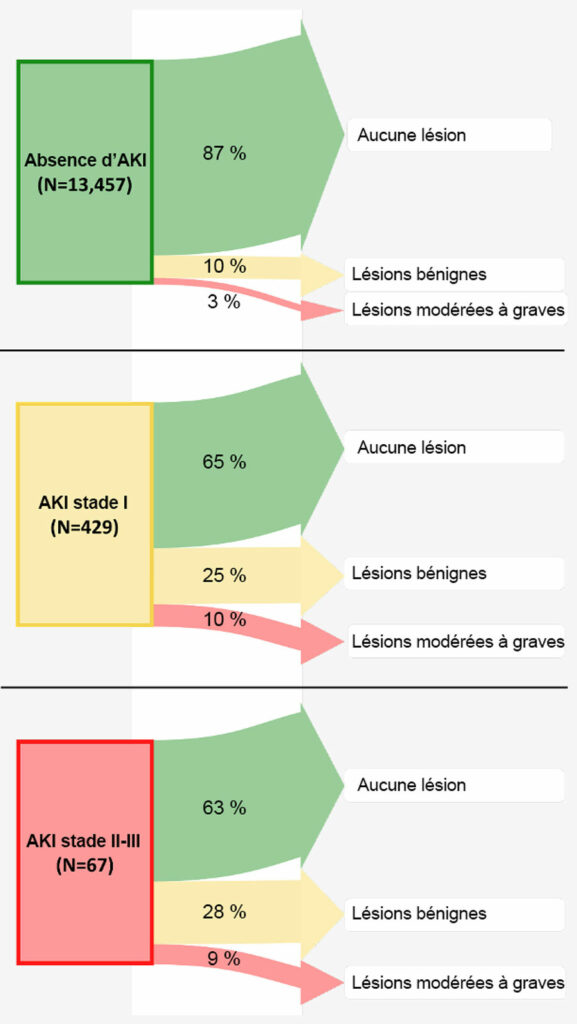
Figure 6 : Résultats rénaux 1 à 2 ans après la chirurgie, en fonction du stade de l’insuffisance rénale aiguë postopératoire. La largeur des flèches représente le pourcentage de patients de chaque groupe étudié souffrant de chaque stade d’insuffisance rénale durable.37 Un quart des patients souffrant d’insuffisance rénale postopératoire de stade I (hausse de la créatine de ≥ 0,3 mg/dl ou 1,5–1,9 fois le niveau de référence) présentait encore une légère insuffisance 1 à 2 ans plus tard, et 10 % présentaient un stade d’insuffisance encore plus élevé. Un bon tiers des patients avec une insuffisance rénale de stade I présentait donc une insuffisance rénale 1 à 2 ans après la chirurgie. Par conséquent, les patients présentant une insuffisance postopératoire de stade I avaient un rapport des cotes (95 % IC) de 2,3 (1,8, 2,9) de souffrir d’insuffisance rénale durable chronique par rapport aux patients sans insuffisance rénale postopératoire. Nous avons donc conclu que chez les adultes se rétablissant d’une chirurgie non cardiaque, même une légère augmentation postopératoire de la créatinine plasmatique, correspondant à une insuffisance rénale de stade I, est associée à un résultat rénal plus grave 1 à 2 ans après la chirurgie, devant par conséquent être considéré comme un résultat périopératoire cliniquement important.
Reproduit et modifié avec l’aimable autorisation des auteurs. Turan A, Cohen B, Adegboye J, Makarova N, Liu L, Mascha EJ, Qiu Y, Irefin S, Wakefield BJ, Ruetzler K, Sessler DI. Mild acute kidney injury after noncardiac surgery is associated with long-term renal dysfunction: a retrospective cohort study. Anesthesiology. 2020;132:1053–1061.
Après une chirurgie non cardiaque, il est courant qu’une nouvelle insuffisance rénale aiguë (AKI) se déclenche, les stades 2–3 survenant chez 1 % des patients,31 et jusqu’à 7,4 % des patients lorsque l’AKI de stade 1 est incluse.32 Il n’existe actuellement aucune méthode fiable de prédiction de l’AKI.33 Le seuil de dommage hypotensif pour l’AKI est semblable ou légèrement supérieur à celui des lésions myocardiques, probablement parce que le métabolisme des reins est élevé.18,32,34
Il convient de noter qu’à un seuil de PAM plus strict <55 mmHg, <5 minutes en-dessous de cette pression est associée à une hausse de 18 % du risque d’AKI.34 D’autres analyses signalent des associations semblables.35 Globalement, ces études confirment un lien fort, en termes à la fois de profondeur et de durée, entre l’hypotension et l’AKI, d’où l’importance de tenir compte de la durée et de l’amplitude pour quantifier l’hypotension.
Les implications de l’AKI periopératoire dépassent l’hospitalisation proprement dite. Dans une étude observationnelle de cohorte de 1869 patients visant à examiner l’association de l’AKI périopératoire et de la mortalité à 1 an, l’AKI était liée à un risque de décès ajusté de 3.36 Enfin, nous notons que même des degrés d’AKI plus faibles ont des conséquences durables : 37 % des AKI de stade 1 persistent ou s’aggravent 1 à 2 ans après une chirurgie non cardiaque (Figure.6).37
Delirium
Le delirium est une complication courante d’une chirurgie cardiaque et est associé à la morbidité et à la mortalité.38-42 L’incidence signalée de delirium après une chirurgie non cardiaque majeure est de l’ordre de 10 % et augmente considérablement lorsque l’âge du patient dépasse 65 ans.43 La pathophysiologie du delirium est multifactorielle mais elle inclut vraisemblablement une perfusion insuffisante du cerveau, qui survient lorsque la pression artérielle moyenne est inférieure à la limite basse d’autorégulation.44-46
Le seuil d’autorégulation cérébrale demeure imprécis, mais il semblerait qu’il existe une variation considérable d’un individu à l’autre et qu’il puisse atteindre 85 mmHg chez certains patients.47,48 Conformément à cette théorie, l’hypotension est associée au delirium et à un déclin cognitif (Figure 7),49-51 bien que ce ne soit pas systématique.52-54 Des données randomisées limitées (n=199) indiquent que l’hypotension cause le delirium.55
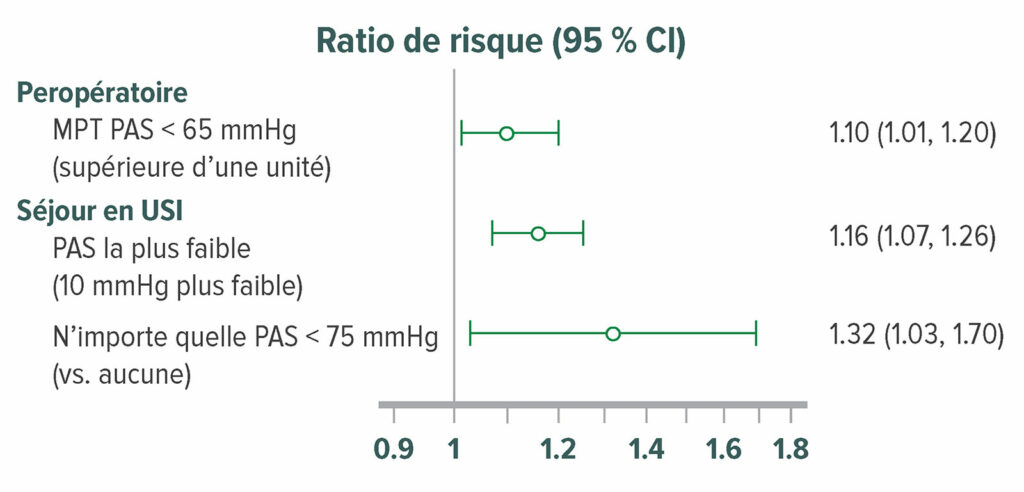
Figure 7 : Rapport de risque ajusté de delirium chez 908 patients postopératoires qui ont été admis directement du bloc opératoire dans l’unité de soins intensifs chirurgicaux. Le delirium a été évalué par la Méthode d’évaluation de la confusion pour les patients des unités de soins intensifs à 12 heures d’intervalles. 316 (35 %) patients présentaient un delirium dans les cinq premiers jours postopératoires dans l’unité de soins intensifs chirurgicaux. L’hypotension peropératoire, PAM <65 mmHg était largement associée à des probabilités plus plus élevées d’un risque important de delirium postopératoire.50 MPT=moyenne pondérée dans le temps.
Reproduit et modifié avec l’aimable autorisation des auteurs. Maheshwari K, Ahuja S, Khanna AK, Mao G, et al. Association between perioperative hypotension and delirium in postoperative critically ill patients: a retrospective cohort analysis. Anesth Analg. 2020;130:636–643.
Les patients souffrant de delirium après une chirurgie sont beaucoup plus susceptibles que d’autres de développer des troubles cognitifs à long terme ;56 cependant, on ne sait toujours pas s’il existe un lien de cause à effet. L’hypotension peut également provoquer un AVC déclaré, ou beaucoup plus communément, un AVC silencieux, fortement lié au delirium.57
Gestion de la tension artérielle
Il est impossible de prédire de manière fiable l’hypotension peropératoire en fonction des co-morbiditésd’un patient ou de la procédure chirurgicale.58 La meilleure méthode de prédiction et de traitement de l’hypotension périopératoire reste incertaine. La corrélation entre l’index cardiaque peropératoire et la tension artérielle est limitée et l’hypothèse que le maintien d’un volume vasculaire suffisant permette de prévenir l’hypotension ne semble pas exacte. En outre, dans une étude, un tiers des hypotensions peropératoires était survenu entre l’induction d’anesthésie et l’incision chirurgicale et était donc à l’évidence la conséquence des produits anesthésiants plutôt que des modifications du volume vasculaire. L’hypotension survenant avant l’incision a un lien aussi fort avec les lésions subies par les organes que l’hypotension ultérieure.59
Le monitorage continu de la pression artérielle permet de mieux détecter l’hypotension que les mesures prises à 5 minutes d’intervalle,60,61 donnant ainsi la possibilité aux cliniciens d’intervenir plus tôt.61 Un développement récent très intéressant est un algorithme qui prédit l’hypotension future à partir de la forme d’onde artérielle.62 Bien qu’un essai avec peu de patients ait signalé moins d’hypotension lorsque la gestion était guidée par l’algorithme,63 une étude plus large n’a pas identifié de bénéfices.64 La différence résulte probablement des différences d’algorithmes de traitement et il est évident qu’il est nécessaire d’effectuer un essai fiable.
Les vasopresseurs tels que la phényléphrine ou la noradrénaline sont couramment utilisés pour traiter l’hypotension pendant une chirurgie. La phényléphrine est de loin le vasopresseur le plus couramment utilisé aux États-Unis,65 alors que la noradrénaline est généralement privilégiée ailleurs. La phényléphrine est un agoniste alpha-adrénergique pur qui élève la pression artérielle en augmentant la résistance vasculaire systémique, associée généralement à une baisse compensatoire du débit cardiaque.66 En revanche, la noradrénaline est un puissant agoniste adrénergique des récepteurs alpha , avec une activité agoniste adrénergique des récepteurs bêta faible, contribuant au maintien du débit cardiaque. Par conséquent, bien que la pression artérielle soit maintenue de manière comparable avec chacun des vasopresseurs,67 la phényléphrine réduit le débit sanguin splanchnique et l’apport d’oxygène.68 Les cliniciens devraient éviter la phényléphrine chez les patients en choc septique.69
Malgré les avantages théoriques de la préservation du débit cardiaque et de la perfusion splanchnique avec l’utilisation de la noradrénaline, il existe peu d’éléments probants d’une quelconque amélioration du devenir des patients chirurgicaux.70 Par conséquent, la phényléphrine et la noradrénaline sont toutes les deux très couramment utilisées dans le cadre de la pratique clinique, principalement en fonction de la préférence clinique et de la disponibilité. Il n’existe aucun élément probant que les vasopresseurs peropératoires à faible dose soient eux-mêmes nocifs et il est probablement imprudent d’autoriser l’hypotension afin d’éviter l’utilisation de vasopresseurs. La noradrénaline peut être administrée sans risque par cathéter central ou sur voie périphérique.71 Une étude récente portant sur 14 328 patients a permis de relever uniquement 5 évènements d’extravasation et pas un seul patient n’a subi de lésion tissulaire locale.72
Dans les services hospitaliers généraux, l’hypotension est courante, prolongée et profonde. Il est probable que les lésions hypotensives périopératoires causées aux organes interviennent le plus souvent après l’intervention plutôt que pendant. Le défi est que la pression artérielle est généralement mesurée par intermittence. Même à 4 heures d’intervalle, environ la moitié des épisodes hypotensifs potentiellement graves passent inaperçus.73 (De même, la majorité des épisodes d’hypoxémie passe inaperçue avec une surveillance intermittente dans les services.30) La détection et le traitement fiables de l’hypotension dans les services nécessiteront une surveillance continue des signes vitaux. Cependant dans cette attente, il est utile d’éviter des inhibiteurs de l’enzyme de conversion de l’angiotensine et les agents bloquant les récepteurs de l’angiotensine le jour de la chirurgie,22 et de reprendre des médicaments contre l’hypertension chronique uniquement si nécessaire.
Association vs. lien de cause à effet
L’hypotension peropératoire est courante. En fonction de la définition et de la population, un quart ou plus de l’ensemble des patients chirurgicaux ont une pression artérielle moyenne < 65 mmHg pendant la chirurgie. L’hypotension est également courante après une chirurgie et seulement environ la moitié des épisodes potentiellement graves sont détectés par la surveillance habituelle des signes vitaux à 4 heures d’intervalle.73 L’hypotension postopératoire est souvent prolongée et il semble probable qu’un grand nombre, voire la majorité, des lésions myocardiques et rénales se développent après la chirurgie.
Actuellement, il existe peu d’éléments pour prouver que les associations entre l’hypotension et les MINS et les AKI ont un lien de cause à effet. Cependant, un petit essai randomisé (n=292) a démontré que la prévention de l’hypotension peropératoire réduit de 25 % le risque de complications majeures, ce qui est biologiquement plausible.74 Deux grands essais devraient permettre d’identifier la part (le cas échéant) des associations observées qui ont un lien de cause à effet : POISE-3 (n=10 000, NCT03505723) est quasiment achevée et GUARDIAN (n=6250, NCT en cours d’attribution) s’apprête à débuter.
Résumé
L’hypotension peropératoire et l’hypotension postopératoire sont associées à des lésions myocardiques et rénales. Les associations sont signalées régulièrement dans diverses populations, à partir de seuils et méthodes d’analyse divers, et elles persistent après les ajustements nécessaires pour tenir compte des co-morbidités connuse. (Les associations avec les co-morbidités sont plus fortes que pour l’hypotension, mais l’hypotension est un facteur de risque modifiable.) Les associations entre l’hypotension et le delirium sont également signalées, mais les éléments probants demeurent rares.
Il existe actuellement peu de données randomisées pour caractériser l’étendue du lien de cause à effet des associations observées. Des grands essais sont en cours, mais les résultats ne seront pas publiés avant quelque temps. La question est donc de savoir comment gérer la pression artérielle dans cette attente.
Deux facteurs méritent une attention particulière. Le premier est de connaître la probabilité d’un lien de cause à effet entre l’hypotension et les dommages causés aux organes. Il est certain que la plupart des associations observées sont liées à des biais de sélection des patients qui sont plus prédictifs que modifiables. Il semble toutefois probable qu’une partie ait un lien de cause à effet, permettant donc une intervention. Le deuxième facteur à prendre en compte est le degré de difficulté associé au maintien de la pression artérielle moyenne peropératoire au-dessus de 65 mmHg ou un seuil semblable. En règle générale, il n’est pas difficile (ni coûteux) de maintenir la pression artérielle peropératoire bien au-dessus du seuil de dommage apparent. Dans de nombreux cas, la simple adaptation de la profondeur d’anesthésie ou l’optimisation du remplissage vasculaire suffisent. Dans d’autres cas, il faudra recourir à des vasopresseurs à dose faible à modérée. Il n’existe aucun élément probant convaincant que l’administration de vasopresseurs à faible dose soit nocive. La prévention de l’hypotension postopératoire est beaucoup plus complexe, cependant une approche utile consiste à différer la mise en place des médicaments contre l’hypertension chronique jusqu’à ce qu’ils soient clairement nécessaires.
La pression artérielle, en particulier la prévention de l’hypotension, est un facteur modifiable qui peut réduire les complications cardiovasculaires. Dans l’attente des résultats d’essais fiables, des efforts raisonnables pour éviter l’hypotension périopératoire semblent prudents.
Daniel I. Sessler, MD, est le professeur et président Michael Cudahy du Département de recherche sur les issues, Institut d’anesthésiologie, Cleveland Clinic, Cleveland, Ohio, États-Unis.
L’auteur est consultant pour Edwards Lifesciences (Irvine, Californie), il siège aux comités consultatifs et a des parts au capital de Sensifree (Cupertino, Californie) et de Perceptive Medical (Newport Beach, Californie).
Documents de référence
- Li G, Warner M, Lang BH, et al. Epidemiology of anesthesia-related mortality in the United States, 1999-2005. Anesthesiology. 2009;110:759–765.
- Pearse RM, Moreno RP, Bauer P, et al. European Surgical Outcomes Study group for the Trials groups of the European Society of Intensive Care M, the European Society of A: mortality after surgery in Europe: a 7 day cohort study. Lancet. 2012;380:1059–1065.
- Bartels K, Karhausen J, Clambey ET, et al. Perioperative organ injury. Anesthesiology. 2013;119:1474–1489.
- The Vascular Events In Noncardiac Surgery Patients Cohort Evaluation (VISION) Study Investigators: association between postoperative troponin levels and 30-day mortality among patients undergoing noncardiac surgery. JAMA. 2012;307:2295–2304.
- Vascular Events in Noncardiac Surgery Patients Cohort Evaluation Study Investigators: association between complications and death within 30 days after noncardiac surgery. CMAJ. 2019;191:E830–E837.
- Devereaux PJ, Sessler DI. Cardiac complications in patients undergoing major noncardiac surgery. N Engl J Med. 2015;373:2258–2269.
- Thygesen K, Alpert JS, Jaffe AS, et al. Fourth Universal Definition of Myocardial Infarction (2018). J Am Coll Cardiol. 2018;72:2231–2264. doi: 10.1016/j.jacc.2018.08.1038. Epub 2018 Aug 25.
- The Vascular Events in Noncardiac Surgery Patients Cohort Evaluation (VISION) Study Investigators: association between complications and death within 30 days after noncardiac surgery. Can Med Assoc J. 2019;191:E830–E837.
- Beattie WS, Wijeysundera DN, Chan MTV, et al. Anzca Clinical Trials Network for the ENIGMA-II Investigators: implication of major adverse postoperative events and myocardial injury on disability and survival: a planned subanalysis of the ENIGMA-II trial. Anesth Analg. 2018;127:1118–1126.
- Eikelboom JW, Connolly SJ, et al. Rivaroxaban with or without aspirin in stable cardiovascular disease. N Engl J Med. 2017;377:1319–1330.
- Devereaux PJ, Duceppe E, Guyatt G, et al. Dabigatran in patients with myocardial injury after non-cardiac surgery (MANAGE): an international, randomised, placebo-controlled trial. Lancet. 2018;391:2325–2334.
- Writing Committee for the Vision Study Investigators, Devereaux PJ, Biccard BM, Sigamani A, et al. Association of postoperative high-sensitivity troponin levels with myocardial injury and 30-day mortality among patients undergoing noncardiac surgery. JAMA. 2017;317:1642–1651.
- Duceppe E, Borges FK, Tiboni M, et al. Association between high-sensitivity troponin I and major cardiovascular events after non-cardiac surgery (abstrract). J Am Coll Cardiol. 2020;75.
- Devereaux PJ, Yang H, Yusuf S, et al. Effects of extended-release metoprolol succinate in patients undergoing non-cardiac surgery (POISE trial): a randomised controlled trial. Lancet. 2008;371:1839–1847.
- Myles PS, Leslie K, Chan MT, et al. Anzca Trials Group for the ENIGMA-II investigators: the safety of addition of nitrous oxide to general anaesthesia in at-risk patients having major non-cardiac surgery (ENIGMA-II): a randomised, single-blind trial. Lancet. 2014;384:1446–1454.
- Devereaux PJ, Sessler DI, Leslie K, et al. Poise-2 Investigators: clonidine in patients undergoing noncardiac surgery. N Engl J Med. 2014;370:1504–1513.
- Devereaux PJ, Mrkobrada M, Sessler DI, et al. Poise-2 Investigators: aspirin in patients undergoing noncardiac surgery. N Engl J Med. 2014;370:1494–1503.
- Salmasi V, Maheshwari K, Yang D, et al. Relationship between intraoperative hypotension, defined by either reduction from baseline or absolute thresholds, and acute kidney and myocardial injury after noncardiac surgery: a retrospective cohort analysis. Anesthesiology. 2017;126:47–65.
- Mascha EJ, Yang D, Weiss S, Sessler DI. Intraoperative mean arterial pressure variability and 30-day mortality in patients having noncardiac surgery. Anesthesiology. 2015;123:79–91.
- Sessler DI, Meyhoff CS, Zimmerman NM, et al. Period-dependent associations between hypotension during and for four days after noncardiac surgery and a composite of myocardial infarction and death: a substudy of the POISE-2 trial. Anesthesiology. 2018;128:317–327.
- Liem VGB, Hoeks SE, Mol K, et al. Postoperative hypotension after noncardiac surgery and the association with myocardial injury. Anesthesiology. 2020;133:510–522.
- Roshanov PS, Rochwerg B, Patel A, et al. Withholding versus continuing angiotensin-converting enzyme inhibitors or angiotensin II receptor blockers before noncardiac surgery: an analysis of the vascular events in noncardiac surgery patients cohort evaluation prospective cohort. Anesthesiology. 2017;126:16–27.
- Bijker JB, Gelb AW. Review article: The role of hypotension in perioperative stroke. Can J Anaesth. 2013;60:159–167.
- Bijker JB, Persoon S, Peelen LM, et al. Intraoperative hypotension and perioperative ischemic stroke after general surgery: A nested case-control study. Anesthesiology. 2012;116:658–664.
- Sun LY, Chung AM, Farkouh ME, et al. Defining an intraoperative hypotension threshold in association with stroke in cardiac surgery. Anesthesiology. 2018;129:440–447.
- Hsieh JK, Dalton JE, Yang D, et al. The association between mild intraoperative hypotension and stroke in general surgery patients. Anesth Analg. 2016;123:933–939.
- Turan A, Cohen B, Rivas E, et al. Association between postoperative haemoglobin and myocardial injury after noncardiac surgery: a retrospective cohort analysis. Br J Anaesth. 2021;126:94–101.
- Turan A, Rivas E, Devereaux PJ, et al. Association between postoperative haemoglobin concentrations and composite of non-fatal myocardial infarction and all-cause mortality in noncardiac surgical patients: post hoc analysis of the POISE-2 trial. Br J Anaesth. 2021;126:87–93.
- Ruetzler K, Yilmaz HO, Turan A, et al. Intra-operative tachycardia is not associated with a composite of myocardial injury and mortality after noncardiac surgery: A retrospective cohort analysis. Eur J Anaesthesiol. 2019;36:105–113.
- Sun Z, Sessler DI, Dalton JE, et al. Postoperative hypoxemia is common and persistent: a prospective blinded observational study. Anesth Analg. 2015;121:709–715.
- Kheterpal S, Tremper KK, Heung M, et al. Development and validation of an acute kidney injury risk index for patients undergoing general surgery: results from a national data set. Anesthesiology. 2009;110:505–515.
- Walsh M, Garg AX, Devereaux PJ, et al. The association between perioperative hemoglobin and acute kidney injury in patients having noncardiac surgery. Anesth Analg. 2013;117:924–931.
- Whitlock EL, Braehler MR, Kaplan JA, et al. Derivation, validation, sustained performance, and clinical impact of an electronic medical record-based perioperative delirium risk stratification tool. Anesth Analg. 2020;131:1901–1910.
- Walsh M, Devereaux PJ, Garg AX, et al. Relationship between intraoperative mean arterial pressure and clinical outcomes after noncardiac surgery: toward an empirical definition of hypotension. Anesthesiology. 2013;119:507–515.
- Sun LY, Wijeysundera DN, Tait GA, et al. Association of intraoperative hypotension with acute kidney injury after elective noncardiac surgery. Anesthesiology. 2015;123:515–523.
- O’Connor ME, Hewson RW, Kirwan CJ, et al. Acute kidney injury and mortality 1 year after major non-cardiac surgery. Br J Surg. 2017;104:868–876.
- Turan A, Cohen B, Adegboye J, et al. Mild acute kidney injury after noncardiac surgery is associated with long-term renal dysfunction: a retrospective cohort study. Anesthesiology. 2020;132:1053–1061.
- Hakim SM, Othman AI, Naoum DO. Early treatment with risperidone for subsyndromal delirium after on-pump cardiac surgery in the elderly: a randomized trial. Anesthesiology. 2012;116:987–997.
- Maldonado JR, Wysong A, van der Starre PJ, et al. Dexmedetomidine and the reduction of postoperative delirium after cardiac surgery. Psychosomatics. 2009;50:206–217.
- Royse CF, Saager L, Whitlock R, et al. Impact of methylprednisolone on postoperative quality of recovery and delirium in the Steroids in Cardiac Surgery Trial: a randomized, double-blind, placebo-controlled substudy. Anesthesiology. 2017;126:223–233.
- Shehabi Y, Grant P, Wolfenden H, et al. Prevalence of delirium with dexmedetomidine compared with morphine based therapy after cardiac surgery: a randomized controlled trial (DEXmedetomidine COmpared to Morphine-DEXCOM Study). Anesthesiology. 2009;111:1075–1084.
- Turan A, Duncan A, Leung S, et al. Dexmedetomidine for reduction of atrial fibrillation and delirium after cardiac surgery (DECADE): a randomised placebo-controlled trial. Lancet. 2020;396:177–185.
- Gou RY, Hshieh TT, Marcantonio ER, et al. One-year medicare costs associated with delirium in older patients undergoing major elective surgery. JAMA Surg. 2021;156:430–442.
- Hayhurst CJ, Pandharipande PP, Hughes CG. Intensive care unit delirium: a review of diagnosis, prevention, and treatment. Anesthesiology. 2016;125:1229–1241.
- Daiello LA, Racine AM, Yun Gou R, et al. Postoperative delirium and postoperative cognitive dysfunction: overlap and divergence. Anesthesiology. 2019;131:477–491.
- Pan H, Liu C, Ma X, et al. Perioperative dexmedetomidine reduces delirium in elderly patients after non-cardiac surgery: a systematic review and meta-analysis of randomized-controlled trials. Can J Anaesth. 2019;66:1489–1500.
- Ono M, Arnaoutakis GJ, Fine DM, et al. Blood pressure excursions below the cerebral autoregulation threshold during cardiac surgery are associated with acute kidney injury. Crit Care Med. 2013;41:464–471.
- Ono M, Brady K, Easley RB, et al. Duration and magnitude of blood pressure below cerebral autoregulation threshold during cardiopulmonary bypass is associated with major morbidity and operative mortality. J Thorac Cardiovasc Surg. 2014;147:483–489.
- Feng X, Hu J, Hua F, et al. The correlation of intraoperative hypotension and postoperative cognitive impairment: a meta-analysis of randomized controlled trials. BMC Anesthesiol. 2020;20:193.
- Maheshwari K, Ahuja S, Khanna AK, et al. Association between perioperative hypotension and delirium in postoperative critically ill patients: a retrospective cohort analysis. Anesth Analg. 2020;130:636–643.
- Hori D, Brown C, Ono M, et al. Arterial pressure above the upper cerebral autoregulation limit during cardiopulmonary bypass is associated with postoperative delirium. Br J Anaesth. 2014;113:1009–1017.
- Hirsch J, DePalma G, Tsai TT, et al. Impact of intraoperative hypotension and blood pressure fluctuations on early postoperative delirium after non-cardiac surgery. Br J Anaesth. 2015;115:418–426.
- Wesselink EM, Kappen TH, van Klei WA, et al. Intraoperative hypotension and delirium after on-pump cardiac surgery. Br J Anaesth. 2015;115:427–433.
- Langer T, Santini A, Zadek F, et al. Intraoperative hypotension is not associated with postoperative cognitive dysfunction in elderly patients undergoing general anesthesia for surgery: results of a randomized controlled pilot trial. J Clin Anesth. 2019;52:111–118.
- Brown CH 4th, Neufeld KJ, Tian J, et al. Effect of targeting mean arterial pressure during cardiopulmonary bypass by monitoring cerebral autoregulation on postsurgical delirium among older patients: A nested randomized clinical trial. JAMA Surg. 2019;154:819–826.
- Brown CH 4th, Probert J, Healy R, et al. Cognitive decline after delirium in patients undergoing cardiac surgery. Anesthesiology. 2018;129:406–416.
- Mrkobrada M, Chan MTV, Cowan D, et al. Perioperative covert stroke in patients undergoing non-cardiac surgery (NeuroVISION): a prospective cohort study. Lancet. 2019; 394:1022–1029.
- Sessler DI, Khan MZ, Maheshwari K, et al. Blood pressure management by anesthesia professionals: evaluating clinician skill from electronic medical records. Anesth Analg. 2021;132:946–956.
- Maheshwari K, Turan A, Mao G, et al. The association of hypotension during non-cardiac surgery, before and after skin incision, with postoperative acute kidney injury: a retrospective cohort analysis. Anaesthesia. 2018;73:1223–1228.
- Naylor AJ, Sessler DI, Maheshwari K, et al. Arterial catheters for early detection and treatment of hypotension during major noncardiac surgery: a randomized trial. Anesth Analg. 2020;131:1540–1550.
- Maheshwari K, Khanna S, Bajracharya GR, et al. A randomized trial of continuous noninvasive blood pressure monitoring during noncardiac surgery. Anesth Analg. 2018;127:424–431.
- Davies SJ, Vistisen ST, Jian Z, et al. Ability of an arterial waveform analysis-derived hypotension prediction index to predict future hypotensive events in surgical patients. Anesth Analg. 2020;130:352–329.
- Wijnberge M, Geerts BF, Hol L, et al. Effect of a machine learning-derived early warning system for intraoperative hypotension vs standard care on depth and duration of intraoperative hypotension during elective noncardiac surgery: the HYPE randomized clinical trial. JAMA. 2020;323:1052–1060.
- Maheshwari K, Shimada T, Yang D, et al. Hypotension prediction index for prevention of hypotension during moderate- to high-risk noncardiac surgery. Anesthesiology. 2020;133:1214–1222.
- Farag E, Makarova N, Argalious M, et al. Vasopressor infusion during prone spine surgery and acute renal injury: a retrospective cohort analysis. Anesth Analg. 2019;129:896–904.
- Ducrocq N, Kimmoun A, Furmaniuk A, et al. Comparison of equipressor doses of norepinephrine, epinephrine, and phenylephrine on septic myocardial dysfunction. Anesthesiology. 2012;116:1083–1091.
- Morelli A, Ertmer C, Rehberg S, et al. Phenylephrine versus norepinephrine for initial hemodynamic support of patients with septic shock: a randomized, controlled trial. Crit Care. 2008;12:R143.
- Reinelt H, Radermacher P, Kiefer P, et al. Impact of exogenous beta-adrenergic receptor stimulation on hepatosplanchnic oxygen kinetics and metabolic activity in septic shock. Crit Care Med. 1999;27:325–331.
- Dellinger RP, Levy MM, Carlet JM, et al. International Surviving Sepsis Campaign Guidelines C, American Association of Critical-Care N, American College of Chest P, American College of Emergency P, Canadian Critical Care S, European Society of Clinical M, Infectious D, European Society of Intensive Care M, European Respiratory S, International Sepsis F, Japanese Association for Acute M, Japanese Society of Intensive Care M, Society of Critical Care M, Society of Hospital M, Surgical Infection S, World Federation of Societies of I, Critical Care M: Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock: 2008. Crit Care Med. 2008;36:296–327.
- Mets B: Should norepinephrine, rather than phenylephrine, be considered the primary vasopressor in anesthetic practice? Anesth Analg. 2016;122:1707–1714.
- Owen VS, Rosgen BK, Cherak SJ, et al. Adverse events associated with administration of vasopressor medications through a peripheral intravenous catheter: a systematic review and meta-analysis. Crit Care. 2021;25:146.
- Pancaro C, Shah N, Pasma W, et al. Risk of major complications after perioperative norepinephrine infusion through peripheral intravenous lines in a multicenter study. Anesth Analg. 2019;131:1060–1065.
- Turan A, Chang C, Cohen B, et al. Incidence, severity, and detection of blood pressure perturbations after abdominal surgery: a prospective blinded observational study. Anesthesiology. 2019;130:550–559.
- Futier E, Lefrant JY, Guinot PG, et al. Effect of individualized vs standard blood pressure management strategies on postoperative organ dysfunction among high-risk patients undergoing major surgery: a randomized clinical trial. JAMA. 2017;318:1346–1357.

