INTRODUCTION
Les blocs nerveux périphériques (PNB) sont des alternatives sûres et efficaces ou complètent une anesthésie générale. Ils peuvent améliorer le contrôle de la douleur pendant et après la chirurgie, évitant ainsi de nombreux effets secondaires des opiacés systémiques. Les PNB peuvent également permettre d’améliorer la satisfaction des patients, réduire la consommation de ressources et peuvent être plus bénéfiques pour l’environnement en réduisant l’utilisation de gaz anesthésiques et autres médicaments.
L’utilisation des PNB a augmenté au fil du temps. Une étude du Registre national des résultats cliniques en anesthésie (National Anesthesia Clinical Outcomes Registry) a analysé les données de 12 911 056 chirurgies ambulatoires entre 2010 et 2015, concluant à une hausse marquée du nombre total de PNB.1 Avec l’augmentation de l’utilisation des blocs nerveux périphériques aux États-Unis, nous souhaitons étudier les questions de sécurité liées à ces procédures. En particulier, nous étudierons la sécurité des blocs nerveux en termes de lésions nerveuses, reconnaissance et traitement de la toxicité systémique des anesthésiques locaux (TSAL) et la réalisation appropriée des time-outs par les professionnels de santé, afin d’éviter des blocs du mauvais côté.
UTILISATION DES BLOCS NERVEUX PÉRIPHÉRIQUES GUIDÉS PAR ULTRASONS POUR AMÉLIORER LA SÉCURITÉ DES PATIENTS
Les PNB guidés par ultrasons sont rapidement devenus la méthode privilégiée par de nombreux anesthésistes. L’utilisation de l’échoguidage par rapport à la neurostimulation périphérique peut permettre une amélioration marquée de la réussite du bloc, la moindre nécessité d’une analgésie en urgence, des douleurs réduites pendant la réalisation du bloc et des nombres plus faibles de pontions vasculaires et pleurales. Bien qu’il n’existe pas de données convaincantes prouvant que l’anesthésie régionale guidée par ultrasons réduit le risque de pneumothorax pour certains blocs tels que les blocs paravertébraux et supra-claviculaires, la possibilité de visualiser la plèvre peut apporter la confirmation que l’espace pleural n’a pas été pénétré.2
Il a été suggéré que le risque de lésions nerveuses pourrait être encore réduit en utilisant les ultrasons pour visualiser directement l’aiguille et le nerf ciblé. Toutefois, les articles publiés ne corroborent pas l’argument que les blocs guidés par ultrasons réduisent l’incidence de symptômes neurologiques postopératoires par rapport à d’autres techniques, telles que la neurostimulation périphérique. La principale source des lésions neurologiques médiées est probablement des lésions mécaniques du fascicule et/ou l’injection d’un anesthésique local dans le fascicule, causant une dégénération myélinique et axonale. Heureusement, la plupart des symptômes neurologiques après un PNB sont transitoires. L’incidence de lésions nerveuses à long terme signalée dans les 3 plus grands registres est de 4 sur 10 000 blocs nerveux périphériques, chiffre semblable à l’incidence historique associée aux blocs guidés par neurostimulation périphérique.2 Une raison de cette absence de différence est peut-être due en partie à la qualité de l’équipement à ultrasons et à la compétence du médecin chargé de la procédure à identifier le nerf ciblé. Il arrive que les opérateurs ne visualisent pas correctement la pointe de l’aiguille et interprètent mal les artéfacts environnants. Le mouvement de l’aiguille et/ou l’hydrodissection peuvent ne pas garantir l’absence de contact entre l’aiguille et le nerf ou l’injection vasculaire d’anesthésiques locaux. Dans un autre registre, l’incidence d’évènements indésirables dans toutes les anesthésies régionales périphériques était de 1,8 sur 1000 blocs pour les symptômes neurologiques postopératoires durant plus de 5 jours, mais de seulement 0,9 sur 1000 blocs pour les symptômes neurologiques postopératoires durant plus de 6 mois.3 Il faut remarquer que les patients présentant une neuropathie existante peuvent être plus à risque d’un dysfonctionnement neurologique postopératoire. Il est d’une importance capitale pour la sécurité du patient d’éviter une injection intraneurale.4
En revanche, l’utilisation des ultrasons réduit considérablement le risque de TSAL. Une étude récente a permis de fournir des données probantes solides indiquant que l’utilisation des ultrasons peut jouer un rôle dans la réduction de l’incidence des TSAL.5 Le guidage par ultrasons permet de guider l’aiguille en temps réel pour éviter les lésions vasculaires et l’injection intravasculaire consécutive d’un anesthésique local. L’utilisation des ultrasons minimise l’incidence des TSAL (2,7 sur 10 000 cas), toutefois il est impératif de porter une attention toute particulière à cette possibilité et les médecins doivent surveiller de près leur apparition.6
TOXICITÉ SYSTÉMIQUE D’UNE ANESTHÉSIE LOCALE
En 1998, Weinberg et ses collègues ont publié la première étude de cas suggérant qu’une injection d’émulsion d’huile de soja, qui était généralement utilisée comme solution de nutrition parentérale totale, pouvait éviter (par traitement préliminaire) ou inverser un arrêt cardiaque causé par une surdose de bupivacaïne chez le rat anesthésié intact.7 Ce n’est que près de vingt années plus tard qu’un signalement de TSAL a été publié, concernant un patient ayant subi un PNB pour une chirurgie de l’épaule, et qui a ensuite fait un arrêt cardiaque. Le patient n’a pas réagi aux efforts standard de réanimation d’une durée d’environ 20 minutes, mais ses signes vitaux sont redevenus normaux peu après l’administration d’un bolus de 100 ml d’émulsion lipidique. Le patient s’est complètement rétabli sans déficits neurologiques ni séquelles cardiovasculaires.8
En 2010, l’American Society of Regional Anesthesia and Pain Medicine a publié sa check-list pour les TSAL, qui a été révisée en 2012, 2017 et le plus récemment en 2020.9 (Figure 1). La dernière révision de la check-list était liée aux retours d’information des simulations et des utilisateurs, mettant en lumière le fait que les différences entre les efforts de réanimation en cas de TSAL et la réanimation cardiaque avancée (ACLS) n’étaient pas soulignées. Les études réalisées sur les animaux ont démontré que certains des médicaments standard utilisés pour l’ACLS, tels que la dose usuelle d’épinéphrine et de vasopressine, aggravaient les résultats en cas de TSAL.10,11 Dans les simulations, lorsque les sujets choisissaient d’utiliser les check-lists des TSAL et également de l’ACLS, la confusion et les faux-pas entraînaient des retards, voire des erreurs de traitement. Des avertissements étaient notés au début des check-lists précédentes, mais ils n’ont pas permis d’éliminer les erreurs. La reconception de 2020 avait pour but d’intégrer un symbole triangulaire standard de mise en garde pour mettre l’accent sur les différences sur la check-list des TSAL et la réanimation ACLS. La mise à jour de 2020 a également simplifié le dosage de l’émulsion lipidique pour les patients de plus de 70 kg à un seul et unique bolus de 100 ml, suivi d’une perfusion, plutôt que l’emploi d’un calcul à partir du poids.9
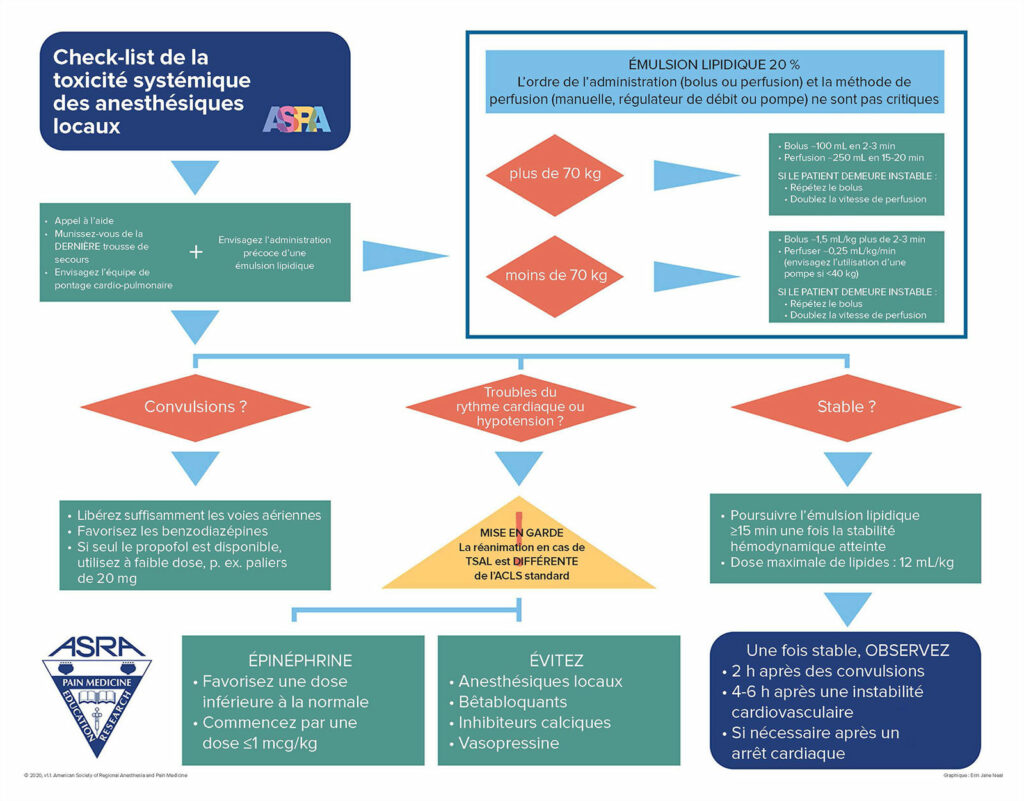
Figure 1. Check-list de la toxicité systémique des anesthésiques locaux.
Utilisée avec l’autorisation de la Société américaine d’anesthésie régionale et de traitement de la douleur (American Society of Regional Anesthesia and Pain Medicine).
LE DANGER DES BLOCS NERVEUX PÉRIPHÉRIQUES SOUS SÉDATION
Un demi-siècle s’est écoulé depuis qu’une étude de cas a attiré l’attention de tous sur le risque de placer une péridurale thoracique sur un patient anesthésié.12 Le patient a souffert une lésion médullaire après quatre tentatives de placement de la péridurale. Toutefois, les publications relatives à la population adulte qui fournissent des recommandations concernant la sécurité ou le risque de l’utilisation de blocs régionaux chez les patients anesthésiés sont rares. Dans la population pédiatrique, l’utilisation de blocs régionaux chez des patients anesthésiés est considérée comme sûre. Ces données sont issues du Pediatric Regional Anesthesia Network, un consortium de recherche pluri-institutionnel qui a créé un registre de plus de 50 000 blocs régionaux chez des enfants de moins de 18 ans.13 En revanche, chez les patients adultes, la pratique principale, qui n’est fondée sur aucune preuve scientifique rigoureuse, consiste à utiliser des anesthésiques régionaux avant l’induction de l’anesthésie générale. La sédation peut améliorer la sécurité et la réussite de l’utilisation du bloc et se conclure par une meilleure satisfaction du patient en améliorant les conditions opératoires pour les anesthésistes qui réalisent le bloc.14 Il faudra des études supplémentaires pour déterminer les risques et les avantages réels de l’utilisation des PNB chez des adultes anesthésiés.
PRÉVENTION DES BLOCS DU MAUVAIS CÔTÉ
Les blocs du mauvais côté sont des « évènements qui ne devraient jamais arriver ou Never Events » qui arrivent quand même
On considère que les blocs du mauvais côté sont des « évènements qui ne devraient jamais arriver ou Never Events » mais qui arrivent quand même à un taux de 7,5 sur 10 000 procédures.15 Le terme « Never Event » a été introduit pour la première fois en 2001 par Ken Kizer, MD, ancien PDG du National Quality Forum (NQF), en référence aux erreurs médicales monstrueuses qui ne devraient jamais survenir.16 Au fil des années, l’utilisation du terme s’est élargie pour désigner des évènements indésirables qui sont sans équivoque, graves et généralement évitables. Depuis l’élaboration de la liste des « Never Events » en 2002, elle a été révisée de nombreuses fois et elle comprend désormais 29 « évènements graves à signaler » regroupés en 7 catégories.17
Certaines caractéristiques sont identifiées dans la plupart des blocs du mauvais côté (Tableau 1). Avant de débuter le bloc nerveux, le patient et l’infirmier(ière) confirment visuellement tous les deux l’endroit correct de la procédure en respectant les normes spécifiques à l’établissement, ce qui peut inclure la pose d’un bracelet portant la mention « oui » du côté correspondant à la chirurgie ou un marquage clair par le chirurgien ou le médecin réalisant la procédure. L’implication du patient dans la démarche avant qu’il ne soit sédaté ou anesthésié permet de réduire le nombre d’erreurs et peut améliorer la satisfaction des patients, qui ont le sentiment d’être des acteurs de la procédure et ont plus confiance dans leurs médecins.14
Tableau 1 : Facteurs qui contribuent à un bloc du mauvais côté15
| Caractéristiques des blocs du mauvais côté |
| Absence de vérification préopératoire du site |
| Absence de marquage adéquat de la zone par le chirurgien |
| Time-out avant l’anesthésie précipité, insuffisant ou absent |
| Distractions |
| Changements de position du patient |
| Changements de programme |
| Mauvaise communication |
Les médecins qui réalisent le bloc régional doivent discuter de la procédure opératoire/invasive avec le patient avant d’administrer l’anesthésie/la sédation modérée. Le patient doit confirmer verbalement que la procédure et le site chirurgical sont corrects et la discussion ainsi que la confirmation verbale du patient doivent être documentées dans le formulaire de consentement. Les obstacles à la communication (p. ex. déficits visuels et auditifs, un patient non anglophone, ainsi que l’état émotionnel du patient) doivent être pris en compte par tous les intervenants afin que le patient puisse participer entièrement aux discussions préopératoires. Les mesures prises pour tenir compte des obstacles à la communication doivent être documentées dans le dossier médical.
Toutes les communications pertinentes, y compris le formulaire de consentement, l’historique des maladies présentes et les données de diagnostic, doivent être vérifiées par l’infirmier(ière) préprocédural(e)/l’équipe chargée de réaliser la procédure. En cas d’écarts ou d’incertitudes, l’infirmier(ière) préprocédural(e)/l’équipe réalisant la procédure devra appeler le chirurgien pour clarification avant de démarrer la procédure.
Juste avant de réaliser le bloc nerveux périphérique, le médecin chargé de la procédure devra mettre en place le « Protocole universel » et respecter un « time-out » avant la procédure (Figure 2). Le « time-out » doit impérativement intervenir juste avant l’incision ou le début de la procédure. Le « time-out » doit être réalisé à l’endroit où la procédure aura lieu et doit impliquer dès le départ les membres immédiats de l’équipe chargée de la procédure, y compris la personne qui la réalise, l’infirmière de liaison et les autres participants actifs impliqués dans la procédure.
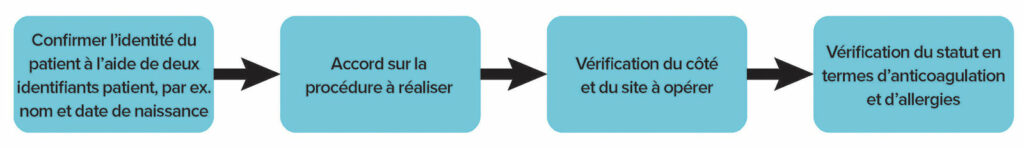
Figure 2. Flux de travail de la procédure de timeout pour la réalisation d’un bloc nerveux périphérique.
Au minimum, il convient de prendre les mesures suivantes avant de réaliser un bloc régional :
Lorsque l’anesthésiste est sur le point de commencer le bloc régional, il ou elle doit confirmer que le site est marqué par la personne réalisant le bloc en utilisant la même méthode que celle décrite ci-dessus. Il s’agit de la pratique que nous appliquons, mais d’autres établissements ont mis en place des protocoles différents.
CONCLUSION
En résumé, l’anesthésie régionale est un complément sûr ou une alternative à une anesthésie générale qui peut améliorer la satisfaction du patient et réduire l’usage des opiacés ainsi que leurs effets secondaires. Alors que les blocs nerveux sont déjà assez sûrs, il est essentiel de veiller à une sécurité maximale tout en administrant des soins excellents. Au fur et à mesure que l’utilisation de l’anesthésie régionale se répand, il est impératif que nos blocs régionaux soient aussi sûrs que possible, en envisageant le guidage par ultrasons s’il est disponible, en comprenant comment reconnaître les TSAL et la réanimation et en exécutant les check-lists correctes avant les procédures afin d’éviter les blocs du mauvais côté.
Christina Ratto, MD, est professeure clinique assistante à la Keck School of Medicine, Los Angeles, Californie.
Joseph Szokol, MD, JD, MBA, est professeur clinique à la Keck School of Medicine, Los Angeles, Californie.
Paul Lee, MD, MS est professeur clinique assistant à la Keck School of Medicine, Los Angeles, Californie.
Les auteurs ne signalent aucun conflit d’intérêts.
DOCUMENTS DE RÉFÉRENCE
- Gabriel RA, Ilfeld BM. Use of regional anesthesia for outpatient surgery within the United States: a prevalence study using a nationwide database. Anesth Analg. 2018;126:2078–84. PMID: 28922231.
- Neal JM, Brull R, Horn JL, et al. The Second American Society of Regional Anesthesia and Pain Medicine evidence-based medicine assessment of ultrasound-guided regional anesthesia: executive summary. Reg Anesth Pain Med. 2016;41:181–194. PMID: 26695878.
- Sites BD, MD, Taenzer AH, Herrick MD. Incidence of local anesthetic systemic toxicity and postoperative neurologic symptoms associated with 12,668 ultrasound-guided nerve blocks an analysis from a prospective clinical registry. Reg Anesth Pain Med. 2012;37:478–482. PMID: 22705953.
- Brull R, McCartney C, Chan V. El-Beheiry H. Neurological complications after regional anesthesia: contemporary estimates of risk. Anesth Analg. 2007;104:965–975. PMID: 17377115.
- Barrington MJ, Kluger R. Ultrasound guidance reduces the risk of local anesthetic systemic toxicity following peripheral nerve blockade. Reg Anesth Pain Med. 2013; 38:289-99. PMID: 23788067.
- El-Boghdadly K, Pawa A, Chin KJ. Local anesthetic systemic toxicity: current perspectives. Local Reg Anesth. 2018;11:35–44. Published online 2018 Aug 8. PMID: 30122981.
- Weinberg GL, VadeBoncouer T, Ramaraju GA, et al. Pretreatment or resuscitation with a lipid infusion shifts the dose-response to bupivacaine-induced asystole in rats. Anesthesiology. 1998;88:1071–1075. PMID: 9579517.
- Rosenblatt MA, Abel M, Fischer GW, et al. Successful use of a 20% lipid emulsion to resuscitate a patient after a presumed bupivacaine-related cardiac arrest. Anesthesiology. 2006;105:217–218. PMID: 16810015.
- Neal JM, Neal EJ, Weinberg GL. American Society of Regional Anesthesia and Pain Medicine local anesthetic systemic toxicity checklist: 2020 version. Reg Anesth Pain Med. 2021;46:81–82. PMID: 33148630.
- Hiller DB, Di Gregorio G, Ripper R, et al. Epinephrine impairs lipid resuscitation from bupivacaine overdose. Anesthesiology. 2009;111:498–505. PMID: 19704251.
- Di Gregorio G, Schwartz D, Ripper R, et al. Lipid emulsion is superior to vasopressin in a rodent model of resuscitation from toxin-induced cardiac arrest. Crit Care Med. 2009;37: 993–999. PMID: 19237909.
- Bromage PR, Benumof JL. Paraplegia following intracord injection during attempted epidural anesthesia under general anesthesia. Reg Anesth Pain Med. 1998;23:104–107. PMID: 9552788.
- Taenzer AH, Walker BJ, Bosenberg AT, et al. Asleep versus awake: does it matter? Pediatric regional block complications by patient state: a report from the Pediatric Regional Anesthesia Network. Reg Anesth Pain Med. 2014;39: 279–283. PMID: 24918334.
- Kubulus C, Schmitt KC, Albert N, et al. Awake, sedated or anaesthetised for regional anaesthesia block placements? A retrospective registry analysis of acute complications and patient satisfaction in adults. Eur J Anaesthl. 2016;33:715–724. PMID: 27355866.
- Barrington MJ, Uda Y, Pattullo SJ, Sites BD. Wrong-site regional anesthesia: review and recommendations for prevention? Curr Opin Anesthesiol. 2015;28:670–684. PMID: 26539787.
- Kizer KW, Stegun MB. Serious reportable adverse events in health care. In: Henriksen K, Battles JB, Marks ES, et al., eds. Advances in patient safety: from research to implementation (volume 4: programs, tools, and products). Advances in Patient Safety. Rockville, 2005:339–352.
- Agency for Healthcare Research and Quality. Patient Safety Network. Never events.https://psnet.ahrq.gov/primer/never-events Accessed December 13, 2023.


 Issue PDF
Issue PDF