La eliminación de una lesión aguda de riñón (AKI) después de una artroplastia total (TJA) programada es posible. Una iniciativa del centro quirúrgico perioperatorio (PSH) dirigida por un anestesista dio lugar a una reducción sostenida de una complicación posoperatoria importante.
 La Sociedad Americana de Anestesiólogos (ASA) define el centro quirúrgico perioperatorio (PSH) como “un modelo de atención en equipo creado por líderes de la ASA para ayudar a responder a las exigencias de un paradigma de atención médica que enfatiza la gratificación en los proveedores, la mejoría de la atención en salud de la población, la reducción de los costos y la satisfacción de los pacientes”. Un equipo de St. Luke’s University Health Network usó el modelo de atención del PSH para reducir la incidencia de lesión aguda de riñón (AKI) después de una artroplastia total (TJA) programada.
La Sociedad Americana de Anestesiólogos (ASA) define el centro quirúrgico perioperatorio (PSH) como “un modelo de atención en equipo creado por líderes de la ASA para ayudar a responder a las exigencias de un paradigma de atención médica que enfatiza la gratificación en los proveedores, la mejoría de la atención en salud de la población, la reducción de los costos y la satisfacción de los pacientes”. Un equipo de St. Luke’s University Health Network usó el modelo de atención del PSH para reducir la incidencia de lesión aguda de riñón (AKI) después de una artroplastia total (TJA) programada.
La AKI es una complicación conocida después de la artroplastia total. Las tasas recogidas en la bibliografía varían del 2 al 15 % para los casos programados.1 La incidencia de AKI puede estar poco documentada por varios factores. La falta de medición de la creatinina el primer día posoperatorio, la incoherencia en la medición de la excreción de orina después de la cirugía, la falta de reconocimiento de la AKI según los criterios de KDIGO2,3 y las diferencias institucionales en la codificación pueden contribuir a que no se declaren los casos. Un episodio de AKI después de cirugía puede tener implicaciones negativas a corto y largo plazo para los pacientes4 y generar un aumento de los costos para el sistema de atención médica.5,6
En 2016, se puso en marcha una iniciativa dirigida por el PSH para reducir la hipotensión y la AKI en nuestra población sometida a una TJA programada. Se reunió un equipo multidisciplinario de profesionales de anestesia, nefrólogos, traumatólogos, médicos hospitalarios de medicina interna, enfermeros, analistas de EPIC y un especialista en recursos de calidad. Se desarrolló y aplicó un protocolo con los siguientes aspectos (Tabla 1):
- Revisión de pacientes mediante nuestro Centro de Optimización Quirúrgica (SOC)
- Ajuste de medicamentos (enzima convertidora de la angiotensina [ACE]/antagonista de los receptores de la angiotensina [ARB]/antinflamatorios no esteroideos [NSAID]/diuréticos) y reemplazo perioperatorio estandarizado de líquidos
- Manejo estandarizado de la anestesia mediante el protocolo de recuperación mejorada después de la cirugía (ERAS)
- Suspensión de los medicamentos antihipertensores si la presión (BP) sistólica es de <130
- Aplicación de un protocolo de líquidos controlado por enfermería para permitir el tratamiento posoperatorio de la hipotensión (Tabla 2)
Tabla 1: Evaluación de riesgo de AKI del Centro de Optimización Quirúrgica
Tabla 2: Resumen del protocolo de enfermería para la hipotensión posoperatoria
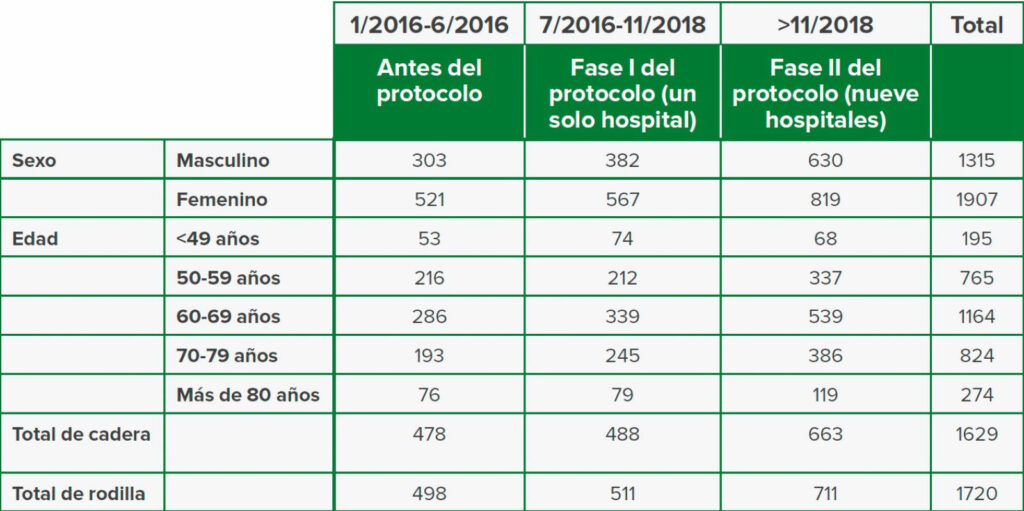
Se incluyeron todos los pacientes sometidos a una TJA (Tabla 3). No hubo ninguna excepción para los pacientes con enfermedad de riñón preexistente o cirugía de corrección. La hipotensión disminuyó del 12,7 % al 5,9 % y la AKI del 6,2 % al 1,2 %. Se publicó más información de nuestra iniciativa de PSH en The Journal of Arthroplasty en junio de 2018.7
Tabla 3: Características de los pacientes para la iniciativa del centro quirúrgico perioperatorio para reducir la incidencia de lesión aguda de riñón después de una artroplastia total
Desde esta publicación, se han hecho nuevas mejoras en el protocolo. Entre ellas, se incluyen:
- Mayor atención antes de la cirugía en pacientes de alto riesgo con consulta preoperatoria de nefrología para pacientes con una filtración glomerular (GFR) de <45 ml/min y adición de hidratación intravenosa ligera antes del procedimiento cuando se indique.
- Incorporación de un monitoreo continuo posoperatorio de los signos vitales, incluyendo la oximetría de pulso continua y la recolección automatizada de signos vitales, y su introducción en tiempo real en el expediente médico electrónico (EMR) mediante la tecnología Masimo Root y Patient SafetyNet (Irvine, CA).
- Mayor aprovechamiento del EMR para mejorar el cumplimiento del protocolo y los índices de detección temprana de anomalías significativas en los signos vitales (es decir, uso de “alertas inteligentes” y mejora de la resolución de los sistemas de puntuación de alerta temprana mediante la actualización del EMR con el monitoreo continuo y en tiempo real de los signos vitales).
Después de demostrar el éxito y la sostenibilidad en un único centro, el protocolo se extendió a otros hospitales de la red que hacían TJA. Esto incluyó a otros 21 cirujanos que hacían procedimientos en nueve hospitales. Después de la ampliación de la red, se observaron reducciones similares de la AKI perioperatoria respecto del valor inicial (del 5,9 % al 0,6 %) (Figura 1).
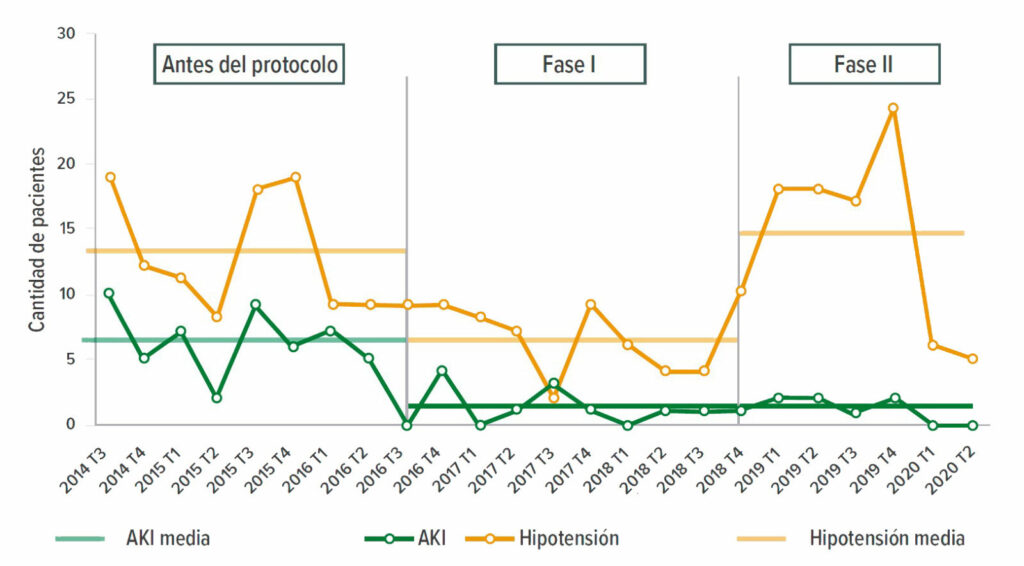
Figura 1: Cambios en la frecuencia de la hipotensión perioperatoria y la AKI antes y durante las dos fases de la iniciativa del PSH.
En general, la duración de la estancia en este período disminuyó de 2,75 días a 2,12 días (p <0,01). La tasa de mortalidad no varió, y los reingresos a 30 días se redujeron de un 3,8 a un 3,2 %, tendencia que no alcanzó significación estadística.
En nuestro Centro Hospitalario, siguiendo los criterios de KDIGO, hemos tenido un solo caso de AKI desde noviembre de 2018 en 1210 procedimientos consecutivos (primarios, de corrección o de enfermedad de riñón previa, todos incluidos) al momento de esta publicación.
En resumen, un enfoque multidisciplinario en el modelo del PSH ha dado lugar a reducciones sostenidas de una complicación significativa después de un procedimiento quirúrgico programado. También se ha creado conciencia sobre el valor de mejorar el monitoreo de los signos vitales y evitar la hipotensión en el entorno perioperatorio. Cada vez hay más pruebas que indican que la hipotensión perioperatoria es frecuente y está infradiagnosticada. La AKI posoperatoria puede ser un marcador de hipoperfusión global, y también se han reportado elevaciones de la troponina cardíaca en pacientes que se sometieron a una TJA.8 Además, la hipotensión es un factor de riesgo importante de lesión de miocardio perioperatoria después de una cirugía no cardíaca, que se ha asociado a peores resultados perioperatorios.9 Es factible que la ampliación del monitoreo de los signos vitales en tiempo real a otras poblaciones de pacientes con mayor riesgo de hipotensión perioperatoria y AKI pueda mejorar aún más la atención a los pacientes.10,11 Por último, aunque lo iniciaron los profesionales de la anestesia, el carácter colaborativo y multidisciplinario de este proyecto fue fundamental para su éxito. Estos resultados no podrían haberse alcanzado ni mantenido sin los aportes ni la colaboración de nuestros colegas médicos y no médicos. Este es un sello distintivo de un programa quirúrgico perioperatorio maduro y un modelo para futuros proyectos de mejora de los pacientes.
Aldo Carmona, MD es jefe de Anestesiología y vicepresidente sénior de Integración Clínica en St. Luke’s University Hospital, Bethlehem, PA.
Christopher Roscher, MD es jefe de sección de Anestesia Cardiotorácica en St. Luke’s University Hospital, Bethlehem, PA.
Daniel Herman, MD es director de Medicina Perioperatoria en St. Luke’s University Hospital, Bethlehem, PA.
Robert Gayner, MD es jefe de Nefrología y vicepresidente de Asuntos Médicos y Académicos en St. Luke’s University Hospital, Bethlehem, PA.
Ajith Malige, MD es residente (en el 5° año de su posgrado [PGY-V]) en el Departamento de Ortopedia de St. Luke’s University Hospital, Bethlehem, PA.
Brian Banas es estudiante de medicina en Geisinger Commonwealth School of Medicine, Scranton, PA.
Los autores no tienen conflictos de intereses.
Referencias
- Kimmel LA, Wilson S, Janardan JD, et al. Incidence of acute kidney injury following total joint arthroplasty: a retrospective review by RIFLE criteria. Clin Kidney J. 2014;7:546–551.
- Kidney Disease: Improving Global Outcomes (KDIGO) Acute Kidney Injury Work Group: KDIGO clinical practice guideline for acute kidney injury. Kidney Int Suppl. 2012;1:le138.
- Luo X, Jiang L, Du B, et al. A comparison of different diagnostic criteria of acute kidney injury in critically ill patients. Crit Care. 2014;18:R144.
- Coca SG, Yusuf B, Shlipak MG, et al. Long-term risk of mortality and other adverse outcomes after acute kidney injury: a systemic review and meta-analysis. Am J Kidney Dis. 2009;53:961–973.
- Che1tow GM, Burdick E, Honour M, Bonventre N, Bates DW. Acute kidney injury, mortality, length of stay and costs in hospitalized patients. JAM Soc Nephrol. 2005;16:336570.
- Silver SA, Chertow GM. The economic consequences of acute kidney injury. Nephron. 2017;137:297-301.
- Lands VW, Malige A, Carmona A, et al. Reducing hypotension and acute kidney injury in the elective total joint arthroplasty population: a multi-disciplinary approach. J Arthroplasty. 2018;33:1686–1692.
- Bass AR, Rodriquez T, Hyun G, et al. Myocardial ischemia after hip and knee arthroplasty: incidence and risk factors. Int Orthop. 2015;39:2011–2016.
- Sessler D, Khanna A. Perioperative myocardial injury and the contribution of hypotension. Intens Care Med. 20l8;44:811–822.
- Futier E, Lefrant JY, Guinot PG, et al. Effect of individualized vs. standard blood pressure management strategies on postoperative organ dysfunction among high-risk patients undergoing major surgery: a randomized clinical trial. JAMA. 2017;318:1346–1357.
- Wu X, Jian Z, Ying J, et al. Optimal blood pressure decreases acute kidney injury after gastrointestinal surgery in elderly hypertensive patients: a randomized study: optimal blood pressure reduces acute kidney injury. J Clin Anesth. 2017;43:77–83.


 Issue PDF
Issue PDF