Reproducción y modificación autorizadas. Lee LA, Caplan RA, Stephens LS, Posner KL, Terman GW, Voepel-Lewis T, Domino KB. Postoperative opioid-induced respiratory depression: a closed claims analysis. Anesthesiology 2015;122:659-65.
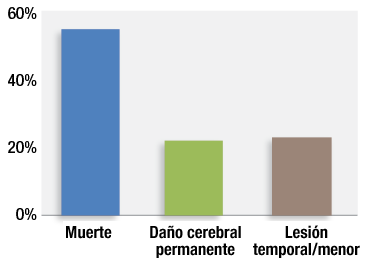
Figura 1. Gravedad de las lesiones en 92 reclamos relacionados con el deterioro ventilatorio posoperatorio inducido por opioides (Postoperative opioid-induced ventilatory impairment, OIVI) del Proyecto de Reclamos Cerrados.
El deterioro ventilatorio inducido por opioides (Postoperative Opioid-Induced Ventilatory Impairment, OIVI) es una causa prevenible de lesiones muy graves a los pacientes y en las últimas dos décadas muchas organizaciones han centrado sus iniciativas en este problema de seguridad de los pacientes. En este campo el progreso ha sido lento debido a que la baja incidencia de estos eventos ha dificultado la investigación de los resultados de intervenciones específicas. El Proyecto de Reclamos Cerrados de Anestesia utiliza un método para estudiar estos eventos poco frecuentes mediante la examinación rigurosa de los factores relacionados con los reclamos cerrados de mala práctica de anestesia de compañías de seguro de responsabilidad profesional que cubren aproximadamente a un tercio de los anestesiólogos de los Estados Unidos. El Proyecto de Reclamos Cerrados encontró 92 reclamos relacionados con el OIVI.1 Su metodología no identificó los casos en los que no hubo daño por un evento respiratorio ni se presentó ningún reclamo (p. ej., un rescate exitoso y rápido con naloxona), un diagnóstico equivocado que pudiera causar la muerte o una lesión cerebral, la gran cantidad de casos que nunca fueron procesados en un entorno médico-legal2 o los casos cubiertos por compañías de seguro de responsabilidad profesional fuera del Proyecto de Reclamos Cerrados. Más de tres cuartas partes de estos 92 reclamos de OIVI conllevaron la muerte o un daño cerebral permanente (Figura 1).1
Debido a la alta gravedad de las lesiones relacionadas con esta complicación, muchas organizaciones institucionales, sociedades profesionales y normativas han desarrollado directrices que recomiendan un mejor monitoreo posoperatorio de los pacientes de alto riesgo que reciben opioides en el período posoperatorio. Estas directrices incluyen intervenciones, tales como un aumento en las revisiones de evaluación en intervalos más cortos, capnografía continua y oximetría de pulso continua con alarmas centralizadas, y tecnologías más modernas, como el uso de impedancia eléctrica para monitorear la ventilación por minuto.3,4 Estas recomendaciones son un inicio lógico para abordar este problema complicado; sin embargo, identificar a todos los pacientes con un alto riesgo de OIVI no es una tarea fácil. Estudios publicados sobre este tema que utilizan diferentes metodologías y bases de datos han identificado diversos factores de riesgo de OIVI posoperatorio, que incluyen edad avanzada, sexo femenino, obesidad, bajo peso, apnea obstructiva del sueño, insuficiencia renal, enfermedad cardíaca, enfermedad pulmonar obstructiva crónica, enfermedad neurológica, diabetes, hipertensión, uso crónico de opioides preoperatorios y cirugía de las vías respiratorias.5-9 Dos tercios de los 92 reclamos relacionados con la depresión respiratoria inducida por opioides en el período posoperatorio en el Proyecto de Reclamos Cerrados se relacionaron con la obesidad, aunque el 63 % de los casos estaba relativamente saludable según la clasificación de Estado Físico 1-2 de ASA.1 Los polimorfismos genéticos específicos que alteran el metabolismo y el transporte de opiáceos cada vez más se identifican y se asocian con el OIVI.7,10,11 Claramente, muchos de estos factores de riesgo no serán diagnosticados, lo cual reduce la exactitud de cualquier lista de verificación de posibles factores de riesgo. Además, las complicaciones posoperatorias que pueden evolucionar, como sepsis, lesión renal aguda, neumonía o delirio, entre otras, podrían afectar la susceptibilidad al OIVI del paciente.
Los factores de riesgo exógenos de esta complicación dependen de las prácticas y las políticas de los profesionales e instituciones de atención médica, y son tan importantes como las afecciones preexistentes de los pacientes. Los factores de riesgo citados incluyen el uso de anestesia general comparado con la anestesia neuroaxial, la administración preoperatoria de oxicodona o gabapentina de acción prolongada, infusión continua de opioides en el período posoperatorio, administración simultánea de otros medicamentos sedantes no opioides, múltiples recetadores posoperatorios y educación inadecuada de los proveedores de atención médica respecto a las señales y los síntomas del OIVI.1,12-14 Estos factores de riesgo exógenos son altamente dependientes de las habilidades, la experiencia y la educación de cada uno de los profesionales involucrados en la atención médica del paciente, desde la admisión, además de la integración y la comunicación entre todos los proveedores de atención médica, especialmente, cuando se establecen nuevas directrices de atención médica. Los recursos institucionales, como las proporciones de asignación de personal de enfermería a pacientes en las habitaciones, la educación continua de los proveedores de todos los niveles sobre las señales y los síntomas del OIVI, el ingreso computarizado de pedidos, el monitoreo electrónico mejorado con alarmas centralizadas y las políticas institucionales que rodean el manejo del dolor, son otras variables significativas que pueden influir en la incidencia de esta complicación.
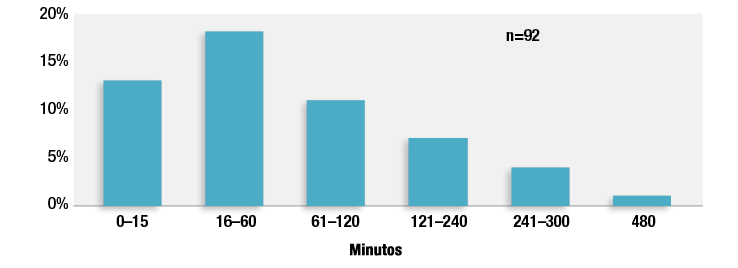
Dada la extensa lista de factores conocidos y desconocidos que contribuyen al OIVI posoperatorio, no es posible que los proveedores de atención médica y las instituciones puedan identificar con exactitud a todos los pacientes que desarrollarán esta complicación. A medida que envejece la población, la obesidad y la epidemia de opioides continúan creciendo y los proveedores de hospitales atienden a pacientes con enfermedades de mayor agudeza que en el pasado. Es probable que la mayoría de los pacientes tenga uno o más de estos factores de riesgo de padecer OIVI. La recomendación de la APSF y otras organizaciones para establecer el monitoreo electrónico continuo de todos los pacientes que reciban opioides en el período posoperatorio reduciría el daño atribuible a los factores de riesgo de pacientes no diagnosticados y diversos factores de riesgo institucional y de proveedores.15 Evitaría la confusión que rodea a la identificación de los pacientes de alto riesgo y promovería la estandarización de la atención médica posoperatoria de todos los pacientes. A medida que el personal de enfermería atienda a más pacientes, el uso del monitoreo electrónico continuo con alarmas centralizadas brindará un monitoreo más objetivo y continuo de los pacientes. Nuestro estudio demostró que se descubrió que casi un tercio de los 92 reclamos relacionados con OIVI posoperatorio tuvo su evento OIVI crítico en el transcurso de una hora después de su última revisión de enfermería y el 42 % dentro de las dos horas siguientes a la última revisión de enfermería (Figura 2).1 Las condiciones fluctuantes de los pacientes y la educación inadecuada del personal de enfermería respecto a las señales y los síntomas del OIVI contribuyeron a estos hallazgos. Estos intervalos de corto tiempo son un argumento de que solo las evaluaciones físicas realizadas por el personal de enfermería en la habitación no son suficientes para detectar el OIVI cuando el personal de enfermería está atendiendo más de un paciente a la vez.
Reproducción y modificación autorizadas. Lee LA, Caplan RA, Stephens LS, Posner KL, Terman GW, Voepel-Lewis T, Domino KB. Postoperative opioid-induced respiratory depression: a closed claims analysis. Anesthesiology 2015;122:659-65.
Figura 2. Tiempo transcurrido entre la última revisión de enfermería y el descubrimiento del deterioro ventilatorio inducido por opioides en 92 reclamos. No se muestran los reclamos de tiempo desconocido (n = 39) y los que no se aplican (en casa, n = 3).
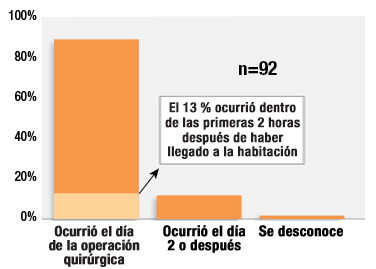
El período crítico del uso del monitoreo electrónico continuo en el período posoperatorio incluye, principalmente, las primeras 24 horas posoperatorias, ya que los datos del Proyecto de Reclamos Cerrados demuestran que un 88 % de estos eventos ocurrió dentro de ese plazo (Figura 3).1 El traslado del área de estimulación más alta y ruidosa de la sala de recuperación con una relación de enfermera a paciente de 1:1 o 1:2 al piso donde los pacientes tendrán menos estimulación y un monitoreo menos intensivo por parte del personal de enfermería es un momento que representa alto riesgo. Nuestro estudio reveló que el 13 % de estos eventos de OIVI ocurrió dentro de las dos horas posteriores al traslado a la habitación. Estos hallazgos son congruentes con otros estudios que han determinado que las primeras 24 horas son el período de más alto riesgo para que los pacientes en posoperatorio desarrollen OIVI.16-18
Reproducción y modificación autorizadas. Lee LA, Caplan
RA, Stephens LS, Posner KL, Terman GW, Voepel-Lewis T,
Domino KB. Postoperative opioid-induced respiratory depression: a closed claims analysis. Anesthesiology 2015;122:659-65.
Figura 3. Tiempo posoperatorio de la depresión respiratoria inducida por opioides en 92 reclamos del Proyecto de Reclamos Cerrados.
Por último, el monitoreo electrónico continuo con alarmas centralizadas, en teoría, sería capaz de alertar a los proveedores sobre la evolución de otras complicaciones posoperatorias que pueden alterar la frecuencia respiratoria y la frecuencia cardíaca, además de la saturación de oxígeno, como sepsis, choque hipovolémico, neumonía y otras enfermedades. Taenzer y colaboradores demostraron con éxito este concepto cuando establecieron la vigilancia electrónica con la oximetría de pulso continua con alarmas centralizadas.19,20 Notaron una significativa reducción del 50 % en los traslados de la habitación a la UCI, una reducción del 60 % en los eventos de rescate del punto de referencia y una reducción en la mortalidad debida a causas relacionadas con los opioides. El rendimiento económico de la inversión también fue muy significativo, con ahorros estimados de USD 1,48 millones a partir de la reducción de traslados a la UCI en su unidad de estudio inicial.21 Esta cifra no tomó en cuenta ninguna reducción potencial en los gastos de por vida de los pacientes por la morbilidad reducida o por la defensa médico-legal institucional. Los datos de las primeras 24 horas en adelante se podrían utilizar para determinar en qué momento se puede separar al paciente del monitoreo electrónico continuo.
En resumen, la estratificación de los riesgos de OIVI es importante para el manejo perioperatorio de los anestésicos y medicamentos, pero no puede realizarse con alta confiabilidad. El concepto de usar solo los estados médicos y enfermedades preexistentes del paciente para identificar cuáles pacientes requieren el monitoreo electrónico continuo en el período posoperatorio anula el impacto significativo que tiene el entorno de atención médica (proveedores e institución) sobre los pacientes en relación con el desarrollo del OIVI de manera variable. El monitoreo electrónico continuo de la oxigenación y la ventilación de todos los pacientes posoperatorios que reciben opioides durante, al menos, las primeras 24 horas simplificaría y estandarizaría la atención posoperatoria y posiblemente reduciría la incidencia del OIVI posoperatorio, además de otras complicaciones. Los esfuerzos iniciales en las instituciones de recursos limitados por aumentar el monitoreo de los pacientes para detectar OIVI se pueden centrar en los factores de riesgo de los pacientes, pero las organizaciones deberían apuntar al objetivo definitivo de monitorear a todos los pacientes que reciban opioides en el período posoperatorio.
La Dra. Lee es miembro del Consejo Editorial del Boletín de la APSF y es anestesióloga del personal con Anestesia Premier en Kadlec Regional Medical Center en Richland, WA.
La Dra. Posner actualmente es profesora de Investigación y Laura Cheney es profesora de Seguridad de los Pacientes de Anestesia en el Departamento de Anestesiología y Medicina del Dolor de la University of Washington en Seattle, WA.
La Dra. Domino es profesora de Anestesiología en la Universidad de Washington en Seattle, WA.
Referencias
- Lee LA, Caplan RA, Stephens LS, et al. Postoperative opioid-induced respiratory depression: a closed claims analysis. Anesthesiology 2015;122:659–65.
- Localio AR, Lawthers AG, Brennan TA, et al. Relation between malpractice claims and adverse events due to negligence. Results of the Harvard Medical Practice Study III. N Engl J Med 1991;325:245–51.
- Joint Commission Enhances Pain Assessment and Management Requirements for Accredited Hospitals. The Joint Commission Perspectives 2017;37:1-4. Available at https://www.jointcommission.org/assets/1/18/Joint_Commission_Enhances_Pain_Assessment_and_Management_Requirements_for_Accredited_Hospitals1.PDF Accessed Dec 3, 2017.
- Center for Clinical Standards and Quality/Survey & Certification Group. Memorandum for requirements for hospital medication administration, particularly intravenous (IV) medications and post-operative care of patients receiving IV opioids. Center for Medicare and Medicaid Services. March 14, 2014. https://www.cms.gov/Medicare/Provider-
Enrollment-and-Certification/SurveyCertificationGenInfo/Downloads/Survey-and-Cert-Letter-14-15.pdf. Accessed Dec 3, 2017. - Gupta K, Prasad A, Nagappa M, et al. Risk factors for opioid-induced respiratory depression and failure to rescue: a review. Curr Opin Anaesthesiol 2018;31:110-119.
- Khelemsky Y, Kothari R, Campbell N, et al. Incidence and demographics of post-operative naloxone administration: a 13-year experience at a major tertiary teaching institution. Pain Physician 2015;18:E827–9.
- Niesters M, Overdyk F, Smith T, et al. Opioid-induced respiratory depression in paediatrics: a review of case reports. Br J Anaesth 2013;110:175–82.
- Chidambaran V, Olbrecht V, Hossain M, et al. Risk predictors of opioid-induced critical respiratory events in children: naloxone use as a quality measure of opioid safety. Pain Med 2014;15:2139–49.
- Pawasauskas J, Stevens B, Youssef R, et al. Predictors of naloxone use for respiratory depression and oversedation in hospitalized adults. Am J Health Syst Pharm 2014;71:746–50.
- Chidambaran V, Venkatasubramanian R, Zhang X, et al. ABCC3 genetic variants are associated with postoperative morphine-induced respiratory depression and morphine pharmacokinetics in children. Pharmacogenomics J 2017;17:162–169.
- Sadhasivam S, Chidambaran V, Zhang X, et al. Opioid-induced respiratory depression: ABCB1 transporter pharmacogenetics. Pharmacogenomics J2015;15:119–26.
- Weingarten TN, Jacob AK, Njathi CW, et al. Multimodal analgesic protocol and postanesthesia respiratory depression during phase 1 recovery after total joint arthroplasty. Reg Anesth Pain Med 2015;40:330–6.
- Cavalcante AN, Sprung J, Schroeder DR, et al. Multimodal analgesic therapy with gabapentin and its association with postoperative respiratory depression. Anesth Analg 2017;125:141–146.
- George JA, Lin EE, Hanna MN, et al. The effect of intravenous opioid patient-controlled analgesia with and without background infusion on respiratory depression: a meta-analysis. J Opioid Manag 2010;6:47–54.
- Stoelting RK and Overdyk FJ for the Anesthesia Patient Safety Foundation. Conclusions and Recommendations from the June 8, 2011, Conference on Electronic Monitoring Strategies (Essential Electronic Monitoring Strategies to Detect Clinically Significant Drug-Induced Respiratory Depression in the Postoperative period). Available at https://www.apsf.org/initiatives.php?id=10 (last accessed Dec 3, 2017).
- Taylor S, Kirton OC, Staff I, et al. Postoperative day one: a high risk period for respiratory events. Am J Surg 2005; 190:752–6.
- Ramachandran SK, Haider N, Saran KA, et al. Life-threatening critical respiratory events: a retrospective study of postoperative patients found unresponsive during analgesic therapy. J Clin Anesth 2011;23:207–13.
- Weingarten TN, Herasevich V, McGlinch MC, et al. Predictors of delayed postoperative respiratory depression assessed from naloxone administration. Anesth Analg 2015;121:422–9.
- Taenzer AH, Pyke JB, McGrath SP, et al. Impact of pulse oximetry surveillance on rescue events and intensive care unit transfers: a before-and-after concurrence study. Anesthesiology 2010;112:282–7.
- McGrath SP, Taenzer AH, Karon N, et al. Surveillance Monitoring management for general care units: strategy, design, and implementation. Jt Comm J Qual Patient Saf 2016;42:293–302.
- Taenzer AH, Blike GT. Postoperative monitoring—the Dartmouth experience. APSF Newsletter 2012;27:1. Available at https://www.apsf.org/newsletters/html/2012/spring/01_postop.htm. Accessed Dec 4, 2017.


 Issue PDF
Issue PDF