ケタミンの起源
 ケタミンは、約60年前にデトロイトの研究所で初めて合成されて以来、他とは異なる薬物特性、不均質で相互に関連する薬物作用機序を持ち、さらには場合によっては競合しうる種々の臨床用途を持つ、複雑な薬物であることが示されてきた。
ケタミンは、約60年前にデトロイトの研究所で初めて合成されて以来、他とは異なる薬物特性、不均質で相互に関連する薬物作用機序を持ち、さらには場合によっては競合しうる種々の臨床用途を持つ、複雑な薬物であることが示されてきた。
ケタミンの起源は、科学者がシクロヘキシルアミンと呼ばれる新しい種の麻酔用薬剤を発見した1956年に遡る。1 この種における最初の薬はフェンシクリジン(PCP)であった。1962年に新しい化合物であるCI-581が発見され、これはPCPが持つ望ましい性質を備えつつも重度の興奮状態や重大な精神病などの主要な副作用がみられないものであった。2 この新しい薬がのちにケタミンと呼ばれるものであった。研究の初期段階でケタミンを投与された被験者の中には「腕も脚もない」かのように感じたものがいたという。また「死んでしまったような」感覚を持ったり、鮮明な幻覚を経験するものもいた。これらにより研究者たちは「解離性麻酔」という用語を用いはじめた。2,3
基礎科学
ケタミンのもつNMDA受容体に対する拮抗作用が、健忘、麻酔、解離作用の主たる原因であると考えられている。4 NMDA受容体遮断は、げっ歯類において記憶形成を遮断することが示されている。5 さらに、脊髄NMDA受容体は痛みの中枢性感作に密接に関係しているため、繰り返されるNMDA受容体活性化により痛覚過敏を引き起こす可能性がある。NO合成酵素、GABA、およびアセチルコリンに対する作用も、ケタミンで見られる独特かつ複雑な作用や副作用に寄与している可能性がある。6
ケタミンの代謝は主に肝臓でなされ、ケタミンはノルケタミンに代謝される。ノルケタミンは強力な麻酔特性も持つ活性代謝産物である。ノルケタミンの作用に加えて、ケタミンの親油性が、その標準的な導入量である1-2 mg/kgの経静脈的投与後の10〜15分という長い分布半減期の原因である可能性がある。他の麻酔導入に使用する薬剤とは異なり、ケタミンを大量に投与された患者は、眼振、瞳孔散大を起こし、薬剤投与量が全身麻酔レベルに達しても閉眼できない状態が見られることがある。表1はケタミンの一般的な利点と副作用をまとめたものである。
表 1.ケタミンの潜在的な利点と副作用
| 利点 |
| 呼吸ドライブの維持 |
| 最小限の心血管抑制 |
| 周術期オピオイド誘発痛覚過敏の減衰 |
| 急性/慢性疼痛症候群の補助的治療 |
| 抗自殺および抗うつ特性 |
| 副作用 |
| 気道分泌物の増加、気道反射減衰は最小 |
| 心拍数、血圧、SVRの上昇、重度CADのある患者における心筋虚血 |
| 幻覚、混乱、鮮明な夢、せん妄 |
| 肝機能障害患者における作用時間の延長 |
| 複視、目のかすみ |
SVR;全身血管抵抗、CAD;冠動脈疾患
ケタミンに関連する生理学的および向精神作用は、初の人体での研究以来よく触れられている(表1)。血圧、心拍数、心収縮力、および全身の血管抵抗の上昇から、ケタミンの交感神経刺激作用がまず示された。2 ここで観察された交感神経緊張の増加は、ケタミンによって副腎カテコラミン放出が引き起こされることによる二次性のものであることが現在知られている。興味深いことに、ケタミン自体には直接的な陰性変力作用があるが、ここで示した交感神経性サージによって目立たなくなっている。高交感神経緊張のある患者(例として外傷患者)をケタミンで麻酔導入する場合は、すでにストレス下にある副腎から放出されているカテコラミンの作用をケタミンの心筋抑制作用が上回る可能性があるため、注意を要する。重度の冠動脈疾患の患者へのケタミン投与に関しても、心筋の酸素需要がケタミン投与による酸素供給の増加に比して不釣り合いに大きいため、慎重を期すべきである。
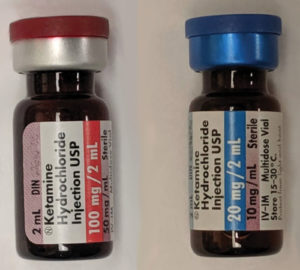
静脈内ケタミンの2用量、50mg/mlおよび10mg/ml。出典:Wikipedia. https://creativecommons.org/share-your-work/licensing-considerations/compatible-licenses
ケタミンは、呼吸様式への影響が最小限である数少ない静脈麻酔薬の1つである。さらに、その気管支拡張作用は喘息患者に特に有益である可能性がある。7 大規模な無作為化対照試験がほとんどなく、投与レジメンが定まっていないため、気管支拡張に関して最適な用量は定まっていない。気道分泌物の増加などの呼吸器への悪影響は、唾液分泌抑制薬を使用することで軽減できる。
ケタミン用量を増加していくと、ガンマバーストパターン(スローデルタ振動によって遮断されたガンマ振動)を生じ、その後に安定したベータ/ガンマパターンが発生するという、特徴的な脳波(Electroencephalogram, EEG)パターンが見られる。8 このEEGの変化は、ケタミンによって誘発される無意識状態への移行に続いて起こる。このようにケタミン使用下では平坦脳波が認められないため、麻酔深度をEEGパターンに合わせて調整することは推奨されない。
以前の報告では、ケタミンが頭蓋内圧(Intracranial Pressure, ICP)を増加させるとしている。9,10 脳血流(Cerebral Blood Flow, CBF)と脳の酸素消費量の増加がこのICP増加につながったと仮定された。そのために古典的な考え方では、神経学的処置においてケタミンの使用は避けられていた。しかしながら、これらの研究にはケタミンによる麻酔導入後 、患者に自発呼吸をさせている例も含んでいるものがあり、高二酸化炭素血症に伴う血管拡張によるICP上昇を見ている可能性がある。11 この定説にも数々の疑義が示されてきている。現在の研究では、人工呼吸器を装着した患者で他の鎮静薬と併用すると、ICPが増加しないことが示唆されている。12–14 ICPに対する麻酔量以下の投与量でのケタミンの効果に関するデータはないが、そのような鎮静用量を下回るような少量の投与量の場合、ICPへの影響は最小限となるのではないだろうか。
臨床麻酔における現在の使用
ケタミンが1970年に米国食品医薬品局(the Food and Drug Administration; FDA)によって承認された後、初めて広く使用されたのはベトナム戦争において戦場での麻酔薬としてであった。3 1985年に世界保健機関はケタミンを「必須医薬品」に分類し、現在では世界で最も一般的に使用されている麻酔薬であると考えられている。15
集中治療室や救急治療室などの急性期医療現場では、ケタミンによる処置時の鎮静がずっと安全に使用されてきた。16 「オピオイドの蔓延 」の発生に伴い、術中の使用が再び注目されている。ケタミンは麻酔量以下の投与量を投与すると、オピオイドへの耐性形成を減少させ、手術後のオピオイド誘発痛覚過敏を減少させる可能性がある。17 脊椎手術を受ける慢性疼痛のある患者にケタミンを投与すると、術後のさまざまな時点で疼痛スコアが低下し、オピオイドの使用量が減少することが示されている。18 オピオイドを投与されたことがない患者においても、痛みを伴う手術処置を受ける場合にケタミンは術後鎮痛に有益である可能性がある。19 表2は、ケタミンの一般的に使用される投与量をまとめたものである。
表 2.管理の提案30,35,36
| ルート | 投与範囲 |
| 麻酔導入 | 1–2 mg/kg |
| 初期投与量(鎮静および鎮痛用) | 呼吸抑制および交感神経反応を回避するために0.1 - 0.5 mg / kgを60秒間かけて投与 |
| ボーラス/追加投与量 | 必要に応じて 0.1–0.5 mg/kg |
| 鎮静/鎮痛(挿管患者用) | 5–30 µg/kg/分 |
| 鎮痛(非挿管患者用) | 1–5 µg/kg/分 |
| 治療抵抗性うつ病 | 0.5 mg/kg を40 分かけて |
添加されている保存剤や直接的な神経細胞アポトーシスによる神経毒性の可能性があるため、神経幹麻酔におけるケタミンの使用は一定の見解が得られていない。20 ただし、上記二つの病因は特定の動物モデルでのみ確認されており21,22 その後の研究では、ヒトにおいて臨床的な神経毒性は示されていない。23 このことが、切断肢の断端痛の発生の予防や24 開胸術後疼痛症候群の軽減に対するケタミンの役割を調査するいくつかの研究につながった。 25
ケタミンは、標準的なオピオイド患者管理鎮痛法(PCA)レジメンでは緩和されない術後疼痛を治療するために、急性疼痛サービスでよく使用されている。鎌状赤血球症における血流閉塞による疼痛発作のような急性または慢性の疼痛増悪を来している非外科的患者もケタミンの恩恵を受ける可能性がある。26 注入速度は外科系患者と比較し低く、一般にボーラス投与の有無にかかわらず0.3 mg/kg/hr未満で管理できる。ケタミンを追加することにより、オピオイドの消費量を減らし、PCAから経口オピオイドへの移行を促進できる。ケタミンを含むPCA(1 – 5 mg /ボーラス)を使用することで疼痛管理を改善し、オピオイド消費を減らすことができるというエビデンスもある。27
安全上の考慮事項
ケタミンの禁忌には、妊娠、肝機能障害、重大な冠動脈疾患、精神病があげられる(表3)。前述のように、ICPの上昇は調節呼吸下での鎮静患者には起こらない。眼圧(IOP)の上昇は、初期の研究に基づいて一般的に禁忌として挙げられている。28 しかし最新のエビデンスではIOPの変動はほとんどないとされている。29 この機序として外眼筋の筋緊張の変化が考えられている。28
表 3.適応/禁忌
| 適応 |
鎮痛
|
| 急性または慢性疼痛の悪化 |
| 鎮静(機械換気) |
| 医療行為を行う際の鎮静 |
| 迅速導入時の気管挿管 |
| 治療抵抗性うつ病 |
| 禁忌 |
| 精神病 |
| 薬物濫用患者 |
| 重度の肝機能障害 |
| 冠動脈疾患 |
| コントロール不良高血圧 |
術中の使用では、ケタミンが単一麻酔薬として使用されるか鎮痛補助剤として使用されるかにかかわらず、標準的な米国麻酔学会(ASA)のモニタリングを適用する必要がある。麻酔量以下の投与量であってもケタミンには、気道障害、心血管系障害、および精神病様症状のリスクが伴うものである。急性期医療の環境では、血圧、心電図、およびパルスオキシメトリを利用できる必要がある。米国局所麻酔疼痛医学会(ASRA)、米国疼痛医学会(AMPA)、および米国麻酔学会(ASA)から出された慢性疼痛に対する静脈内ケタミン使用に関する共通ガイドラインによると、30 指導医はAdvanced Cardiovascular Life Support(ACLS)認定を受けている必要があり、またASAの求める中程度の鎮静のための要件を満たしている必要がある。ケタミンを投与する者の条件として、少なくとも看護学位を所持し、中程度の鎮静とケタミンの薬理学に関する訓練を受けており、ACLS認定を取得していることが求められる。
抗うつ薬としてのケタミン
ケタミンは、エスケタミンとアルケタミンのラセミ混合物として生成される。2019年3月、治療抵抗性うつ病の管理のための画期的医薬品(ファーストインクラス)としてラセミ体ケタミンの陽性鏡像異性体であるエスケタミンのFDA認可が通り、ケタミンへの科学的および一般的関心が高まった。31
ケタミンは強力な抗自殺および抗うつ特性を有している。32 しかし抗うつ薬としては、異なる血清濃度では異なる効果を発揮する可能性があり、またその効果は標準的な用量反応曲線に従わない可能性がある。麻酔導入での投与量をはるかに超える投与量でも、麻酔量以下の投与量の際と比較してケタミンの抗うつ効果がより大きくなることはなさそうだ。この点で、トラザドンのような他の精神薬と類似している。33 トラザドンは150 mg未満の用量では鎮静剤として機能するが、150 mgを超える用量では抗うつ剤として機能する一般的な多機能薬である。
ケタミンの抗自殺および抗うつ作用の機序として、AMPA活性化による血清グルタミン酸濃度が挙げられる。うつ病治療として患者に静脈内ケタミンを投与している学術機関の臨床医は、最近まで、40分かけて0.5 mg / kgを投与する方法を一般的に取っていた(表 2)。34 これはこの用量での研究が多く行われているためであり、この投与法では約2000 - 3000 ng / mLの血清濃度に至る。治療は通常、週に1-3回行われる。しかしながらケタミン投与プロトコールの共有は進まず、研究と実経験の両方において有用性が示されている用量の漸増を慎重に行う投与レジメンが施設ごとに差異はありながら存在している状態である。
麻酔学会のガイドラインと同様に、30,36 米国精神医学会は外来でケタミンを投与する医療者はACLS認定を受けることを求めている。34 ケタミンは低用量で使用した場合に呼吸抑制を起こす可能性が低いため、低用量では比較的「安全な」薬品として認識されている。交感神経刺激作用(心拍数と血圧の上昇)は麻酔導入量の投与でしばしばみられるが、このような変化は麻酔量以下の投与量であれは稀である。35 鎮静時モニタリングには、最低でも連続的な経皮的動脈酸素飽和度測定と10分ごとの血圧測定を行う。35 同様に、自殺念慮がある状態または重度のうつ病状態に対して使用される場合、患者の安全を確保するために、短期および長期的な精神的影響を観察し、管理する必要がある。34 治療前に患者に問診を行い、当初の症状と治療への反応を評価しなければならない。投薬後、一般的に患者は30分から2時間で回復したのち付添人とともに退院する。このガイドラインは我々の施設で実際に採用しているものであり、他施設においては異なるモニタリング基準と治療法がありうることに留意する必要がある。一連のガイドラインを広く採用する前には、さらなるエビデンスに基づく推奨事項が必要となる。
結論
ケタミンは歴史のある薬で、周術期医療とうつ病管理において臨床医の間で新たな関心が高まっている。オピオイドを使わない疼痛管理を必要とする慢性疼痛の患者が増加するのに従って、またうつ病やその他の精神疾患の治療における少量投与の実用性が高まってきており、この使い古された薬は有用性を増してきている。しかし、術後や外来での本薬剤投与において適切なモニタリングに関しては、さらなる調査が必要であろう。
Dr. Kung は、マサチューセッツ州ボストンの Massachusetts General Hospital の麻酔科レジデントである。
Dr. Meisner は、マサチューセッツ州ベルモントの McClean Hospital のケタミンサービスのメディカルディレクターであり、マサチューセッツ州ボストンの Massachusetts General Hospital の精神科助手である。
Dr. Berg は、マサチューセッツ州ボストンの Massachusetts General Hospital の麻酔学助教である。
Dr. Ellis は、マサチューセッツ州ボストンの Massachusetts General Hospital で麻酔学インストラクターを務めている。
Dr.Kung、Dr. Berg、及び Dr. Ellis には利益相反はない。Dr. Meisner は Janssen Pharmaceutical の諮問委員を務めた。
参考文献
- Maddox VH, Godefroi EF, Parcell RF. The synthesis of phencyclidine and other 1-arylcyclohexylamines. J Med Chem. 1965;8:230–235.
- Domino EF, Chodoff P, Corssen G. Pharmacologic effects of CI-581, a new dissociative anesthetic, in man. Clin Pharmacol Ther. 1965;6:279–291.
- Mion G. History of anaesthesia. Clin Pharmacol Ther. 2017;34: 571–575.
- Persson J. Wherefore ketamine? Curr Opin Anaesthesiol. 2010;23:455–460.
- Mathews MJ, Mead RN, Galizio, M. Effects of N-Methyl-D-aspartate (NMDA) antagonists ketamine, methoxetamine, and phencyclidine on the odor span test of working memory in rats. Exp Clin Psychopharmacol. 2018;26:6–17.
- Kohrs R, Durieux ME. Ketamine. Anesth Analg. 1998;87,
1186–1193. - Agrawal A, Goyal S. Ketamine in status asthmaticus: a review. Indian J Crit Care Med. 2013;17:154–161.
- Akeju O, Song AH, Hamilos AE, et al. Electroencephalogram signatures of ketamine anesthesia-induced unconsciousness. Clin Neurophysiol. 2016;127: 2414–2422.
- Gardner AE, Dannemiller FJ, Dean D. Intracranial cerebrospinal fluid pressure in man during ketamine anesthesia. Anesth Analg. 1972;51:741–745.
- Gardner AE, Olson BE, Lichtiger M. Cerebrospinal-fluid pressure during dissociative anesthesia with ketamine. Anesthesiology. 1971;35:226–228.
- Wang X, Ding X, Tong Y, et al. Ketamine does not increase intracranial pressure compared with opioids: meta-analysis of randomized controlled trials. J Anesth. 2014;28:821–827.
- Chang LC, Raty SR, Ortiz J, et al. The emerging use of ketamine for anesthesia and sedation in traumatic brain injuries. CNS Neurosci Ther. 2013;19:390–395.
- Zeiler FA, Teitelbaum J, West M, et al. The ketamine effect on ICP in traumatic brain injury. Neurocrit Care. 2014;21: 163–173.
- Zeiler FA, Teitelbaum J, West M, Gillman LM. The ketamine effect on intracranial pressure in nontraumatic neurological illness. J Crit Care. 2014;29:1096–1106.
- Fact file on ketamine. (2016, March). Retrieved from https://www.who.int/medicines/news/20160309_FactFile_Ketamine.pdf?ua=1.
- Sheikh S, Phyllis H. The expanding role of ketamine in the emergency department. Drugs. 2018;78:727–735.
- Nielsen RV, Fomsgaard JS, Siegel H, et al. Intraoperative ketamine reduces immediate postoperative opioid consumption after spinal fusion surgery in chronic pain patients with opioid dependency. Pain. 2017;158:463–470.
- Loftus RW, Yeager MP, Clark JA, et al. Intraoperative ketamine reduces perioperative opiate consumption in opiate-dependent patients with chronic back pain undergoing back surgery. Anesthesiology. 2010;113:639–646.
- Laskowski K, Stirling A, McKay WP, Lim HJ. A systematic review of intravenous ketamine for postoperative analgesia. Can J Anaesth. 2011;58:911–923.
- Schmid R, Katz J. Neural toxicity of ketamine and other NMDA antagonists. Pain. 2000;88:312.
- Borgbjerg FM, Svennson BA, Frigast C, Gordh T Jr., Histopathology after repeated intrathecal injections of preservative-free ketamine in the rabbit: a light and electron microscopic examination. Anesth Analg. 1994;79:105–111.
- Olney JW, Labruyere J, Price MT. Pathological changes induced in cerebrocortical neurons by phencyclidine and related drugs. Science. 1989;244:1360–1362.
- Subramaniam K, Subramaniam B, Steinbrook RA. Ketamine as adjuvant analgesic to opioids: a quantitative and qualitative systematic review. Anesth Analg. 2004;99:482–495.
- Wilson JA, Nimmo AF, Fleetwood-Walker SM, et al. A randomised double blind trial of the effect of pre-emptive epidural ketamine on persistent pain after lower limb amputation. Pain. 2008;135:108–118.
- Feltracco P, Barbieri S, Rizzi S, et al. Perioperative analgesic efficacy and plasma concentrations of s( )-ketamine in continuous epidural infusion during thoracic surgery. Anesth Analg. 2013;116:1371–1375.
- Puri L, Morgan KJ, Anghelescu DL. Ketamine and lidocaine infusions decrease opioid consumption during vaso-occlusive crisis in adolescents with sickle cell disease.Curr Opin Support Palliat Care. 2019;13:402–407.
- Wang L, Johnston B, Kaushal A, et al. Ketamine added to morphine or hydromorphone patient-controlled analgesia for acute postoperative pain in adults: a systematic review and meta-analysis of randomized trials. Can J Anaesth. 2016;63:311–325.
- Yoshikawa K, Murai Y. The effect of ketamine on intraocular pressure in children. Anesth Analg. 1971;50:199–202.
- Drayna PC, Estrada C, Wang W, et al. Ketamine sedation is not associated with clinically meaningful elevation of intraocular pressure. Am J Emerg Med. 2012;30:1215–1218.
- Cohen SP, Bhatia A, Buvanendran A, et al. Consensus guidelines on the use of intravenous ketamine infusions for chronic pain from the American Society of Regional Anesthesia and Pain Medicine, the American Academy of Pain Medicine, and the American Society of Anesthesiologists. Reg Anesth Pain Med. 2018;43:521–546.
- Kim J, Farchione T, Potter A, et al. Esketamine for treatment-resistant depression—first FDA-approved antidepressant in a new class. NEJM. 2019;381:1–4.
- Ionescu DF, Swee MB, Pavone KJ, et al. Rapid and sustained reductions in current suicidal ideation following repeated doses of intravenous ketamine secondary analysis of an open label study. J Clin Psychiatry. 2016;77:e7-19-25.
- Stahl SM. Mechanism of action of trazodone: a multifunctional drug. CNS Spectr. 2009;14:536–546.
- Sanacora G, Frye MA, Mcdonald W, et al. A Consensus Statement on the Use of Ketamine in the Treatment of Mood Disorders. JAMA Psychiatry. 2017;74:399.
- Riva-Posse P, Reiff CM, Edwards JA, et al. Blood pressure safety of subanesthetic ketamine for depression: a report on 684 infusions. J Affect Disord. 2018;236:291–297.
- Schwenk ES, Viscusi ER, Buvanendran A, et al. Consensus guidelines on the use of intravenous ketamine infusions for acute pain management from the American Society of Regional Anesthesia and Pain Medicine, the American Academy of Pain Medicine, and the American Society of Anesthesiologists. Reg Anesth Pain Med. 2018:43:456-466.

