| As informações fornecidas são somente para fins educacionais relacionados à segurança, e não constituem aconselhamento médico ou legal. Respostas individuais ou de grupo são somente comentários, fornecidos para fins educacionais ou para debate e não constituem afirmações nem opiniões da APSF. Não é intenção da APSF fornecer aconselhamento médico ou legal específico ou apoiar quaisquer pontos de vista ou recomendações em resposta às questões propostas. Em hipótese alguma a APSF será responsável direta, ou indiretamente, por qualquer dano ou perda causados por ou supostamente causados por ou em conexão com a confiança nas informações mencionadas. |
Durante décadas, o campo da epidemiologia hospitalar estudou a transmissão de infecções no âmbito dos serviços de saúde. Sabemos que a disseminação de organismos nos hospitais ocorre através da interação de pacientes, profissionais de saúde e seus ambientes. Os pacientes são colonizados com organismos (patogênicos e não patogênicos) nas vias aéreas, no trato gastrointestinal e na pele. Esses organismos contaminam o ambiente hospitalar e os equipamentos dos pacientes1.
A contaminação do ambiente tem duas consequências diretas: contaminar as mãos do profissional de saúde e expor o próximo paciente internado na mesma área. As mãos dos profissionais ficam contaminadas não apenas depois do contato com um paciente, mas também depois de tocar em superfícies contaminadas no ambiente do paciente (ou seja, a “zona do paciente”)2. As luvas não impedem de maneira confiável a contaminação das mãos, pois descobriu-se que 13 a 29% das mãos do profissional de saúde estavam contaminadas após a remoção das luvas3,4. Pacientes internados em salas anteriormente ocupadas por pacientes colonizados ou infectados com enterococos resistente à vancomicina (ERV), Staphylococcus aureus resistentes à meticilina (SARM) ou Clostridium difficile correm maior risco de adquirir essas bactérias do que outros pacientes em todo o hospital5. Essa evidência sustenta a premissa de que a transmissão de organismos de paciente para paciente ocorre através de um ambiente contaminado. Um suporte adicional a esse ponto é a constatação de que a desinfecção adequada do ambiente hospitalar está associada à diminuição da transmissão de bactérias resistentes a múltiplas drogas6. A maior parte do nosso conhecimento sobre a transmissão cruzada baseada em organismos no ambiente hospitalar vem de estudos envolvendo unidades de internação, mas as salas de cirurgia não são tão extensivamente estudadas. No entanto, foi demonstrado que a contaminação das mãos e do ambiente transmite S. aureus, Enterococcus spp. e bacilos gram-negativos no ambiente da sala de cirurgia7-9. Além disso, a contaminação de torneiras de três vias por organismos presentes nos pacientes, equipamentos e mãos do profissional de saúde tem sido associada à transmissão durante e entre os casos10-12.
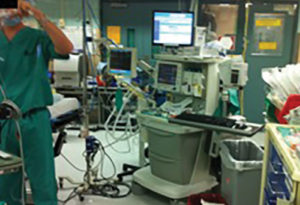
Figura 1: Foto de uma típica sala de cirurgia ocupada exibindo desordem, condições de lotação e uso de várias peças de equipamento que aumentam a probabilidade de transmissão de patógenos. Foto de L. S. Munoz-Price, MD, PhD.
Do ponto de vista do epidemiologista hospitalar, as áreas perioperatórias e salas de cirurgia especificamente, onde os três componentes necessários para a transmissão (pacientes, ambiente e profissionais de saúde) estão próximos (Figura 1), criam a situação ideal para a transmissão cruzada de organismos. As salas de cirurgia acomodam vários pacientes todos os dias, com inúmeras oportunidades de transmissão através do ambiente. No espaço confinado das salas de cirurgia, os profissionais de saúde tocam pacientes, dispositivos (por exemplo, cateteres intravenosos), superfícies do ambiente e equipamentos com grande frequência e realizam uma higiene limitada das mãos13. Além disso, a desinfecção dos equipamentos e do ambiente na sala de cirurgia podem não ser suficientes14.
A contaminação das superfícies da sala de cirurgia foi demonstrada tanto pela cultura do ambiente15 quanto pelo uso de marcadores fluorescentes14,16,17 . Esses marcadores são géis transparentes visíveis à luz ultravioleta que podem ser limpos com um pano úmido; sua presença 24 a 48 horas após a aplicação significa ausência de limpeza (pelo menos uma vez)14,17. Estudos observacionais sugerem que a limpeza de sala em todo o país, tanto no final quanto entre os casos, não é ideal14,17. Em dois estudos separados, marcadores fluorescentes foram usados para avaliar a limpeza por um período de 24 horas. Mais da metade das superfícies marcadas tinha os marcadores ainda presentes, indicando limpeza inadequada14, 17.

Figura 2: Contaminação bruta do paciente e do ambiente (cateter IV) após a aplicação do marcador fluorescente na boca de um manequim em uma sala de cirurgia simulada.16
Com permissão de uso de Anesthesia & Analgesia. Birnbach DJ, Rosen LF, Fitzpatrick M, et al. The use of a novel technology to study dynamics of pathogen transmission in the operating room. Anesth & Analg. 2015; 120:844-847.
O possível papel das mãos dos profissionais de saúde na contaminação do ambiente da sala de cirurgia foi examinado usando um ambiente simulado16. O gel fluorescente foi aplicado na boca de um simulador de paciente humano antes da intubação e o simulador e a sala de cirurgia foram avaliados após o contato (Figura 2). Mais da metade das quarenta áreas avaliadas foram positivas para o marcador fluorescente em pelo menos nove das dez simulações, treze das quais foram contaminadas nas dez simulações16.
A contaminação do equipamento e do ambiente pode, em parte, ocorrer em função do design das instalações e de fatores operacionais que não são propícios à limpeza e desinfecção entre os casos. Além disso, embora os hospitais monitorem e acompanhem de perto o tempo de virada das salas de cirurgia, eles são menos propensos a medir a eficácia da limpeza e da desinfecção18,19. Uma possível associação entre tempos de virada mais curtos à eficácia da limpeza e transmissão da doença merece mais estudos. Do nosso ponto de vista, tempos de virada inferiores a 30 minutos20 (e até 60 minutos) têm probabilidade de tornar a limpeza e desinfecção eficaz extremamente desafiadora, considerando todas as superfícies horizontais desordenadas dentro e sobre os carrinhos de anestesia e as superfícies complicadas da máquina de anestesia.
Desinfetar as mãos com frequência suficiente para impedir a transmissão de organismos na área de trabalho da anestesia também pode ser um desafio. As oportunidades para contaminação das mãos são muito frequentes — com média de cerca de 150 contatos na superfície por hora durante a indução e 60 por hora durante a manutenção13. Devido à natureza do trabalho, executar a higiene das mãos de acordo com as diretrizes da Organização Mundial da Saúde (OMS)21 pode ser impraticável, levando a um desempenho de higiene das mãos pouco frequente, apesar das inúmeras oportunidades recomendadas pela OMS para a higiene das mãos (antes de tocar no paciente, depois de tocar no paciente, após tocar nos arredores do paciente, após contato com fluidos corporais e antes de técnicas assépticas)22. Tornar os desinfetantes para as mãos à base de álcool mais acessíveis teve resultados mistos. A colocação de dispensers na máquina de anestesia mostrou uma melhoria mínima, enquanto os lembretes eletrônicos aumentaram em dez vezes a taxa de higiene das mãos23,24. O uso de desinfetantes portáteis para mãos à base de álcool pode aumentar significativamente a frequência da desinfecção das mãos e reduzir a contaminação das torneiras de três vias25. Embora as luvas possam proteger os profissionais de anestesia do contato com superfícies contaminadas, elas não eliminam a contaminação de pacientes ou equipamentos.
Birnbach et al. observou que a contaminação era encontrada 60% do tempo na maçaneta da porta da sala de cirurgia, embora nenhum dos profissionais médicos usasse luvas no momento da saída durante um exercício de simulação16. Isso sugere a importância não apenas da substituição das luvas, mas também da higiene das mãos, mesmo quando as luvas são usadas.
Para enfrentar esses desafios, a Society for Healthcare Epidemiology of America (SHEA) colaborou com a American Society of Anesthesiology (ASA), a Anesthesia Patient Safety Foundation (APSF), a Association of periOperative Registered Nurses (AORN) e a American Association of Nurse Anesthetists (AANA) para publicar diretrizes de controle de infecção para a área de trabalho de anestesia26. Essa orientação foi elaborada para fornecer técnicas práticas e baseadas em evidências, com conselhos sobre como implementá-las (Tabela 1). No entanto, para que essas recomendações sejam eficazes, os anestesiologistas precisam mudar seu comportamento de acordo.
Tabela 1: Resumo das recomendações, orientação especializada da SHEA: Prevenção de infecções na área de trabalho de anestesia26
| Higiene das mãos |
| Realizada no mínimo: |
| • Antes das tarefas assépticas |
| • Depois de remover as luvas |
| • Quando as mãos estão sujas ou contaminadas |
| • Antes de tocar no conteúdo do carrinho de anestesia |
| • Ao entrar e sair da sala de cirurgia |
| Considere luvas duplas durante o manejo das vias aéreas |
| • Remova as luvas externas imediatamente após a manipulação das vias aéreas |
| • Remova as luvas internas e realize a higiene das mãos o mais rápido possível |
| Localize dispensers de solução à base de álcool para higienização das mãos na entrada da sala de cirurgia e próximo a anestesistas na sala de cirurgia |
| Evidências insuficientes para o uso de álcool nas mãos com luvas |
| • É preferível trocar as luvas e fazer a higiene das mãos entre colocar e retirar as luvas |
| Desinfecção do Ambiental |
| Laringoscópios/Videolaringoscópios |
| • Desinfecção completa de alto nível das lâminas e cabos padrão de laringoscópio e videolaringoscópio reutilizáveis |
| • Considere a substituição por dispositivos descartáveis |
| Máquina e carrinho de anestesia |
| • Evidência insuficiente para uso de capa descartável |
| • Limpe as superfícies externas acessíveis entre os casos |
| • Efetue a higiene das mãos antes de abrir e manusear o conteúdo da gaveta |
| • Evite armazenar suprimentos em cima do carro |
| Preparação da sala de cirurgia entre usos |
| • Limpe e desinfete as superfícies de grande contato na máquina de anestesia e na área de trabalho de anestesia entre os usos da sala de cirurgia |
| Conexões de injeção |
| • Use apenas conexões desinfetadas para acesso intravenoso |
| • Desinfecção de conexões |
| • Esfregue com um desinfetante estéril à base de álcool imediatamente antes de cada uso |
| • Cubra as conexões continuamente com tampas estéreis contendo álcool isopropílico |
| • Desinfete antes da injeção individual do medicamento ou no início de uma rápida sucessão de injeções (por exemplo, indução da anestesia) |
| Frascos de medicamentos |
| • Limpe a tampa de borracha e a ampola com álcool 70% antes de cada acesso |
| • Use frascos para doses únicas sempre que possível |
| • Frascos de doses múltiplas devem ser usados para 1 paciente, use agulha e seringa estéreis para cada aplicação |
| • Nunca reutilize seringas ou agulhas em outro paciente |
| Precauções de barreira total |
| • Uso de touca, roupa privativa estéril, máscara, luvas estéreis e cortina grande estéril |
| • Use para inserção de todos os CVCs e cateteres arteriais femorais e axilares |
| Seringas sem agulha |
| • Tampe novamente se estiver administrando doses múltiplas ao mesmo paciente a partir da mesma seringa |
| Profissional preparou injetáveis estéreis |
| • Use o mais rápido possível após a preparação |
| Bolsas IV com conector tipo spike |
| • Minimize o tempo entre a punção e a administração |
| Teclados e touchscreens |
| • Limpe e desinfete após cada caso |
| Isolamento de contato |
| • Siga todas as políticas específicas da instituição para higiene das mãos, equipamentos de proteção individual e limpeza do ambiente |
| Implantação |
| • Realize avaliação e monitoramento regulares das práticas, higiene das mãos e limpeza e desinfecção do ambiente |
| • Incentive a colaboração de profissionais da linha de frente e da liderança |
| • Evidências insuficientes para recomendar o monitoramento baseado em tecnologia |
Como epidemiologistas hospitalares, solicitamos aos anestesiologistas que reconheçam que a transmissão de organismos existe dentro de hospitais, incluindo salas de cirurgia, e que mudanças são necessárias na área de trabalho de anestesia. Desafiamos você a ajudar a impedir a transmissão dos organismos nas salas de cirurgia, melhorando a aderência à higiene das mãos, defendendo uma melhor desinfecção do ambiente e de equipamentos e identificando oportunidades para a reengenharia da área de trabalho de anestesia que facilitará a desinfecção e evitará a transmissão cruzada. Por exemplo, a higiene das mãos é prejudicada pelo fluxo de trabalho e pela falta de fácil disponibilidade dos produtos26. A contratação de equipes perioperatórias e engenheiros de fatores humanos para reprojetar os fluxos de trabalho poderia auxiliar mais com a higiene adequada das mãos. Da mesma forma, a contratação de engenheiros biomédicos para reprojetar equipamentos pode melhorar a higiene das mãos e a desinfecção. Sabemos que algumas das recomendações de orientação26 podem ser descartadas como irrealistas, irracionais ou sem fundamento; no entanto, a transmissão de patógenos de paciente para paciente é uma ocorrência inegável e precisa ser abordada.
Nós e nossos colegas de prevenção de infecções frequentemente somos questionados: e daí? E daí se os pacientes forem expostos aos organismos de pacientes anteriores? E daí se a higiene das mãos não é realizada? A resposta é que as evidências mostram que essas práticas apresentam riscos para a transmissão bacteriana. O caminho para enfrentar esses desafios foi estabelecido, e nós, na epidemiologia da saúde, estamos prontos para ajudar você. Procuramos lideranças dentro da sala de cirurgia para ter a oportunidade de evitar danos ao paciente.
Joshua Schaffzin, MD, PhD, professor assistente de Pediatria Clínica, Divisão de Doenças Infecciosas, Centro Médico do Hospital Infantil de Cincinnati, Departamento de Pediatria, Faculdade de Medicina da Universidade de Cincinnati, Cincinnati, OH.
Lynn Johnston, MD, MSc, FRCPC, professora de Medicina, Divisão de Doenças Infecciosas, Departamento de Medicina, Universidade Dalhousie e Queen Elizabeth II Health Sciences Center, Halifax, NS.
Silvia Munoz-Price, MD, PhD, professora de Medicina, Divisão de Doenças Infecciosas, Departamento de Medicina, Froedtert and the Medical College of Wisconsin, Milwaukee, WI.
Drs. Schaffzin, Johnston e Munoz-Price atuaram na força-tarefa para o desenvolvimento das Diretrizes da SHEA.
Referências
- Boyce JM, Havill NL, Otter JA, et al. Widespread environmental contamination associated with patients with diarrhea and methicillin-resistant Staphylococcus aureus colonization of the gastrointestinal tract. Infect Control Hosp Epidemiol. 2007;28:1142–1147.
- Bhalla A, Pultz NJ, Gries DM, et al. Acquisition of nosocomial pathogens on hands after contact with environmental surfaces near hospitalized patients. Infect Control Hosp Epidemiol. 2004;25:164–167.
- Olsen RJ, Lynch P, Coyle MB, et al. Examination gloves as barriers to hand contamination in clinical practice. JAMA. 1993;270:350–353.
- Tenorio AR, Badri SM, Sahgal NB, et al. Effectiveness of gloves in the prevention of hand carriage of vancomycin-resistant enterococcus species by health care workers after patient care. Clin Infect Dis. 2001;32:826–829.
- Huang SS, Datta R, Platt R. Risk of acquiring antibiotic-resistant bacteria from prior room occupants. Arch Intern Med. 2006;166:1945–1951.
- Donskey CJ. Does improving surface cleaning and disinfection reduce health care-associated infections? Am J Infect Control. 2013;41:S12–S19.
- Loftus RW, Brown JR, Patel HM, et al. Transmission dynamics of gram-negative bacterial pathogens in the anesthesia work area. Anesth Analg. 2015;120:819–826.
- Loftus RW, Koff MD, Brown JR, et al. The epidemiology of Staphylococcus aureus transmission in the anesthesia work area. Anesth Analg. 2015;120:807–818.
- Loftus RW, Koff MD, Brown JR, et al. The dynamics of Enterococcus transmission from bacterial reservoirs commonly encountered by anesthesia providers. Anesth Analg. 2015;120:827–836.
- Gargiulo DA, Mitchell SJ, Sheridan J, et al. Microbiological contamination of drugs during their administration for anesthesia in the operating Room. Anesthesiology. 2016;124:785–794.
- Loftus RW, Brown JR, Koff MD, et al. Multiple reservoirs contribute to intraoperative bacterial transmission. Anesth Analg. 2012;114:1236–1248.
- Mermel LA, Bert A, Chapin KC, et al. Intraoperative stopcock and manifold colonization of newly inserted peripheral intravenous catheters. Infect Control Hosp Epidemiol. 2014;35:1187–1189.
- Munoz-Price LS, Riley B, Banks S, et al. Frequency of interactions and hand disinfections among anesthesiologists while providing anesthesia care in the operating room: induction versus maintenance. Infect Control Hosp Epidemiol. 2014;35:1056–1059.
- Jefferson J, Whelan R, Dick B, et al. A novel technique for identifying opportunities to improve environmental hygiene in the operating room. AORN J. 2011;93:358–364.
- Loftus RW, Koff MD, Burchman CC, et al. Transmission of pathogenic bacterial organisms in the anesthesia work area. Anesthesiology. 2008;109:399–407.
- Birnbach DJ, Rosen LF, Fitzpatrick M, et al. The use of a novel technology to study dynamics of pathogen transmission in the operating room. Anesth Analg. 2015;120:844–847.
- Munoz-Price LS, Birnbach DJ, Lubarsky DA, et al. Decreasing operating room environmental pathogen contamination through improved cleaning practice. Infect Control Hosp Epidemiol. 2012;33:897–904.
- Rothstein DH, Raval MV. Operating room efficiency. Semi Pediatr Surg. 2018;27:79–85.
- Russ S, Arora S, Wharton R, et al. Measuring safety and efficiency in the operating room: development and validation of a metric for evaluating task execution in the operating room. J Am Coll Surg. 2013;216:472–481.
- Bhatt AS, Carlson GW, Deckers PJ. Improving operating room turnover time: a systems based approach. J Med Syst. 2014;38:148.
- World Health Organization. “WHO Guidelines on Hand Hygiene in Health Care.” World Health Organization 2009.
- Munoz-Price LS, Lubarsky DA, Arheart KL, et al. Interactions between anesthesiologists and the environment while providing anesthesia care in the operating room. Am J Infect Control. 2013;41:922–924.
- Munoz-Price LS, Patel Z, Banks S, et al. Randomized crossover study evaluating the effect of a hand sanitizer dispenser on the frequency of hand hygiene among anesthesiology staff in the operating room. Infect Control Hosp Epidemiol. 2014;35:717–720.
- Rodriguez-Aldrete D, Sivanesan E, Banks S, et al. Recurrent visual electronic hand hygiene reminders in the anesthesia work area. Infect Control Hosp Epidemiol. 2016;37:872–874.
- Koff MD, Loftus RW, Burchman CC, et al. Reduction in intraoperative bacterial contamination of peripheral intravenous tubing through the use of a novel device. Anesthesiology. 2009;110:978–985.
- Munoz-Price LS, Bowdle A, Johnston BL, et al. Infection prevention in the operating room anesthesia work area. Infect Control Hosp Epidemiol. 2019;40:1–17.


 Issue PDF
Issue PDF