يمكن أن يكون التثبيط التنفسي الناتج عن المواد الأفيونية من المضاعفات التي تشكل خطرًا على حياة الأطفال، حتى وإن كان من الممكن تفاديه. ويلزم التعرف على المعرضين لخطر التثبيط التنفسي الناتج عن المواد الأفيونية، ووضع ممارسات أكثر أمانًا، بما في ذلك استخدام العوامل المساعدة التي تقلل من استخدام المواد الأفيونية، وإجراء تقييمات متكررة للتهدئة، والمراقبة اليقظة. ولسوء الحظ، لم يتم تصميم أي نماذج للتنبؤ بخطر فشل معاوضة الجهاز التنفسي الناتجة عن المواد الأفيونية في الوقت الحالي لدى الأطفال، ومع ذلك فإن استخدام أجهزة العرض التكميلية المتعددة، قد يتيح تقليل الأحداث الخطيرة المتعلقة بالمواد الأفيونية.
 يمكن أن يحدث التثبيط التنفسي بعد الجراحة لأسباب متنوعة ويؤدي إلى مضاعفات قد تكون كارثية.1 أحد الأسباب المتكررة للتثبيط التنفسي في فترة ما بعد الجراحة هو استخدام المواد الأفيونية في الفترة المحيطة بالجراحة.2 بناءً على ذلك، وضعت المؤسسات والجمعيات المهنية، بما في ذلك مؤسسة التخدير وسلامة المرضى (APSF)، توصيات تتعلق بمراقبة المرضى3، 4 ونشرت مقالات تدعو إلى أن تكون القرارات المتعلقة بالمستوى المناسب من المراقبة بعد الجراحة مستندة إلى تقييم قبل الجراحة لعوامل الخطر الخاصة بالمريض.5 وكما هو الحال مع البالغين، تحدث مضاعفات تنفسية في الفترة المحيطة بالجراحة لدى المرضى الأطفال وتشكل سببًا شائعًا للأحداث السلبية التي تحدث بعد الجراحة.6 ومع ذلك، يجب أن نأخذ في الحسبان أن الأطفال ليسوا “بالغين صغارًا”. لذلك، يجب توخي الحذر عند استقراء الإرشادات والدراسات المنشورة سابقًا.
يمكن أن يحدث التثبيط التنفسي بعد الجراحة لأسباب متنوعة ويؤدي إلى مضاعفات قد تكون كارثية.1 أحد الأسباب المتكررة للتثبيط التنفسي في فترة ما بعد الجراحة هو استخدام المواد الأفيونية في الفترة المحيطة بالجراحة.2 بناءً على ذلك، وضعت المؤسسات والجمعيات المهنية، بما في ذلك مؤسسة التخدير وسلامة المرضى (APSF)، توصيات تتعلق بمراقبة المرضى3، 4 ونشرت مقالات تدعو إلى أن تكون القرارات المتعلقة بالمستوى المناسب من المراقبة بعد الجراحة مستندة إلى تقييم قبل الجراحة لعوامل الخطر الخاصة بالمريض.5 وكما هو الحال مع البالغين، تحدث مضاعفات تنفسية في الفترة المحيطة بالجراحة لدى المرضى الأطفال وتشكل سببًا شائعًا للأحداث السلبية التي تحدث بعد الجراحة.6 ومع ذلك، يجب أن نأخذ في الحسبان أن الأطفال ليسوا “بالغين صغارًا”. لذلك، يجب توخي الحذر عند استقراء الإرشادات والدراسات المنشورة سابقًا.
عوامل الخطر المرتبطة بالتثبيط التنفسي الناتج عن المواد الأفيونية لدى الأطفال
توجد مؤلفات محدودة متاحة تتناول عوامل الخطر المرتبطة بالتثبيط التنفسي الناتج عن المواد الأفيونية لدى الأطفال. وتُعَد الأمراض المصاحبة مثل داء السكري وأمراض القلب عوامل خطر كبيرة للإصابة بالحالات التنفسية الحرجة لدى البالغين بعد العلاج بالمواد الأفيونية عن طريق الحقن،7، 8 إلا أن معدل حدوثها المنخفض لدى الأطفال يجعل من غير المرجح أن تكون هذه الأمراض عوامل رئيسية في مجال طب الأطفال. ومن ناحية أخرى، ساعدت الأدلة المستمدة من عمليات التدقيق المتعلقة بالمرضى وتتبع بيانات إعطاء النالوكسون، وهو مؤشر بديل للتثبيط التنفسي الناتج عن المواد الأفيونية، على تحديد عوامل الخطر (الشكل 1). على سبيل المثال، حُددت الأمراض التنفسية الكامنة وتأخر النمو بوصفها أمراضًا مصاحبة قد تؤدي دورًا في زيادة خطر الإصابة بالتثبيط التنفسي الناتج عن المواد الأفيونية لدى الأطفال.9-11
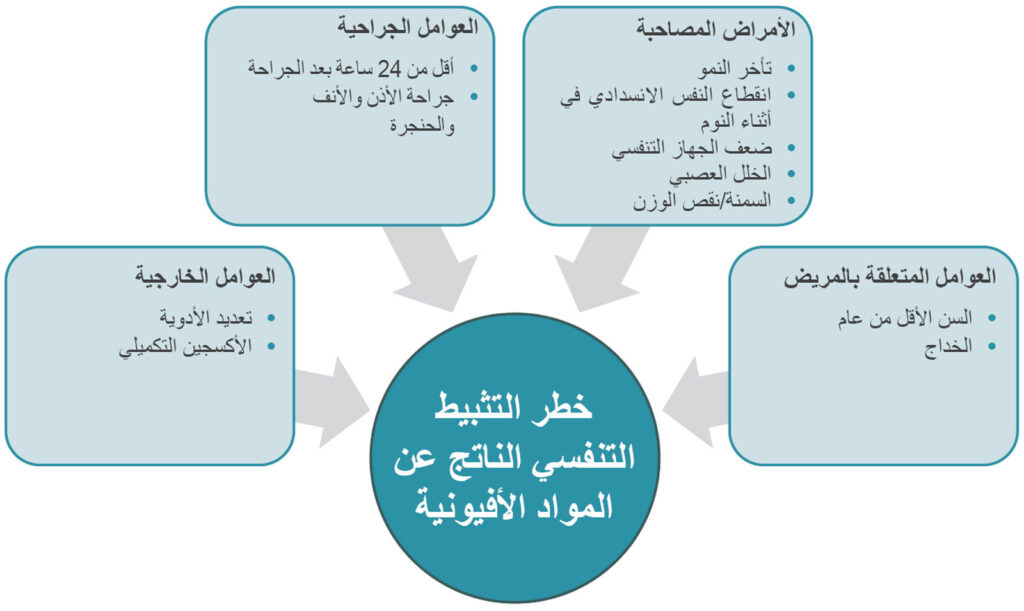
الشكل 1. ملخص لعوامل الخطر المرتبطة بزيادة خطر الإصابة بالتثبيط التنفسي الناتج عن المواد الأفيونية (OIRD) لدى الأطفال.4، 10
من عوامل الخطر الأخرى للإصابة بالتثبيط التنفسي الناتج عن المواد الأفيونية لدى الأطفال صغر السن. في مراجعة استرجاعية للمرضى الأطفال الذين احتاجوا إلى النالوكسون بسبب حالات تنفسية حرجة، ارتبط ارتفاع معدل الإصابة بصغر السن وكذلك بالخداج.10 وقد تُعزى زيادة خطر الإصابة إلى الاختلافات الفسيولوجية المتعلقة بعملية الاستقلاب وإخراج المواد الأفيونية بين الرضع الصغار والأطفال الأكبر سنًا والبالغين. على سبيل المثال، يطول العمر النصفي للمورفين ويقل معدل تخلص الجسم منه عند الأطفال حديثي الولادة. ومن ثَم، بناءً على الجرعات، قد تكون لدى الرضع الذين تقل سنهم عن شهر واحد مستويات أعلى من المصل تنخفض بشكل أبطأ مقارنةً بالمستويات لدى الأطفال الأكبر سنًا والبالغين، ما يعرضهم لمخاطر كبيرة.12
تم الإبلاغ أيضًا عن زيادة خطر الإصابة بالتثبيط التنفسي بعد الجراحة لدى الأطفال المصابين بانقطاع النفس الانسدادي في أثناء النوم13. بعد استئصال اللوزتين، يصبح الأطفال المصابون بانقطاع النفس الانسدادي الشديد في أثناء النوم أكثر حساسية للتثبيط التنفسي الناتج عن المورفين ويحتاجون إلى جرعات أقل من المورفين مقارنةً بالأطفال المصابين بانقطاع النفس الخفيف في أثناء النوم.14 يُعَد انقطاع النفس الانسدادي في أثناء النوم شائعًا نسبيًا في طب الأطفال، حيث يصيب 1-5% من الأطفال.15 ومع ذلك، يمكن أن تمثل عملية الفحص قبل الجراحة تحديًا بعض الشيء. يُعَد تخطيط النوم المعيار المثالي للتشخيص، ولكنه غير متاح لمعظم المرضى الأطفال. لا يوجد استبيان معتمد لتقييم المخاطر قابل للتطبيق على الأطفال من جميع الأعمار، ومع ذلك، تم الإبلاغ عن عوامل الخطر والأعراض الخاصة بانقطاع النفس الانسدادي في أثناء النوم لدى الأطفال.16
تُعَد السمنة في مرحلة الطفولة أيضًا أحد عوامل الخطر لإعطاء النالوكسون.10 ويمكن أن يُعزى ذلك إلى الارتباط القوي بين السمنة وانقطاع النفس الانسدادي في أثناء النوم، أو قد يعكس جرعات غير دقيقة تتعلق بالسمنة. على عكس البالغين، تُعَد الجرعات المعتمدة على الوزن ممارسة شائعة للعديد من الأدوية المخصصة للأطفال، ولكن جرعات المواد الأفيونية المعتمدة على الوزن الإجمالي للجسم يمكن أن تؤدي إلى تثبيط تنفسي خطير. لذلك، يجب أن تعتمد الجرعات على كتلة الجسم المثالية أو كتلة الجسم الخالي من الدهن.17 ومن المثير للاهتمام، أن نقص الوزن عند الأطفال هو عامل خطر للحالات التنفسية أيضًا.10
لوحظت التهدئة المفرطة قبل الإصابة بالأمراض المرتبطة بالمواد الأفيونية لدى غالبية الأطفال.4 في حين أن التأثيرات المهدئة للمواد الأفيونية معروفة جيدًا في المرضى غير المعتادين على المواد الأفيونية، فمن الممكن أن يتفاقم تثبيط الجهاز العصبي المركزي (CNS) بسبب الاستخدام المتزامن لمضادات القلق، ومرخيات العضلات، ومضادات التشنجات، وأدوية مهدئة أخرى. يمكن أن تؤدي هذه التركيبات إلى حالات تنفسية تهدد الحياة وزيادة خطر التدخلات باستخدام النالوکسون.10 ويتسم هذا الأمر بأهمية خاصة حيث تم الإبلاغ عن أن الاستخدام المتزامن للمواد الأفيونية ومثبطات الجهاز العصبي المركزي الأخرى أمر شائع في ممارسة طب الأطفال، حيث أفاد أكثر من 40% من المشاركين في استطلاع حول ممارسات إدارة الألم في طب الأطفال عام 2010 بأنهم يسمحون بالاستخدام المتزامن لهذه الأدوية.18 وعلى الرغم من أن الممارسة قد تكون قد تغيرت في العقد الماضي، فإن التركيز الأخير على تقليل استخدام المواد الأفيونية باستخدام أنظمة التسكين متعددة الأنماط يجعل من غير المرجح أن يكون هذا الاستخدام المتعدد للأدوية قد انخفض بشكل كبير.
يكون أعلى خطر للإصابة بالتثبيط التنفسي خلال اليوم الأول بعد الجراحة. في الواقع، 75% من النوبات التي تعرض لها الأطفال الذين تلقوا النالوكسون بسبب حالات تنفسية حرجة حدثت خلال أول 24 ساعة بعد الجراحة. حدثت الحالات لدى المرضى الذين تلقوا المواد الأفيونية عن طريق الوريد والفم والطرق العصبية المحورية، ما يشير إلى عدم وجود طريقة إعطاء خالية تمامًا من المخاطر.10
التوصيات الحالية لمراقبة المرضى الأطفال
خبراء يقترحون إجراء مراقبة مستمرة للأكسجة والتهوية لمدة لا تقل عن 24 ساعة بعد الجراحة في المرضى الأطفال الذين يتلقون المواد الأفيونية
لتقليل خطر الإصابة بالتثبيط التنفسي، طالما دعت مؤسسة APSF إلى استخدام المراقبة الإلكترونية المستمرة للأكسجة والتهوية، عند تقديم الأكسجين التكميلي، لتحديد حالات التثبيط التنفسي الناتج عن المواد الأفيونية بشكل استباقي ومنعها.3 على الرغم من عدم وجود دراسات تميز بشكل محدد متطلبات المراقبة للمرضى الأطفال، فإن بيان الإجماع الذي أيدته جمعية تخدير الأطفال يدعم ضرورة توخي الحذر بشكل أكبر عند رعاية مرضى معينين، منهم حديثو الولادة، والأطفال المصابون بانقطاع النفس الانسدادي في أثناء النوم، وأولئك المصابون بأمراض عصبية عضلية كامنة أو ضعف إدراكي يمكن أن يؤثر في وظيفة عضلات التنفس و/أو يعوق تقييم مستوى الألم أو الوعي لدى المريض. إضافةً إلى ذلك، ينبغي توخي مزيد من الحذر عندما يتعلق الأمر بمرضى أطفال يبدؤون العلاج بالمواد الأفيونية، وخاصةً في الفترة الأولى بعد الجراحة، وكذلك الذين يتلقون جرعات متزايدة من المواد الأفيونية عن طريق الحقن، وأولئك الذين يتلقون المواد الأفيونية بالتزامن مع مثبطات الجهاز العصبي المركزي الأخرى.4
تدعم آراء الخبراء مراقبة المرضى الأطفال الذين يتلقون الجرعات الأولية من المواد الأفيونية عن طريق الحقن أو المواد الأفيونية عبر نظام تسكين يتحكم فيه المريض (PCA)، و/أو نظام تسكين يتحكم فيه شخص بالنيابة عن المريض، و/أو التسريب المستمر، مع التوصية على وجه التحديد بمراقبة معدل التنفس وقياس التأكسج النبضي بشكل مستمر خلال أول 24 ساعة ما لم يكن المريض مستيقظًا وتتم مراقبته بنشاط.4، 12 تدعم الأبحاث السابقة استخدام المراقبة المستمرة بشكل أكثر تكرارًا لدى الأطفال. أفاد المشاركون في استطلاع أُجري عام 2010 حول ممارسات إدارة الألم في طب الأطفال أن المراقبة المستمرة لقياس التأكسج النبضي كانت شائعة عند تقديم المواد الأفيونية عبر نظام تسكين يتحكم فيه المريض.18 ومع ذلك، كانت المراقبة المستمرة لمعدل التنفس أقل استخدامًا بشكل ثابت (الشكل 2).
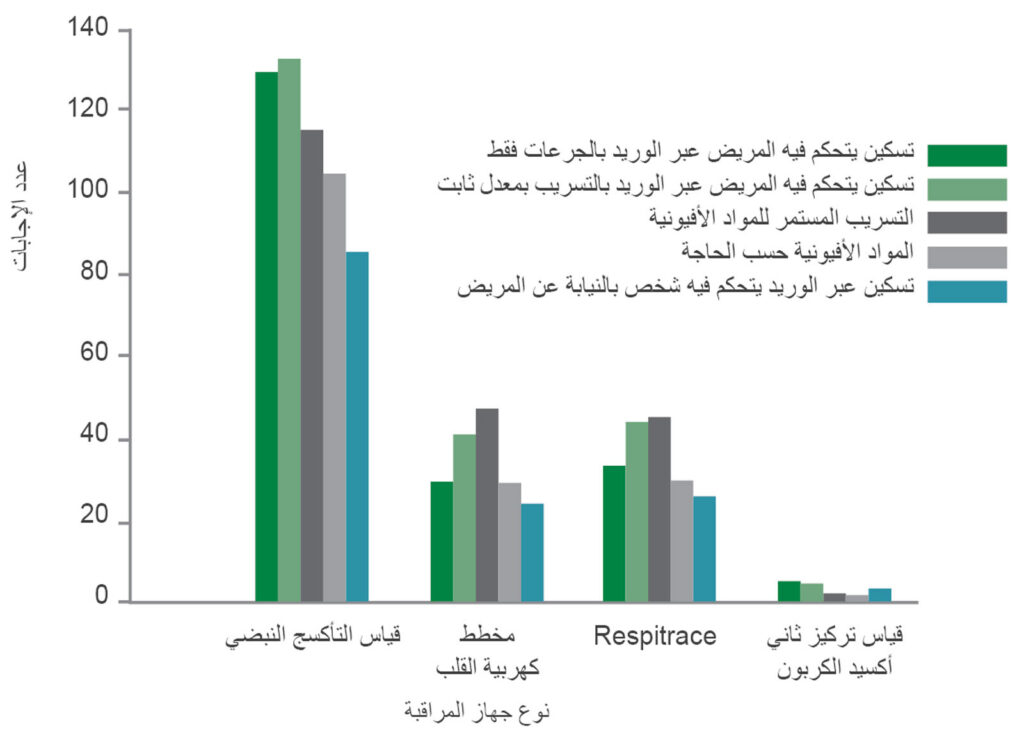
الشكل 2: نوع المراقبة المستخدمة عند إعطاء المواد الأفيونية للمرضى الأطفال. (إجمالي عدد المشاركين الذين أجابوا عن السؤال هو 149، وإجمالي عدد المشاركين الذين قدموا تسكينًا عبر الوريد يتحكم فيه شخص بالنيابة عن المريض هو 95.) أفاد تسعون في المئة من المشاركين بأنهم يستخدمون مراقبة قياس التأكسج النبضي عند إعطاء المرضى تسكينًا يتحكم فيه المريض. استُخدمت مراقبة تخطيط القلب الكهربائي وقياس تركيز ثاني أكسيد الكربون دائمًا بالتزامن مع قياس التأكسج النبضي، في حين أن تخطيط التحجم الحثي لجهاز التنفس (Respitrace) تم توفيره دائمًا تقريبًا بالتزامن مع قياس التأكسج النبضي (أقل من 90%)، ولكن استُخدم في بعض الأحيان كنوع وحيد من المراقبة.17 تمت إعادة الطباعة بإذن من Anesthesia & Analgesia وWolters Kluwer Health, Inc. Nelson KL, Yaster M, Kost-Byerly S, Monitto CL. A national survey of American Pediatric Anesthesiologists: patient-controlled analgesia and other intravenous opioid therapies in pediatric acute pain management. Anesth Analg. 2010;110:754–760.18
تتضمن التوصيات الإضافية من جمعية تخدير الأطفال بشأن استخدام المواد الأفيونية في الفترة المحيطة بالجراحة لدى الأطفال تقييمًا منتظمًا لمستوى التهدئة باستخدام مقياس تهدئة موثوق يقيِّم مستوى يقظة المريض، بدلاً من مقياس مصمم لمراقبة التهدئة الإجرائية. مقياس باسيرو للتهدئة بالمواد الأفيونية هو أحد الخيارات المتاحة.19 يُنصح بإدخال المرضى إلى بيئة تخضع لمراقبة عالية، مثل وحدة الرعاية المتوسطة، أو وحدة عناية ما بعد التخدير، أو وحدة العناية المركزة، عند بدء استخدام المسكنات الأفيونية لدى الرضع الذين تقل سنهم عن ثلاثة أشهر. يوصى أيضًا بالنظر في المراقبة المستمرة لمعدل التنفس وتخطيط كهربية القلب للمرضى الأطفال الذين يتلقون علاج الأكسجين، حيث إن الأكسجين التكميلي قد يؤثر في حساسية جهاز قياس التأكسج النبضي ووقت استجابته وهو جهاز يراقب حالات انقطاع النفس/ضعف التنفس.4
مراقبة الجهاز التنفسي لدى الأطفال والتحديات المرتبطة بها
انخفاض تشبع الأكسجين يمكن أن يكون علامة تحذيرية متأخرة على القصور التنفسي عندما يتلقى المرضى الأكسجين
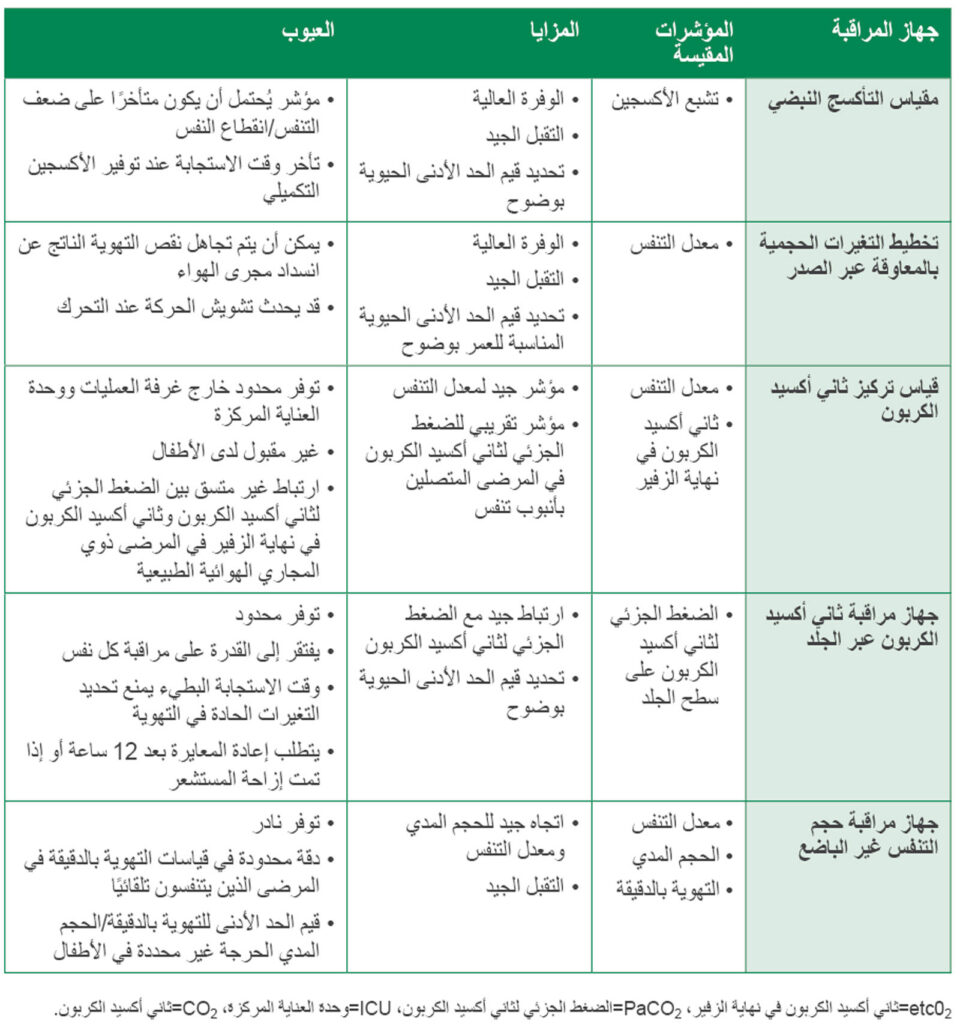
كما هو الحال مع البالغين، يجب أن تحدد مراقبة الجهاز التنفسي لدى الأطفال حالات التثبيط التنفسي الناتج عن المواد الأفيونية بشكل استباقي وفي الوقت المناسب للتدخل ومنع حدوث حالات حرجة. في الوضع المثالي، ينبغي لمراقبة الجهاز التنفسي أن تقيس الأكسجة ومعدل التنفس وضغط ثاني أكسيد الكربون (2CO)، وتدفق الهواء بشكل مستمر ودقيق. توجد حاليًا أجهزة مراقبة لتتبع كل مؤشر، ولكن لكل منها قيود في ما يخص التنبؤ بفشل الجهاز التنفسي الوشيك (الجدول 1).
الجدول 1: ملخص لأساليب مراقبة التنفس لاكتشاف التثبيط التنفسي الناتج عن المواد الأفيونية.2، 4، 6، 7، 20-23
أكثر طرق المراقبة شيوعًا في ممارسة طب الأطفال هي قياس التأكسج النبضي المستمر وتخطيط التغيرات الحجمية بالمعاوقة عبر الصدر. قدم قياس التأكسج النبضي منذ إدخاله في ممارسة طب الأطفال في الثمانينيات معلومات حيوية حول كفاية الأكسجة عند الرضع والأطفال. تتوفر عادةً مراقبة قياس التأكسج النبضي في وحدات الأطفال، ويتقبل المرضى من جميع الأعمار المراقبة نفسها بشكل جيد. ومع ذلك، يمكن أن يكون انخفاض تشبع الأكسجين علامة تحذيرية متأخرة على القصور التنفسي، خصوصًا عندما يتلقى المرضى الأكسجين التكميلي.4 ولسوء الحظ، تشير الدراسات إلى وجود حاجة متكررة إلى الأكسجين التكميلي للحفاظ على كفاية الأكسجة بعد الجراحة، سواء بسبب التعقيد الجراحي أو الأمراض المصاحبة لدى المريض أو إعطاء المسكنات.11، 18 وتعرض هذه الحاجة الأطفال لخطر متزايد للإصابة بنقص التهوية غير الملحوظ من خلال زيادة الوقت بين انقطاع النفس/ضعف التنفس وانخفاض تشبع الأكسجين.
من الأساليب المتوفرة أيضًا والمقبولة مراقبة معدل التنفس باستخدام تخطيط التغيرات الحجمية بالمعاوقة عبر الصدر، وهي تقنية يمكنها تحديد انقطاع النفس وضعف التنفس، وهما علامتان مميزتان لتأثير المواد الأفيونية في مراكز التنفس في جذع الدماغ. ومع ذلك، يجب توخي الحذر لاستخدام مؤشرات التنفس المناسبة للعمر. لسوء الحظ، قد تكون مراقبة معدل التنفس باستخدام هذه التقنية غير دقيقة بسبب وضع الأقطاب الكهربائية في مخطط كهربية القلب بشكل غير مثالي، وتشويش الحركة، والحالات الفسيولوجية التي تسبب حركة جدار الصدر، مثل السعال والبكاء. إضافةً إلى ذلك، قد تفشل هذه التقنية في تحديد القصور التنفسي في حال وجود انسداد في مجرى الهواء لم يُشَخَّص بعد.
يوفر قياس الضغط الجزئي لثاني أكسيد الكربون الشرياني (PaCO2) تقييمًا موثوقًا للتهوية، ولكنه يتطلب الوصول إلى الشرايين ولا يقدم معلومات بشكل مستمر. تشمل القياسات البديلة غير الباضعة للضغط الجزئي لثاني أكسيد الكربون التي توفر بيانات مستمرة مراقبة الضغط الجزئي لثاني أكسيد الكربون عبر الجلد وفي نهاية الزفير (etCO2). تراجعت شعبية مراقبة الغاز عبر الجلد في الثمانينيات جزئيًا بسبب التحديات التقنية، بما في ذلك خطر حروق الجلد عند استخدامها على حديثي الولادة. ولكن نتيجة للتقدم التقني، أصبحت مراقبة الضغط الجزئي لثاني أكسيد الكربون عبر الجلد الآن قابلة للتطبيق سريريًا وآمنة. تم تقييم أجهزة المراقبة هذه في فئة الأطفال،20 لكن لم تتم دراستها في الرضع والأطفال الذين يتلقون أدوية أفيونية في مرحلة ما بعد الجراحة. وعلى الرغم من أن علاقة الترابط في هذه الأجهزة تكون جيدة مع الضغط الجزئي لثاني أكسيد الكربون في الحالة المستقرة، فإن زمن الاستجابة يمنع التعرف السريع على التغيرات الحادة في التهوية، ما يحد من فائدتها كأجهزة مراقبة للتحذير المبكر.
يجب استخدام قياس تركيز ثاني أكسيد الكربون عند تقديم الأكسجين التكميلي إلى المرضى الذين يتلقون المواد الأفيونية بعد الجراحة
على الجانب الآخر، توفر أجهزة مراقبة ثاني أكسيد الكربون في نهاية الزفير (etCO2) تحذيرات مبكرة وموثوقة من قصور التهوية عند استخدامها لمراقبة المرضى المتصلين بأنبوب تنفس أو المرضى الذين تم تخديرهم أو الواقعين تحت تأثير مهدئ عميق. تمت دراسة قياس تركيز ثاني أكسيد الكربون بأخذ عينات من الأنف والفم في البالغين غير المتصلين بأنبوب تنفس الذين يتلقون تسكينًا يتحكم فيه المريض2، 7 وهو مؤشر أكثر حساسية على وجود خلل في الجهاز التنفسي مقارنةً بمراقبة تشبع الأكسجين، ما يدعم إمكانية استخدام قياس تركيز ثاني أكسيد الكربون كطريقة مراقبة للتحذير المبكر من القصور التنفسي الوشيك. في ضوء هذه النتائج، أوصت مؤسسة APSF باستخدام قياس تركيز ثاني أكسيد الكربون لمراقبة التهوية عند توفير الأكسجين التكميلي بعد الجراحة للمرضى الذين يتلقون أدوية أفيونية. ومع ذلك، يتطلب الاستخدام المناسب تعاون المريض في ارتداء القنية المصممة خصوصًا لقياس تركيز ثاني أكسيد الكربون لفترات طويلة من أجل اكتشاف الأحجام المدية المنخفضة الخارجة من كل من الفم والأنف. يمكن أن تكون هذه القنيات غير مريحة أو تتداخل مع أنشطة مثل الأكل أو التحدث، ما يؤثر في التزام المرضى. وعندما تمت دراسة قياس تركيز ثاني أكسيد الكربون في المرضى الأطفال غير المتصلين بأنبوب تنفس وغير الخاضعين لتأثير مهدئ بعد الجراحة، كان في كثير من الأحيان غير مقبول بسبب هذه الأسباب، ما يحد من تنفيذه في أنظمة مراقبة الأطفال.21
إن الفهم الواضح للمعلومات التي توفرها مراقبة تركيز ثاني أكسيد الكربون أمر ضروري. يوفر قياس تركيز ثاني أكسيد الكربون مقياسًا دقيقًا لمعدل التنفس، إلا أن معنى قيم قياس ثاني أكسيد الكربون في نهاية الزفير قد يختلف بشكل كبير بين المرضى ذوي المجرى الهوائي الطبيعي أو الصناعي. كما ذُكر في تجربة PRODIGY، تعرض أكثر من 60% من المرضى الذين خضعوا للمراقبة لنوبات انخفاض ثاني أكسيد الكربون في نهاية الزفير إلى أقل من 15 ملم زئبق (أكثر من 50% كان لديهم انخفاض في ثاني أكسيد الكربون في نهاية الزفير وانخفاض في معدل التنفس)، ولكن لم يواجه أي مريض ارتفاعًا في ثاني أكسيد الكربون في نهاية الزفير إلى أكثر من 60 ملم زئبق.7 تشير هذه النتائج إلى أنه في العديد من الحالات، لم تعكس قيم ثاني أكسيد الكربون في نهاية الزفير الضغط الجزئي لثاني أكسيد الكربون، بل كانت مؤشرًا بديلاً على ضعف تدفق الهواء بسبب انسداد غير معروف.
قد توفر التقنيات الأحدث، مثل مراقبة حجم التنفس غير الباضعة، تقييمًا أكثر حساسية لتدفق الهواء، وتحديدًا الحجم المدي والتهوية بالدقيقة. تم التحقق من صحة أجهزة المراقبة لدى كل من البالغين والرضع والأطفال المتصلين بأنبوب تنفس والخاضعين للتهوية الميكانيكية تحت التخدير العام.6، 22 ومع ذلك، عند البالغين الذين يتنفسون تلقائيًا، كان الحجم المدي واتجاه معدل التنفس جيدين، لكن دقة قياسات التهوية بالدقيقة كانت محدودة مقارنةً بالمعيار المثالي، وهو قياس التنفس.23 وعلى الرغم من ذلك، فإن مراقبة الاتجاه التي يمكن أن توفرها هذه الأجهزة قد تدعم إدراجها في إستراتيجيات المراقبة المستقبلية. تشير البيانات الأولية من دراسة تجريبية على المراهقين الذين يتلقون مواد أفيونية عبر نظام تسكين يتحكم فيه المريض بعد جراحة دمج الفقرات الخلفي (الشكل 3) إلى أن أجهزة المراقبة مقبولة لدى المراهقين (تواصل شخصي مع C. Monitto)، ما يعني أن استخدامها في نماذج مراقبة الأطفال قابل للتطبيق. ومع ذلك، فإن القيم الحيوية للحد الأدنى للتهوية التي يمكن استخدامها للتنبؤ بحدوث خلل وشيك في الجهاز التنفسي، أو اكتشاف خلل حالي غير ملحوظ، لم تُحدد بوضوح عند الأطفال حتى الآن.
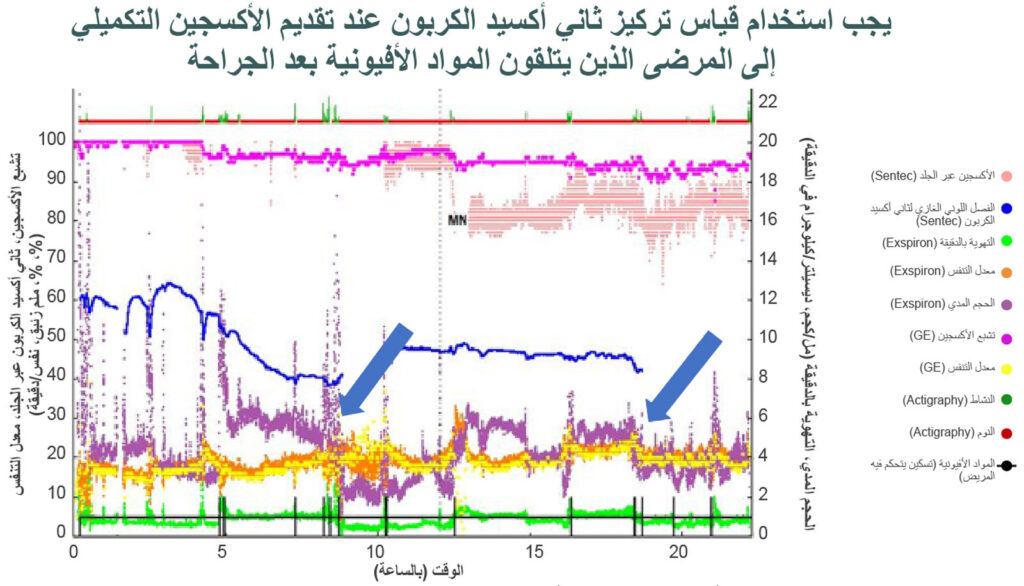
الشكل 3: تدفق بيانات على مدار 24 ساعة لمستويات تشبع الأكسجين، ومعدل التنفس، وثاني أكسيد الكربون عبر الجلد، والتهوية بالدقيقة، والحجم المدي، وتخطيط الحركة (actigraphy)، واستخدام المواد الأفيونية من خلال تسكين يتحكم فيه المريض لدى المرضى المراهقين بعد دمج الفقرات الخلفي. تم إظهار انخفاض الحجم المدي (TV) بعد استخدام جرعات تسكين يتحكم فيه المريض بسهمين باللون الأزرق. يشير الاختصار MN إلى منتصف الليل. (بيانات غير منشورة من Constance Monitto).
في الختام، لا توجد نماذج مصممة للتنبؤ بمخاطر تدهور الجهاز التنفسي الناتج عن المواد الأفيونية لدى الأطفال حاليًا. عند تصنيف المخاطر، يجب تضمين العوامل الخاصة بالمرضى التي ينفرد بها الأطفال بدلاً من الاعتماد على نتائج الدراسات التي أجريت على البالغين. تشير التقارير إلى أن المراقبة التنفسية الإلكترونية المستمرة للأطفال تُستخدم بشكل أكثر شيوعًا مقارنةً بالبالغين، لكن لا توجد تقنية واحدة توفر حلاً شاملاً لمراقبة الأشخاص ذوي المجاري الهوائية الطبيعية. في المستقبل، قد يؤدي استخدام عدة أجهزة مراقبة متكاملة بالتزامن مع نماذج مصممة لتضمين مؤشرات إنذار للحدود الخاصة بالأطفال إلى تمكين تحديد نوبات القصور التنفسي في هذه الفئة الضعيفة في وقت مبكر.
Tricia Vecchione، MD، MPH، أستاذة مساعدة في قسم التخدير في كلية الطب بجامعة جونز هوبكينز، بالتيمور، ماريلاند.
Constance L. Monitto، MD، أستاذة مساعدة في قسم التخدير في كلية الطب بجامعة جونز هوبكينز، بالتيمور، ماريلاند.
ليس لدى المؤلفين تضارب في المصالح.
المراجع
- Lee LA, Caplan RA, Stephens LS, et al. Postoperative opioid-induced respiratory depression: a closed claims analysis. Anesthesiology. 2015;122:659–665. PMID: 25536092.
- Overdyk FJ, Carter R, Maddox RR, et al. Continuous oximetry/capnometry monitoring reveals frequent desaturation and bradypnea during patient-controlled analgesia. Anesth Analg. 2007;105:412–418. PMID: 17646499.
- Weinger MB, Lee LA. “No patient shall be harmed by opioid-induced respiratory depression.” APSF Newsletter. 2011;26:21–40. https://www.apsf.org/article/no-patient-shall-be-harmed-by-opioid-induced-respiratory-depression/. Accessed February 28, 2024.
- Cravero JP, Agarwal R, Berde C, et al. The Society for Pediatric Anesthesia recommendations for the use of opioids in children during the perioperative period. Paediatr Anaesth. 2019;29:547–571. PMID: 30929307.
- Weingarten TN. Opioid-induced respiratory depression–beyond sleep disordered breathing. APSF Newsletter. 2023;38:2,42–45. https://www.apsf.org/article/opioid-induced-respiratory-depression-beyond-sleep-disordered-breathing/. Accessed February 28, 2024.
- Gomez-Morad AD, Cravero JP, Harvey BC, et al. The evaluation of a noninvasive respiratory volume monitor in pediatric patients undergoing general anesthesia. Anesth Analg. 2017;125:1913–1919. PMID: 28759491.
- Khanna AK, Bergese SD, Jungquist CR, et al. PRediction of Opioid-induced respiratory Depression In patients monitored by capnoGraphY (PRODIGY) group collaborators. prediction of opioid-induced respiratory depression on inpatient wards using continuous capnography and oximetry: an international prospective, observational trial. Anesth Analg. 2020;131:1012–1024. PMID: 32925318.
- Ramachandran SK, Haider N, Saran KA, et al. Life threatening critical respiratory events: a retrospective study of postoperative patients found unresponsive during analgesic therapy. J Clin Anesth. 2011;23:207–213. PMID: 21570616.
- Morton NS, Errera A. APA national audit of pediatric opioid infusions. Paediatr Anaesth. 2010;20:119–125. PMID: 19889193.
- Chidambaran V, Olbrecht V, Hossain M, et al. Risk predictors of opioid-induced critical respiratory events in children: naloxone use as a quality measure of opioid safety. Pain Med. 2014;15:2139–2149. PMID: 25319840.
- Voepel-Lewis T, Marinkovic A, Kostrzewa A, et al. The prevalence of and risk factors for adverse events in children receiving patient-controlled analgesia by proxy or patient-controlled analgesia after surgery. Anesth Analg. 2008; 107:70–75. PMID: 18635469.
- Monitto CL, George JA, Yaster M: Pediatric acute pain management. In: Davis PJ, Cladis FP (eds). Smith’s anesthesia for infants and children. 10th edition. Elsevier, Philadelphia, PA, 481–518, 2022.
- Chung F, Liao P, Elsaid H, et al. Factors associated with postoperative exacerbation of sleep-disordered breathing. Anesthesiology. 2014;120:299–311. PMID: 24158050.
- Brown KA, Laferriere A, Moss IR. Recurrent hypoxemia in young children with obstructive sleep apnea is associated with reduced opioid requirement for analgesia. Anesthesiology. 2004;100:806–810. PMID: 15087614.
- Marcus CL, Brooks LJ, Draper KA, et al. Diagnosis and management of childhood obstructive sleep apnea syndrome. Pediatrics. 2012;130:576–584. PMID: 22926173.
- Coté CJ, Posner KL, Domino KB. Death or neurologic injury after tonsillectomy in children with a focus on obstructive sleep apnea: Houston, we have a problem! Anesth Analg. 2014;118:1276–1283. PMID: 23842193.
- Mortensen A, Lenz K, Abildstrom H, Lauritsen TL. Anesthetizing the obese child. Paediatr Anaesth. 2011;21:623–629. PMID: 21429056.
- Nelson KL, Yaster M, Kost-Byerly S, Monitto CL. A national survey of American pediatric anesthesiologists: patient-controlled analgesia and other intravenous opioid therapies in pediatric acute pain management. Anesth Analg. 2010;110:754–760. PMID: 20185654.
- Quinlan-Colwell A, Thear G, Miller-Baldwin E, Smith A. Use of the Pasero Opioid-induced Sedation Scale (POSS) in pediatric patients. J Pediatr Nurs. 2017;33:83–87. PMID: 28209260.
- Berkenbosch JW, Tobias JD. Transcutaneous carbon dioxide monitoring during high-frequency oscillatory ventilation in infants and children. Crit Care Med. 2002;30:1024–1027. PMID: 12006797.
- Miller KM, Kim AY, Yaster M, et al. Long-term tolerability of capnography and respiratory inductance plethysmography for respiratory monitoring in pediatric patients treated with patient-controlled analgesia. Paediatr Anaesth. 2015; 25:1054–1059. PMID: 26040512.
- Atkinson DB, Sens BA, Bernier RS, et al. The evaluation of a noninvasive respiratory volume monitor in mechanically ventilated neonates and infants. Anesth Analg. 2022; 134:141–148. PMID: 33929346.
- Gatti S, Rezoagli E, Madotto F, et al. A non-invasive continuous and real-time volumetric monitoring in spontaneous breathing subjects based on bioimpedance-ExSpiron®Xi: a validation study in healthy volunteers. J Clin Monit Comput. 2024;38:539–551. PMID: 38238635.